ATP, NAD A FAD
ATP
Buňky používají jako zdroj energie molekulu zvanou adenosintrifosfát (neboli ATP) (viz obrázek 2). Fosfáty v této molekule mohou dodávat energii substrátům v našich buňkách. V našich buňkách existují enzymy, které mohou odstranit fosfát z ATP a připojit ho k jiné molekule – obvykle k bílkovině (viz obrázek 3). Když k tomu dojde, říkáme, že protein byl fosforylován. Představte si třetí fosfát jako malý pytlík energie. Když je přenesen na bílkovinu, může být tato energie k něčemu použita. Například na obrázku 3 protein změní svůj tvar, když se stane fosforylovaným. Když bílkoviny mění svůj tvar, často tomu říkáme konformační změna struktury bílkoviny. V těle existuje mnoho proteinů, které využívají fosfát z ATP k vyvolání konformační změny. Tato změna tvaru bílkoviny nakonec umožňuje takové věci, jako je svalová kontrakce, pohyblivost buněk, membránový transport a činnost enzymů. Buňky a život existují pouze tehdy, je-li k dispozici stálý a trvalý přísun ATP.
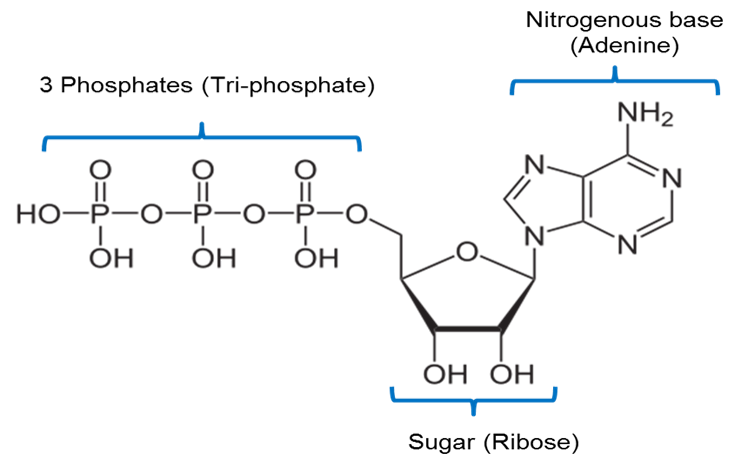
Obrázek vytvořil JS na BYU Idaho F2013.
Výše uvedený obrázek znázorňuje chemickou strukturu ATP. ATP obsahuje dusíkatou bázi zvanou adenin spojenou s pětiuhlíkatým cukrem zvaným ribóza a 3 fosfátové skupiny.
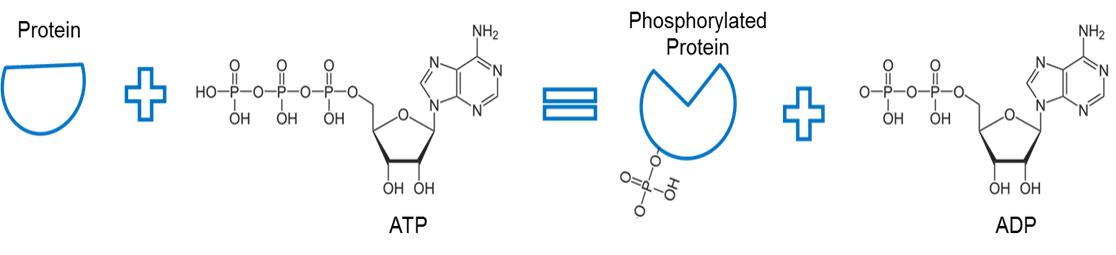
Obrázek vytvořil JS na BYU Idaho F2013.
ATP se používá k fosforylaci bílkovin. Enzym zvaný kináza (není zobrazen) odstraní fosfát z ATP a usnadní vazbu mezi fosfátem a nějakým jiným proteinem. Takové spojení fosfátu s bílkovinou se nazývá fosforylace. Fosfátová kost s bílkovinou má vyšší energii. Všimněte si, že fosforylace využívá tuto energii k vyvolání konformační změny tvaru bílkoviny.
NAD a FAD
Nikotinamidadenindinukleotid (NAD) a flavinadenindinukleotid (FAD) jsou koenzymy účastnící se vratných oxidačních a redukčních reakcí. Často se uvádí, že tyto sloučeniny jsou přenašeči elektronů, protože přijímají elektrony (stávají se redukovanými) během katabolických kroků při rozkladu organických molekul, jako jsou sacharidy a lipidy. Tyto redukované koenzymy pak mohou tyto elektrony odevzdat některé jiné biochemické reakci, která se obvykle účastní procesu, který je anabolický (například syntéza ATP).
NAD+ / NADH
Nikotinamidadenindinukleotid se v oxidovaném stavu nazývá NAD+, po redukci (neboli přijetí elektronů) se označuje jako NADH. Molekulární znázornění viz obrázek 4. K získání této sloučeniny se používá vitamin niacin (nazývaný také B3). Niacin poskytuje organickou kruhovou strukturu, která se bude přímo podílet na přenosu atomu vodíku a 2 elektronů. NAD+ se často vyskytuje ve spojení s enzymem „dehydrogenáza“. Dehydrogenázová reakce odstraňuje dva atomy vodíku; jeden jako hydrid (:H-) (hydrid je atom vodíku se 2 elektrony) a jeden jako vodíkový kation (H+) (a vodíkový kation samozřejmě nemá žádné elektrony). Hydrid se váže s NAD+ a vytváří redukovanou sloučeninu niktinamid adenindinukleotidu (NADH). Druhý atom vodíku (H+) se uvolní do roztoku viz obrázek 4.
Při zkoumání reakcí pro metabolismus hledejte reakce, při kterých vzniká NADH. NADH bude důležitý, protože bude dodávat vodíky a elektrony, které získá, biochemickým procesům, které mohou využít elektrony a vodíky k výrobě ATP.
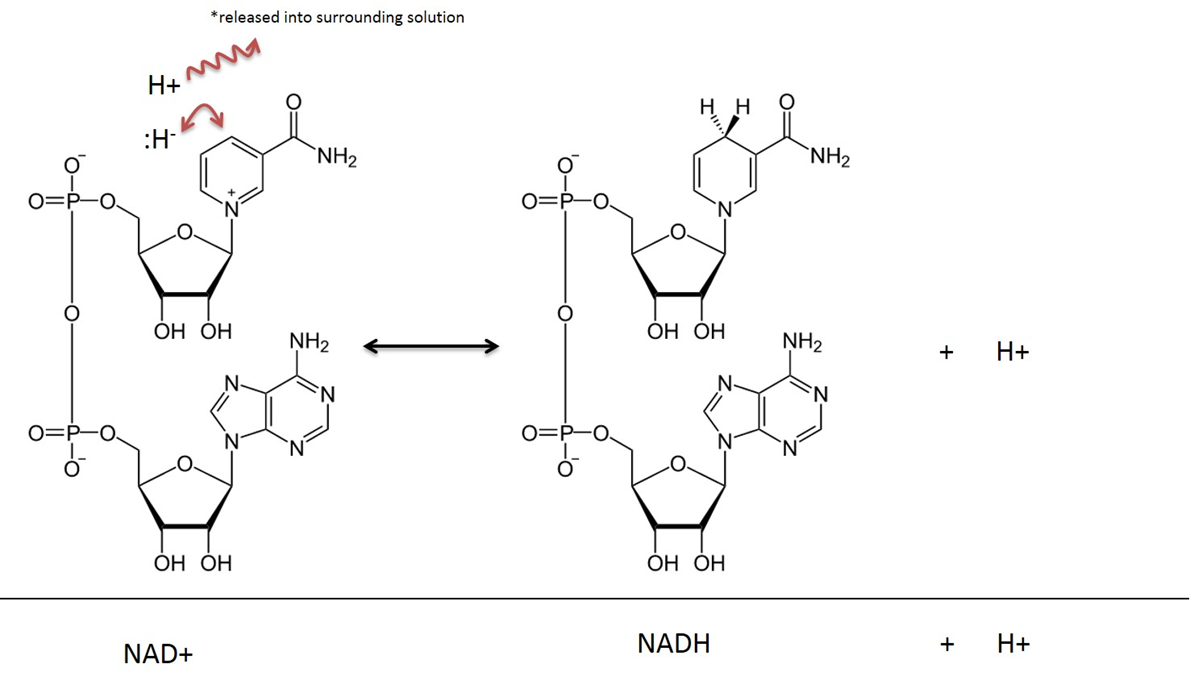
Obrázek vytvořil JS na BYU Idaho F2013.
V metabolických reakcích, které zahrnují NAD, jsou dva atomy vodíku a dva elektrony odebrány ze substrátu a přeneseny na NAD+. NAD+ přijme hydridový ion (vodík se dvěma elektrony) a stane se nikotinamidadenindinukleotidem v redukované formě (NADH). Vodíkový kationt, který je při reakci rovněž zachycen, se uvolní do okolního roztoku. Nezapomeňte, že tato reakce je vratná.
Při vysvětlování reakcí, které probíhají v Metabolismu, se běžně ignoruje H+ uvolněný do roztoku a v tomto textu bude výsledek redukce NAD znázorněn jednoduše jako NADH, nikoliv NADH + H+.
FAD / FADH2
Flavin adenindinukleotid v oxidovaném stavu se nazývá FAD. Po redukci se nazývá FADH2. Molekulární znázornění viz obrázek 5. K získání této sloučeniny se používá vitamin riboflavin (nebo B2). Riboflavin poskytuje kruhové struktury, které se budou přímo podílet na přenosu dvou atomů vodíku (tentokrát každý s jedním elektronem). Podobně jako NAD funguje FAD ve spojení s enzymem „dehydrogenázou“. Reakce odstraní dva atomy vodíku; každý proton s jedním elektronem. Oba atomy vodíku se spojí s FAD. Při této reakci se neuvolňuje H+ do roztoku jako při redukci NAD.
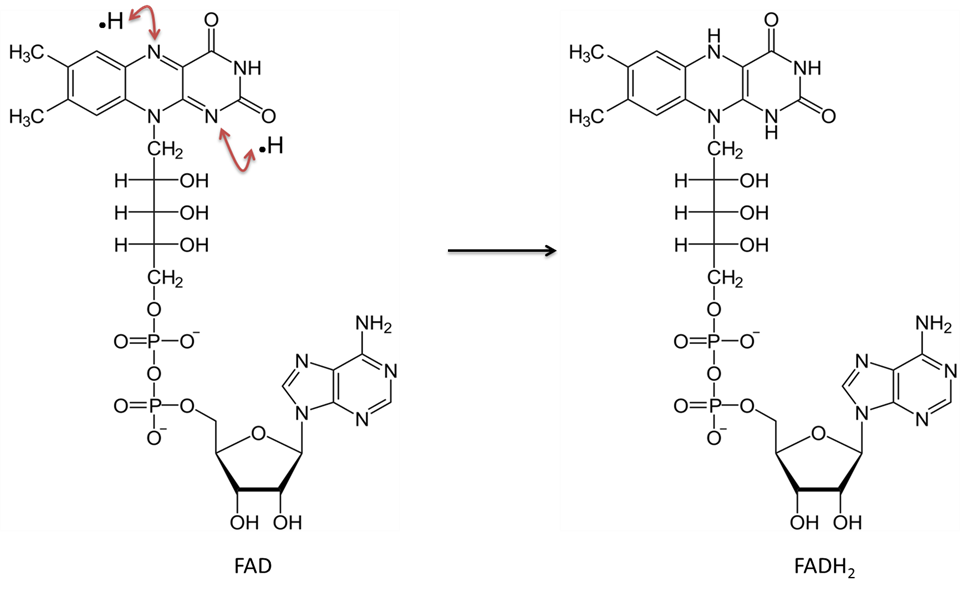
Obrázek vytvořil JS na BYU Idaho F2013.
Flavin adenindinukleotid v oxidované formě (FAD) přijme dva atomy vodíku (každý s jedním elektronem) a stane se FADH2.
Při zkoumání reakcí pro metabolismus hledejte reakci, při které vzniká FADH2. Podobně jako NADH bude FADH2 důležitý, protože bude dodávat vodíky a elektrony biochemickým procesům, které mohou využít elektrony a vodíky k tvorbě ATP.
**Níže uvedenými tlačítky můžete přejít na další nebo předchozí čtení v tomto modulu**

