Generischer Name: Phendimetrazintartrat
Dosierungsform: Tablette
Medically reviewed by Drugs.com. Zuletzt aktualisiert am 22. Juni 2020.
- Übersicht
- Nebenwirkungen
- Dosierung
- Professional
- Interaktionen
- Mehr
Rx only
Der Markenname Bontril Slow Release wurde in den U.S. Wenn generische Versionen dieses Produkts von der FDA zugelassen wurden, können generische Äquivalente verfügbar sein.
- Bontril-Beschreibung
- Bontril – Klinische Pharmakologie
- Indikationen und Anwendung von Bontril
- Kontraindikationen
- Warnhinweise
- Vorsichtsmaßnahmen
- Wechselwirkungen mit anderen Arzneimitteln
- Karzinogenese, Mutagenese, Beeinträchtigung der Fertilität
- Schwangerschaft
- Verwendung in der Schwangerschaft
- Stillende Mütter
- Anwendung bei Kindern
- Nebenwirkungen
- Drogenmissbrauch und Abhängigkeit
- Kontrollierte Substanz
- Abhängigkeit
- Überdosierung
- Bontril Dosierung und Verabreichung
- Normale Dosierung für Erwachsene
- Wie wird Bontril geliefert
- Hauptanzeigefeld – 35 mg Tabletten Flaschenetikett
- Mehr über Bontril Slow Release (Phendimetrazin)
- Verbraucherinformationen
- Fachinformationen
- Verwandte Behandlungsleitfäden
Bontril-Beschreibung
Phendimetrazintartrat hat als Dextro-Isomer die chemische Bezeichnung (2S,3S)-3,4-Dimethyl-2-phenylmorpholin L-(+)-tartrat (1:1).
Die Strukturformel lautet:
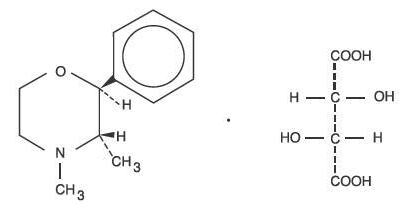
C12H17NO-C4H6O6 M.W. 341.36
Phendimetrazintartrat ist ein weißes, geruchloses kristallines Pulver. Es ist gut löslich in Wasser, schwer löslich in warmem Alkohol, unlöslich in Chloroform, Aceton, Ether und Benzol.
Außerdem sind folgende inaktive Bestandteile enthalten: Puderzucker, Puderzucker, D&C Gelb #10, FD&C Blau #1, FD&C Gelb #6, Isopropylalkohol, Lactose wasserfrei, Magnesiumstearat, mikrokristalline Cellulose, Povidon, gereinigtes Wasser, Natriumstärkeglycolat.
Bontril – Klinische Pharmakologie
Phendimetrazintartrat ist ein sympathomimetisches Amin mit ähnlicher pharmakologischer Aktivität wie die Prototyp-Medikamente dieser Klasse, die bei Fettleibigkeit eingesetzt werden, die Amphetamine. Zu den Wirkungen gehören die Stimulation des zentralen Nervensystems und die Erhöhung des Blutdrucks. Tachyphylaxie und Toleranz wurden bei allen Arzneimitteln dieser Klasse, bei denen diese Phänomene untersucht wurden, nachgewiesen.
Die bei Fettleibigkeit eingesetzten Arzneimittel dieser Klasse werden gemeinhin als „Anorektika“ oder „Anorexigenika“ bezeichnet. Es ist jedoch nicht erwiesen, dass die Wirkung solcher Medikamente bei der Behandlung von Fettleibigkeit in erster Linie in der Unterdrückung des Appetits besteht. Andere Wirkungen des Zentralnervensystems oder metabolische Wirkungen können zum Beispiel beteiligt sein.
Erwachsene fettleibige Personen, die in eine Diät eingewiesen und mit anorektischen Arzneimitteln behandelt werden, verlieren im Durchschnitt mehr Gewicht als diejenigen, die mit Placebo und Diät behandelt werden, wie in relativ kurzfristigen klinischen Studien festgestellt wurde.
Das Ausmaß des erhöhten Gewichtsverlustes der mit Arzneimitteln behandelten Patienten gegenüber den mit Placebo behandelten Patienten beträgt nur einen Bruchteil eines Pfundes pro Woche. Der Gewichtsverlust ist in den ersten Wochen der Therapie sowohl bei den Medikamenten- als auch bei den Placebo-Patienten am größten und nimmt in den darauffolgenden Wochen tendenziell ab. Der mögliche Grund für den erhöhten Gewichtsverlust, der auf die verschiedenen Wirkungen des Medikaments zurückzuführen ist, ist nicht bekannt. Das Ausmaß des mit der Einnahme eines anorektischen Medikaments verbundenen Gewichtsverlusts variiert von Studie zu Studie, und der erhöhte Gewichtsverlust scheint zum Teil mit anderen Variablen als dem verordneten Medikament zusammenzuhängen, z. B. mit dem Prüfarzt, der behandelten Population und der verordneten Diät. Die Studien lassen keine Rückschlüsse auf die relative Bedeutung der medikamentösen und nichtmedikamentösen Faktoren für die Gewichtsabnahme zu.
Der natürliche Verlauf der Fettleibigkeit wird in Jahren gemessen, während die zitierten Studien auf eine Dauer von wenigen Wochen beschränkt sind; daher muss die Gesamtwirkung der medikamenteninduzierten Gewichtsabnahme gegenüber der alleinigen Diät als klinisch begrenzt angesehen werden.
Der Hauptausscheidungsweg erfolgt über die Nieren, wo der größte Teil des Medikaments und der Metaboliten ausgeschieden wird. Ein Teil des Arzneimittels wird zu Phenmetrazin und auch zu Phendimetrazin-N-Oxid metabolisiert. Die durchschnittliche Ausscheidungshalbwertszeit liegt bei Untersuchungen unter kontrollierten Bedingungen bei etwa 3,7 Stunden, sowohl für die Formen mit verlängerter Wirkstofffreisetzung als auch für die mit sofortiger Freisetzung. Die Absorptionshalbwertszeit des Wirkstoffs aus den 35 mg Phendimetrazin-Tabletten mit sofortiger Freisetzung ist deutlich schneller als die Absorptionsrate des Wirkstoffs aus der Formulierung mit verzögerter Freisetzung.
Indikationen und Anwendung von Bontril
Bontril®PDM (Phendimetrazintartrat) ist indiziert bei der Behandlung von exogener Adipositas als kurzfristige Ergänzung (einige Wochen) einer auf Kalorienrestriktion basierenden Gewichtsreduktion bei Patienten mit einem anfänglichen Body-Mass-Index (BMI) von 30 kg/m2 oder höher, die auf eine geeignete gewichtsreduzierende Therapie (Diät und/oder Bewegung) allein nicht angesprochen haben. Nachstehend finden Sie eine Tabelle mit dem Body-Mass-Index (BMI) für verschiedene Körpergrößen und -gewichte. Der BMI wird berechnet, indem das Gewicht des Patienten in Kilogramm (kg) durch die Größe des Patienten in Metern (m) zum Quadrat geteilt wird. Metrische Umrechnungen sind wie folgt: Pfund ÷ 2,2 = kg; Zoll x 0,0254 = Meter.
| BODY MASS INDEX (BMI), kg/m2 Höhe (Fuß, Zoll) |
||||||
|---|---|---|---|---|---|---|
| Gewicht (Pfund) |
5’0″ | 5’3″ | 5’6″ | 5’9″ | 6’0″ | 6’3″ |
| 140 | 27 | 25 | 23 | 21 | 19 | 18 |
| 150 | 29 | 27 | 24 | 22 | 20 | 19 |
| 160 | 31 | 28 | 26 | 24 | 22 | 20 |
| 170 | 33 | 30 | 28 | 25 | 23 | 21 |
| 180 | 35 | 32 | 29 | 27 | 25 | 23 |
| 190 | 37 | 34 | 31 | 28 | 26 | 24 |
| 200 | 39 | 36 | 32 | 30 | 27 | 25 |
| 210 | 41 | 37 | 34 | 31 | 29 | 26 |
| 220 | 43 | 39 | 36 | 33 | 30 | 28 |
| 230 | 45 | 41 | 37 | 34 | 31 | 29 |
| 240 | 47 | 43 | 39 | 36 | 33 | 30 |
| 250 | 49 | 44 | 40 | 37 | 34 | 31 |
Phendimetrazintartrat ist nur zur Anwendung als Monotherapie angezeigt.
Kontraindikationen
Bekannte Überempfindlichkeit oder idiosynkratische Reaktionen auf Sympathomimetika.
Fortgeschrittene Arteriosklerose, symptomatische kardiovaskuläre Erkrankungen, mäßiger und schwerer Bluthochdruck, Hyperthyreose und Glaukom.
Hochgradig nervöse oder unruhige Patienten.
Patienten mit Drogenmissbrauch in der Vorgeschichte.
Patienten, die andere ZNS-Stimulanzien einnehmen, einschließlich Monoaminoxidase-Hemmer.
Warnhinweise
Phendimetrazintartrat sollte nicht in Kombination mit anderen anorektischen Mitteln, einschließlich verschriebenen Arzneimitteln, rezeptfreien Präparaten und pflanzlichen Produkten, angewendet werden.
In einer epidemiologischen Fall-Kontroll-Studie wurde die Anwendung von anorektischen Mitteln, einschließlich Phendimetrazintartrat, mit einem erhöhten Risiko für die Entwicklung einer pulmonalen Hypertonie, einer seltenen, aber oft tödlichen Erkrankung, in Verbindung gebracht. Die Einnahme von Anorektika über einen Zeitraum von mehr als drei Monaten war mit einem 23-fach erhöhten Risiko für die Entwicklung einer pulmonalen Hypertonie verbunden. Ein erhöhtes Risiko für pulmonale Hypertonie bei wiederholter Therapie kann nicht ausgeschlossen werden.
Das Auftreten oder die Verschlimmerung von Belastungsdyspnoe oder unerklärliche Symptome von Angina pectoris, Synkope oder Ödemen der unteren Extremitäten deuten auf die Möglichkeit des Auftretens einer pulmonalen Hypertonie hin. Unter diesen Umständen sollte Phendimetrazintartrat sofort abgesetzt und der Patient auf das mögliche Vorhandensein einer pulmonalen Hypertonie untersucht werden.
Es wurde über Herzklappenerkrankungen im Zusammenhang mit der Anwendung einiger anorektischer Mittel wie Fenfluramin und Dexfenfluramin berichtet. Mögliche Faktoren sind die Anwendung über einen längeren Zeitraum, eine höhere als die empfohlene Dosis und/oder die Anwendung in Kombination mit anderen Magentabletten. Es wurden jedoch keine Fälle dieser Valvulopathie berichtet, wenn Phendimetrazintartrat allein angewendet wurde.
Das potenzielle Risiko möglicher schwerwiegender unerwünschter Wirkungen wie Herzklappenerkrankungen und pulmonaler Hypertonie sollte sorgfältig gegen den potenziellen Nutzen einer Gewichtsabnahme abgewogen werden. Vor Beginn einer Phendimetrazin-Behandlung sollte eine kardiologische Basisuntersuchung in Betracht gezogen werden, um vorbestehende Herzklappenerkrankungen oder pulmonale Hypertonie zu erkennen. Phendimetrazintartrat wird bei Patienten mit bekannten Herzgeräuschen oder Herzklappenerkrankungen nicht empfohlen. Ein Echokardiogramm während und nach der Behandlung könnte nützlich sein, um eventuell auftretende Herzklappenerkrankungen zu erkennen. Um ungerechtfertigte Belastungen und Risiken zu begrenzen, sollte die Behandlung mit Phendimetrazintartrat nur fortgesetzt werden, wenn der Patient innerhalb der ersten 4 Wochen der Behandlung eine zufriedenstellende Gewichtsabnahme aufweist (d. h. eine Gewichtsabnahme von mindestens 4 Pfund oder wie vom Arzt und Patienten festgelegt).
Eine Toleranz gegenüber der anorektischen Wirkung von Phendimetrazin entwickelt sich innerhalb weniger Wochen. Wenn dies eintritt, sollte die Anwendung abgebrochen werden; die empfohlene Höchstdosis sollte nicht überschritten werden.
Die Anwendung von Phendimetrazintartrat innerhalb von 14 Tagen nach der Verabreichung von Monoaminoxidase-Hemmern kann zu einer hypertensiven Krise führen.
Ein abruptes Absetzen der Einnahme nach längerer hoher Dosierung führt zu extremer Müdigkeit und Depression. Aufgrund der Wirkung auf das zentrale Nervensystem kann Phendimetrazintartrat die Fähigkeit des Patienten beeinträchtigen, potenziell gefährliche Tätigkeiten auszuüben, wie z. B. das Bedienen von Maschinen oder das Führen eines Kraftfahrzeugs; der Patient sollte daher entsprechend gewarnt werden.
Phendimetrazintartrat wird nicht für Patienten empfohlen, die innerhalb des letzten Jahres Anorektika angewendet haben.
Vorsichtsmaßnahmen
Bei der Verschreibung von Phendimetrazin an Patienten mit selbst leichtem Bluthochdruck ist Vorsicht geboten.
Der Insulinbedarf bei Diabetes mellitus kann sich im Zusammenhang mit der Anwendung von Phendimetrazintartrat und der begleitenden Diät verändern.
Phendimetrazintartrat kann die blutdrucksenkende Wirkung von Guanethidin verringern. Die kleinstmögliche Menge sollte auf einmal verschrieben oder abgegeben werden, um die Möglichkeit einer Überdosierung zu minimieren.
Wechselwirkungen mit anderen Arzneimitteln
Die Wirksamkeit von Phendimetrazintartrat mit anderen anorektischen Mitteln wurde nicht untersucht, und die kombinierte Anwendung kann das Potenzial für schwerwiegende kardiale Probleme haben.
Karzinogenese, Mutagenese, Beeinträchtigung der Fertilität
Studien mit Phendimetrazintartrat wurden nicht durchgeführt, um das karzinogene Potenzial, das mutagene Potenzial oder die Auswirkungen auf die Fertilität zu bewerten.
Schwangerschaft
Schwangerschaftskategorie C
Reproduktionsstudien an Tieren wurden mit Phendimetrazintartrat nicht durchgeführt. Es ist auch nicht bekannt, ob Phendimetrazintartrat den Fötus schädigen kann, wenn es einer schwangeren Frau verabreicht wird, oder ob es die Fortpflanzungsfähigkeit beeinträchtigen kann.
Verwendung in der Schwangerschaft
Die sichere Anwendung in der Schwangerschaft wurde nicht nachgewiesen. Bis weitere Informationen vorliegen, sollte Phendimetrazintartrat von Frauen, die schwanger sind oder schwanger werden könnten, nicht eingenommen werden, es sei denn, der potenzielle Nutzen überwiegt nach Ansicht des Arztes die möglichen Risiken.
Stillende Mütter
Es ist nicht bekannt, ob dieses Arzneimittel in die Muttermilch ausgeschieden wird. Da viele Arzneimittel in die Muttermilch ausgeschieden werden, sollte Phendimetrazintartrat von stillenden Frauen nicht eingenommen werden, es sei denn, der potenzielle Nutzen überwiegt nach Ansicht des Arztes die möglichen Risiken.
Anwendung bei Kindern
Die Sicherheit und Wirksamkeit bei pädiatrischen Patienten wurde nicht nachgewiesen.
Nebenwirkungen
Kardiovaskulär: Herzklopfen, Tachykardie, erhöhter Blutdruck, ischämische Ereignisse.
Es wurde über Herzklappenerkrankungen im Zusammenhang mit der Anwendung einiger anorektischer Wirkstoffe wie Fenfluramin und Dexfenfluramin berichtet, sowohl unabhängig als auch insbesondere in Kombination mit anderen anorektischen Wirkstoffen. Es wurde jedoch kein Fall dieser Valvulopathie berichtet, wenn Phendimetrazintartrat allein angewendet wurde.
Zentralnervensystem: Überstimulation, Unruhe, Schlaflosigkeit, Unruhe, Erröten, Zittern, Schwitzen, Schwindel, Kopfschmerzen, psychotischer Zustand, Verschwommensehen.
Gastrointestinal: Mundtrockenheit, Übelkeit, Durchfall, Verstopfung, Magenschmerzen.
Genitourinär: Harnfrequenz, Dysurie, Veränderungen der Libido.
Drogenmissbrauch und Abhängigkeit
Kontrollierte Substanz
Bontril® PDM (Phendimetrazintartrat) ist eine kontrollierte Substanz der Liste lll.
Abhängigkeit
Phendimetrazintartrat ist chemisch und pharmakologisch mit den Amphetaminen verwandt. Amphetamine und verwandte Stimulanzien sind in großem Umfang missbraucht worden, und die Möglichkeit des Missbrauchs von Phendimetrazin sollte bei der Beurteilung der Zweckmäßigkeit der Einbeziehung eines Medikaments in ein Programm zur Gewichtsreduktion berücksichtigt werden. Der Missbrauch von Amphetaminen und verwandten Drogen kann mit einer starken psychischen Abhängigkeit und schweren sozialen Störungen einhergehen. Es gibt Berichte von Patienten, die die Dosis auf ein Vielfaches der empfohlenen Menge erhöht haben. Ein abruptes Absetzen nach längerer Einnahme hoher Dosen führt zu extremer Müdigkeit und psychischer Depression; auch im Schlaf-EEG werden Veränderungen festgestellt. Zu den Manifestationen einer chronischen Intoxikation mit Anorektika gehören schwere Dermatosen, ausgeprägte Schlaflosigkeit, Reizbarkeit, Hyperaktivität und Persönlichkeitsveränderungen. Die schwerste Manifestation einer chronischen Intoxikation ist eine Psychose, die klinisch oft nicht von einer Schizophrenie zu unterscheiden ist.
Überdosierung
Eine akute Überdosierung mit Phendimetrazintartrat kann sich durch folgende Anzeichen und Symptome äußern: ungewöhnliche Unruhe, Verwirrtheit, Streitsucht, Halluzinationen und Panikzustände. Müdigkeit und Depression folgen in der Regel auf die zentrale Stimulation. Zu den kardiovaskulären Wirkungen gehören Herzrhythmusstörungen, Bluthochdruck oder Hypotonie und Kreislaufkollaps. Zu den gastrointestinalen Symptomen gehören Übelkeit, Erbrechen, Durchfall und Bauchkrämpfe. Vergiftungen können zu Krämpfen, Koma und Tod führen.
Die Behandlung einer Überdosierung ist weitgehend symptomatisch. Sie umfasst eine Sedierung mit einem Barbiturat. Bei ausgeprägtem Bluthochdruck sollte die Verwendung eines Nitrats oder eines schnell wirkenden Alpha-Rezeptorenblockers in Betracht gezogen werden. Die Erfahrungen mit der Hämodialyse oder der Peritonealdialyse sind unzureichend, um Empfehlungen für deren Anwendung zu geben.
Bontril Dosierung und Verabreichung
Normale Dosierung für Erwachsene
1 Tablette (35 mg) zweimal täglich oder dreimal täglich eine Stunde vor den Mahlzeiten.
Die Dosierung sollte individuell angepasst werden, um eine angemessene Reaktion mit der niedrigsten wirksamen Dosis zu erreichen. In einigen Fällen kann ½ Tablette (17,5 mg) pro Dosis ausreichend sein. Die Dosierung sollte 2 Tabletten dreimal täglich nicht überschreiten.
Wie wird Bontril geliefert
Dreischichtige grün-weiß-gelbe Tablette mit „B 35“ auf der geritzten Seite und dem Buchstaben „V“ auf der anderen. Bontril® PDM Tabletten, die 35 mg Phendimetrazintartrat enthalten, sind in Flaschen zu 100 (NDC 0187-0497-01) und 1000 (NDC 0187-0497-02) erhältlich.
Bewahren Sie die Tabletten bei 25°C (77°F) auf; Abweichungen von 15°C-30°C (59°F-86°F) sind zulässig.
DEA-Bestellformular erforderlich.
Vertrieben von:
Valeant Pharmaceuticals North America
One Enterprise
Aliso Viejo, CA 92656 USA
Hergestellt von:
Mallinckrodt, Inc.
Hobart, NY 13788
Gedruckt mit lebensmittelechter Tinte.
MG #20886
Rev. 10/07
Teilnr. L2BB01
Hauptanzeigefeld – 35 mg Tabletten Flaschenetikett
NDC 0187-0497-02
Nur RX
CIII
Bontril® PDM
(Phendimetrazintartrat-Tabletten, USP)
35 mg
Je drei Schichten
grün, weiße und gelbe
Tablette enthält 35 mg
Phendimetrazin
tartrat
1000
Tabletten
VALEANT™
| Bontril PDM Phendimetrazin Tartrat-Tablette |
||||||||||||||||||||||||||
|
||||||||||||||||||||||||||
|
||||||||||||||||||||||||||
|
||||||||||||||||||||||||||
|
||||||||||||||||||||||||||
|
||||||||||||||||||||||||||
|
||||||||||||||||||||||||||
Labeler -. Valeant Pharmaceuticals International (042230623)
| Einrichtung | |||
| Name | Adresse | ID/FEI | Betrieb |
| MALLINCKRODT INC | 957414238 | HERSTELLUNG(0187-0497) | |
Mehr über Bontril Slow Release (Phendimetrazin)
- Nebenwirkungen Wirkungen
- In der Schwangerschaft
- Informationen zur Dosierung
- Abbildungen
- Wechselwirkungen
- 35 Bewertungen
- Medikamentenklasse: Anorexantien
Verbraucherinformationen
- Patienteninformationen
- Bontril (Advanced Reading)
- Bontril Slow-Release (Advanced Reading)
Fachinformationen
- Rezeptinformationen
- Phendimetrazin (AHFS-Monographie)
Andere Marken Fendique ER
Verwandte Behandlungsleitfäden
- Adipositas
Medizinischer Haftungsausschluss