ATP, NAD Y FAD
ATP
Las células utilizan una molécula llamada Trifosfato de Adenosina (o ATP) como fuente de energía (Ver figura 2). Los fosfatos de esta molécula pueden suministrar energía a los sustratos de nuestras células. En nuestras células existen enzimas que pueden eliminar un fosfato del ATP y unirlo a una molécula diferente, normalmente una proteína (véase la figura 3). Cuando esto ocurre, decimos que la proteína ha sido fosforilada. Piense que el tercer fosfato es un pequeño saco de energía. Cuando se transfiere a una proteína, esta energía puede utilizarse para hacer algo. Por ejemplo, en la figura 3, la proteína cambia de forma cuando se fosforila. Cuando las proteínas cambian de forma, solemos llamar a esto un cambio conformacional en la estructura de la proteína. Hay muchas proteínas en el cuerpo que utilizan un fosfato del ATP para inducir un cambio conformacional. Este cambio de forma de la proteína permite, en última instancia, cosas como la contracción muscular, la movilidad celular, el transporte de membrana y la acción de las enzimas. Las células y la vida sólo existen si se dispone de un suministro constante y estable de ATP.
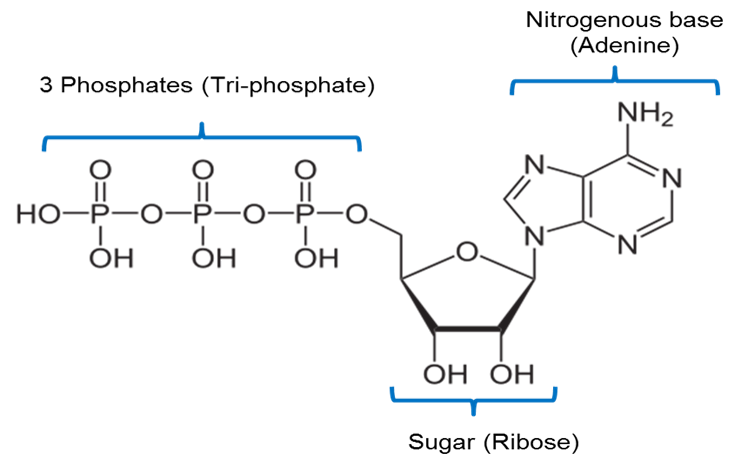
Imagen creada por JS en BYU Idaho F2013.
La imagen de arriba es una representación de la estructura química del ATP. El ATP incluye una base nitrogenada llamada adenina unida a un azúcar de 5 carbonos llamado ribosa y 3 grupos fosfato.
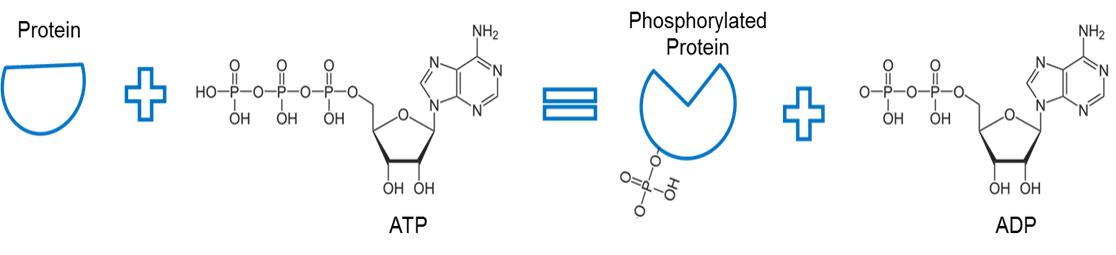
Imagen creada por JS en BYU Idaho F2013.
El ATP se utiliza para fosforilar una proteína. Una enzima, llamada quinasa (no mostrada) elimina un fosfato del ATP y facilita una unión entre el fosfato y alguna otra proteína. La unión de un fosfato a una proteína de esta manera se llama fosforilación. El hueso del fosfato con la proteína tiene mayor energía. Obsérvese que la fosforilación utiliza esta energía para provocar un cambio conformacional de la forma de la proteína.
NAD y FAD
El dinucleótido de adenina nicotinamida (NAD) y el dinucleótido de adenina flavina (FAD) son coenzimas que intervienen en las reacciones reversibles de oxidación y reducción. A menudo se dice que estos compuestos son portadores de electrones porque aceptan electrones (se reducen) durante los pasos catabólicos en la descomposición de moléculas orgánicas como los carbohidratos y los lípidos. Entonces, estas coenzimas reducidas pueden donar estos electrones a alguna otra reacción bioquímica normalmente implicada en un proceso que es anabólico (como la síntesis de ATP).
NAD+ / NADH
El dinucleótido de adenina nicotinamida en su estado oxidado se denomina NAD+, después de ser reducido (o aceptar electrones), se denomina NADH. Véase la figura 4 para una ilustración molecular. La vitamina Niacina (también llamada B3) se utiliza para obtener este compuesto. La niacina proporciona la estructura de anillo orgánico que participará directamente en la transferencia de un átomo de hidrógeno y 2 electrones. El NAD+ se encuentra a menudo en combinación con una enzima «deshidrogenasa». Una reacción de deshidrogenasa elimina dos átomos de hidrógeno; uno como hidruro (:H-) (un hidruro es un átomo de hidrógeno con 2 electrones) y otro como catión de hidrógeno (H+) (y por supuesto, un catión de hidrógeno no tiene electrones). El hidruro se une al NAD+ y crea un compuesto reducido de Nictinamida Adenina Dinucleótido (NADH). El segundo átomo de hidrógeno (H+) se libera en la solución, véase la figura 4.
Al examinar las reacciones del metabolismo, busque las reacciones que producen NADH. El NADH será importante ya que entregará los hidrógenos y los electrones que recoge a los procesos bioquímicos que pueden utilizar los electrones y los hidrógenos para fabricar ATP.
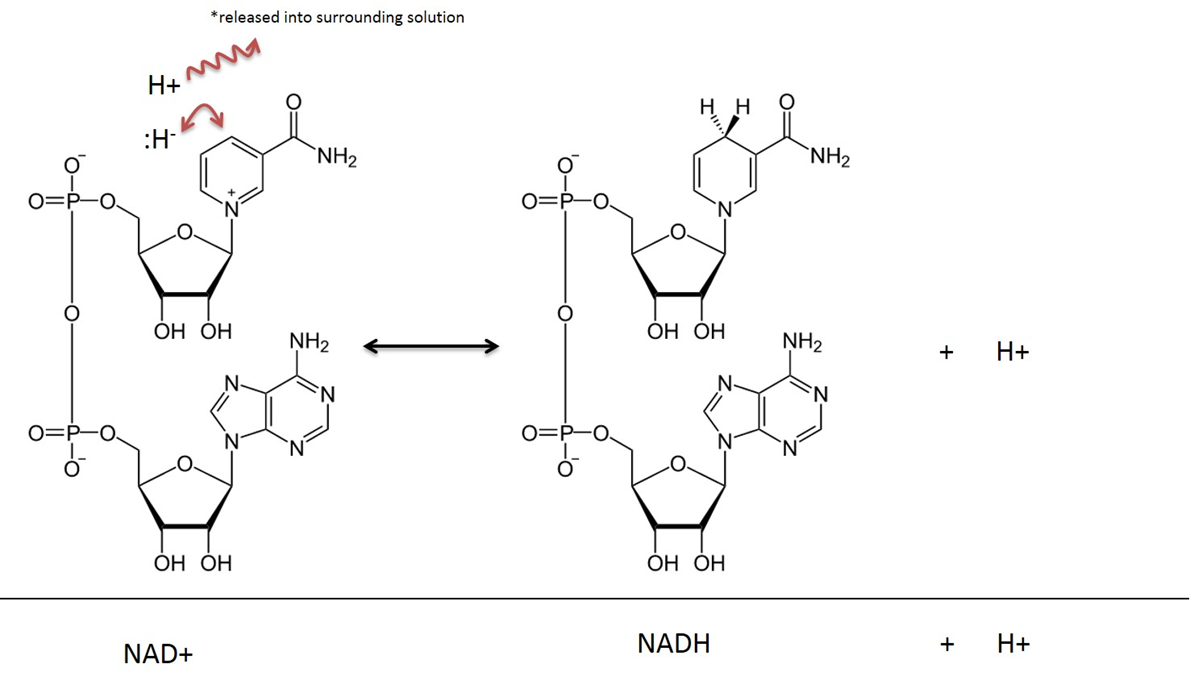
Imagen creada por JS en BYU Idaho F2013.
En las reacciones metabólicas que implican al NAD, se eliminan dos átomos de hidrógeno y dos electrones de un sustrato y se transfieren al NAD+. El NAD+ acepta un ion hidruro (un hidrógeno con 2 electrones) y se convierte en Nicotinamida Adenina Dinucleótido en la forma reducida (NADH). El catión hidrógeno que también se captura en la reacción se libera en la solución circundante. Recuerde que esta reacción es reversible.
En la explicación de las reacciones que ocurren en el Metabolismo, es común ignorar el H+ liberado en la solución y este texto representará el resultado de la reducción del NAD como simplemente NADH, en lugar de NADH + H+.
FAD / FADH2
El dinucleótido de adenina flavina en su estado oxidado se llama FAD. Una vez reducido, se denomina FADH2. Véase la figura 5 para una ilustración molecular. La vitamina riboflavina (o B2) se utiliza para obtener este compuesto. La riboflavina proporciona las estructuras de anillo que participarán directamente en la transferencia de dos átomos de hidrógeno (cada uno con un electrón esta vez). Al igual que el NAD, el FAD funciona en asociación con una enzima «deshidrogenasa». La reacción elimina dos átomos de hidrógeno, cada uno con un protón y un electrón. Ambos átomos de hidrógeno se unen al FAD. Esta reacción no libera un H+ en la solución como lo hace la reducción del NAD.
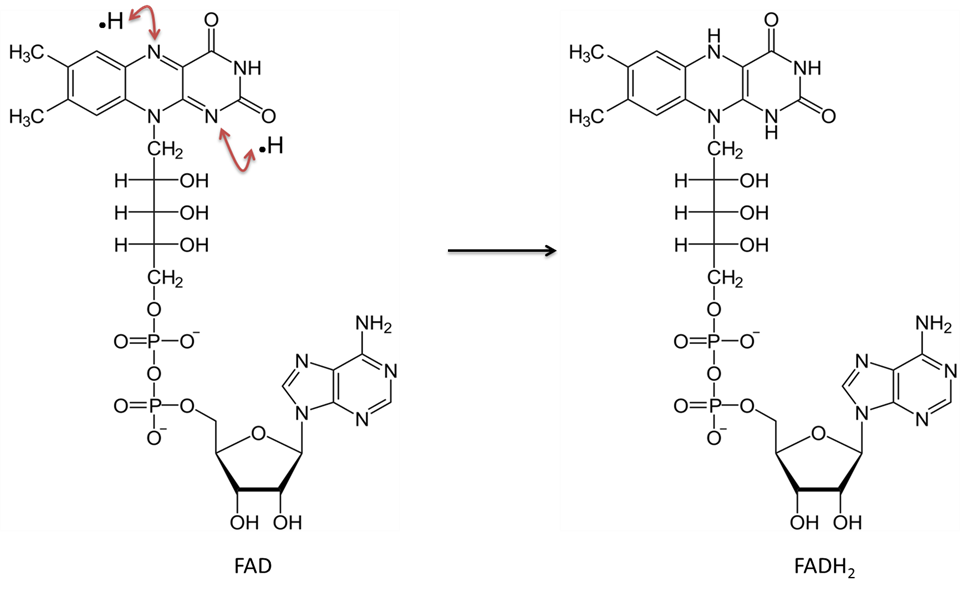
Imagen creada por JS en BYU Idaho F2013.
El dinucleótido de adenina de flavina en la forma oxidada (FAD) acepta dos átomos de hidrógeno (cada uno con un electrón) y se convierte en FADH2.
Al examinar las reacciones del metabolismo, busque una reacción que produzca FADH2. Al igual que el NADH, el FADH2 será importante ya que entregará hidrógenos y electrones a los procesos bioquímicos que pueden utilizar los electrones e hidrógenos para fabricar ATP.
**Puede utilizar los botones de abajo para ir a la lectura siguiente o anterior de este Módulo**

