Nombre genérico: clorhidrato de naftifina
Forma farmacéutica: gel
Revisado médicamente por Drugs.com. Actualizado por última vez el 1 de abril de 2020.
- Descripción general
- Efectos secundarios
- Dosificación
- Profesional
- Embarazo
- Más
- Indiciones y Uso de Naftin Gel
- Dosis y administración de NAFTIN ® Gel
- Formas de dosificación y concentraciones
- Contraindicaciones
- Advertencias y precauciones
- Reacciones adversas locales
- Reacciones adversas
- Experiencia en ensayos clínicos
- Experiencia posterior a la comercialización
- Uso en poblaciones específicas
- Embarazo
- Lactancia
- Uso pediátrico
- Uso geriátrico
- Descripción de NAFTIN ® Gel
- Naftin Gel – Farmacología clínica
- Mecanismo de acción
- Farmacodinámica
- Farmacocinética
- Microbiología
- Toxicología no clínica
- Carcinogénesis, Mutagénesis, Alteración de la fertilidad
- Estudios clínicos
- Cómo se suministra/almacenamiento y manipulación
- Información al paciente
- PANEL DE PRESENTACIÓN PRINCIPAL – Tubo de 45g Cartón
- PANEL DE PRESENTACIÓN PRINCIPAL – Tubo de cartón de 60 g
- Más información sobre Naftin (naftifine topical)
- Recursos para el consumidor
- Recursos profesionales
- Otras formulaciones
- Guías de tratamiento relacionadas
Indiciones y Uso de Naftin Gel
NAFTIN ® Gel es un antifúngico de alilamina indicado para el tratamiento de la tinea pedis interdigital causada por los organismos Trichophyton rubrum, Trichophyton mentagrophytes, y Epidermophyton floccosum.
Dosis y administración de NAFTIN ® Gel
Aplique una fina capa de NAFTIN ® Gel una vez al día en las zonas afectadas más un margen de aproximadamente ½ pulgada de piel sana circundante durante 2 semanas.
Sólo para uso tópico. NAFTIN ® Gel no es para uso oftálmico, oral o intravaginal.
Formas de dosificación y concentraciones
Gel, 2%. Cada gramo contiene 20 mg de clorhidrato de naftifina en un gel incoloro a amarillo.
Contraindicaciones
Ninguna.
Advertencias y precauciones
Reacciones adversas locales
Si se produce irritación o sensibilidad con el uso de NAFTIN ® Gel, debe interrumpirse el tratamiento.
Reacciones adversas
Experiencia en ensayos clínicos
Debido a que los ensayos clínicos se llevan a cabo en condiciones muy variadas, las tasas de reacciones adversas observadas en los ensayos clínicos de un medicamento no pueden compararse directamente con las tasas en los ensayos clínicos de otro medicamento y pueden no reflejar las tasas observadas en la práctica clínica.
En dos ensayos aleatorizados, controlados con vehículo, 1143 sujetos fueron tratados con NAFTIN ® Gel frente a 571 sujetos tratados con el vehículo. Los sujetos del ensayo tenían entre 12 y 92 años de edad, eran principalmente hombres (76%), y eran 59% caucásicos, 38% negros o afroamericanos y 23% hispanos o latinos. Los sujetos recibieron dosis una vez al día, por vía tópica, durante 2 semanas para cubrir las zonas de piel afectadas más un margen de ½ pulgada de piel sana circundante. Las reacciones adversas más comunes fueron las reacciones en el lugar de aplicación, que se produjeron en una proporción del 2% en el brazo del gel de Naftin frente al 1% en el brazo del vehículo. La mayoría de las reacciones adversas fueron de gravedad leve.
En un ensayo abierto de farmacocinética y seguridad pediátrica, 22 sujetos pediátricos de 12 a 17 años de edad con tinea pedis interdigital recibieron NAFTIN ® Gel. La incidencia de reacciones adversas en la población pediátrica fue similar a la observada en la población adulta.
Las pruebas de irritación acumulativa revelaron el potencial de NAFTIN ® Gel para causar irritación. No hubo pruebas de que NAFTIN ® Gel cause sensibilización por contacto, fototoxicidad o fotoalergenicidad en la piel sana.
Experiencia posterior a la comercialización
Debido a que estas reacciones se notifican voluntariamente desde una población de tamaño incierto, no siempre es posible estimar de forma fiable su frecuencia o establecer una relación causal con la exposición al medicamento. Se han identificado las siguientes reacciones adversas durante el uso posterior a la aprobación del hidrocloruro de naftifina: ampollas, sensación de ardor, formación de costras, sequedad, eritema/enrojecimiento, inflamación, irritación, maceración, dolor, prurito/picazón, erupción e hinchazón.
Uso en poblaciones específicas
Embarazo
Resumen de riesgos
No se dispone de datos sobre el uso de NAFTIN® Gel en mujeres embarazadas para evaluar un riesgo asociado al fármaco de defectos congénitos importantes, aborto espontáneo o resultados maternos o fetales adversos.
En estudios de reproducción animal, no se observaron efectos adversos sobre el desarrollo embriofetal a dosis orales administradas durante el periodo de organogénesis hasta 37 veces la dosis máxima recomendada en humanos (MRHD) en ratas preñadas o a dosis subcutáneas administradas durante el periodo de organogénesis hasta 4 veces la MRHD en ratas preñadas o 7 veces la MRHD en conejas preñadas ( ver Datos).
Todos los embarazos tienen un riesgo de fondo de defectos de nacimiento, pérdida u otros resultados adversos. Se desconoce el riesgo de fondo estimado de defectos congénitos importantes y de aborto espontáneo para la población indicada. En la población general de EE.UU., el riesgo de fondo estimado de defectos congénitos importantes y de aborto espontáneo en embarazos clínicamente reconocidos es del 2 al 4% y del 15 al 20%, respectivamente.
Datos
Datos en animales
Se realizaron estudios de desarrollo embriofetal sistémico en ratas y conejos. Para la comparación de las dosis en animales con las humanas, la MRHD se establece en 4 g de gel al 2% por día (1,33 mg/kg/día para un individuo de 60 kg).
Se administraron dosis orales de 30, 100 y 300 mg/kg/día de clorhidrato de naftifina durante el período de organogénesis a ratas hembras preñadas. No se observaron efectos relacionados con el tratamiento sobre la toxicidad embriofetal a dosis de hasta 300 mg/kg/día (37 veces la MRHD basada en la comparación de mg/m 2). Se administraron dosis subcutáneas de 10 y 30 mg/kg/día de clorhidrato de naftifina durante el período de organogénesis a ratas hembras preñadas. No se observaron efectos relacionados con el tratamiento sobre la toxicidad embriofetal a 30 mg/kg/día (4 veces la MRHD basada en la comparación de mg/m 2). Se administraron dosis subcutáneas de 3, 10 y 30 mg/kg/día de clorhidrato de naftifina durante el período de organogénesis a conejas hembras preñadas. No se observaron efectos relacionados con el tratamiento sobre la toxicidad embriofetal a 30 mg/kg/día (7 veces la MRHD basada en la comparación de mg/m 2).
Se realizó un estudio de desarrollo peri y postnatal en ratas. Se administraron dosis orales de 30, 100 y 300 mg/kg/día de clorhidrato de naftifina a ratas hembras desde el día 14 de gestación hasta el día 21 de lactancia. Se observó una reducción del aumento de peso corporal de las hembras durante la gestación y de las crías durante la lactancia con 300 mg/kg/día (37 veces el MRHD basado en la comparación de mg/m 2). No se observó toxicidad para el desarrollo con 100 mg/kg/día (12 veces la MRHD basada en la comparación de mg/m 2).
Lactancia
Resumen de riesgos
No se dispone de información sobre la presencia de clorhidrato de naftifina en la leche humana, los efectos del medicamento en el lactante, o los efectos del medicamento en la producción de leche tras la aplicación tópica de Naftin Gel en mujeres que están amamantando. Se desconoce si el clorhidrato de naftifina se excreta en la leche humana. Debido a que muchos fármacos se excretan en la leche humana, se debe tener precaución cuando se administre naftifina hidrocloruro a una mujer que esté amamantando.
La falta de datos clínicos durante la lactancia impide una determinación clara del riesgo de Naftin Gel para un lactante durante la lactancia. Por lo tanto, deben considerarse los beneficios para el desarrollo y la salud de la lactancia junto con la necesidad clínica de Naftin Gel por parte de la madre y cualquier efecto adverso potencial sobre el lactante a causa de Naftin Gel o de la enfermedad materna subyacente.
Uso pediátrico
Se ha establecido la seguridad y eficacia de NAFTIN® Gel en el grupo de edad de 12 a 18 años con tinea pedis interdigital.
El uso de NAFTIN® Gel en este grupo de edad está respaldado por la evidencia de ensayos adecuados y bien controlados en adultos con datos adicionales de seguridad y PK de un ensayo abierto, realizado en 22 adolescentes ≥12 años de edad que fueron expuestos a NAFTIN® Gel a una dosis de aproximadamente 4 g/día .
No se ha establecido la seguridad y eficacia en pacientes pediátricos <12 años de edad.
Uso geriátrico
Durante los ensayos clínicos, 99 sujetos (9%) de 65 años o más fueron expuestos a NAFTIN ® Gel. La seguridad y la eficacia fueron similares a las reportadas por los sujetos más jóvenes.
Descripción de NAFTIN ® Gel
NAFTIN ® Gel es un gel transparente a amarillo para uso tópico solamente. Cada gramo de NAFTIN ® Gel contiene 20 mg de clorhidrato de naftifina, un compuesto antifúngico sintético de alilamina.
Químicamente, naftifina HCl es clorhidrato de (E)-N-cinamil-N-metil-1-naftalenometilamina.
La fórmula molecular es C 21H 21N∙HCl con un peso molecular de 323,86.
La fórmula estructural del clorhidrato de naftifina es :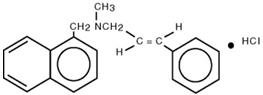
NAFTIN ® Gel contiene los siguientes ingredientes inactivos: alcohol, alcohol bencílico, edetato disódico, hidroxietilcelulosa, agua purificada, propilenglicol, polisorbato 20 y trolamina.
Naftin Gel – Farmacología clínica
Mecanismo de acción
NAFTIN ® Gel es un medicamento antimicótico tópico .
Farmacodinámica
La farmacodinámica de NAFTIN ® Gel no se ha establecido.
Farmacocinética
Los estudios de biodisponibilidad in vitro e in vivo han demostrado que la naftifina penetra en el estrato córneo en concentración suficiente para inhibir el crecimiento de los dermatofitos.
El análisis farmacocinético de muestras de plasma de 32 sujetos con tinea pedis tratados con una dosis media de 3,9 gramos de NAFTIN ® Gel aplicada una vez al día en ambos pies durante 14 días mostró un aumento de la exposición a lo largo del periodo de tratamiento, con una media geométrica (CV%) del AUC 0-24 (área bajo la curva de concentración plasmática frente al tiempo desde el tiempo 0 hasta las 24 horas) de 10,5 (118) ng∙hr/mL el día 1 y un AUC 0-24 de 70 (59) ng∙hr/mL el día 14. La relación de acumulación basada en el AUC fue de aproximadamente 6.
La concentración máxima (C máx.) también aumentó durante el período de tratamiento; la media geométrica (CV%) de la C máx. tras una dosis única fue de 0,9 (92) ng/mL el Día 1; la C máx. el Día 14 fue de 3,7 (64) ng/mL. La mediana de la T máxima fue de 20,0 horas (rango: 8, 20 horas) después de una sola aplicación el Día 1 y de 8,0 horas (rango: 0, 24 horas) el Día 14. Las concentraciones plasmáticas mínimas aumentaron durante el período de prueba y alcanzaron el estado estable después de 11 días. En el mismo ensayo farmacocinético, la fracción de dosis excretada en la orina durante el período de tratamiento fue menor o igual al 0,01% de la dosis aplicada.
En un segundo ensayo, se evaluó la farmacocinética de NAFTIN ® Gel en 22 sujetos pediátricos de 12 a 17 años de edad con tinea pedis. Los sujetos fueron tratados con una dosis media de 4,1 gramos de NAFTIN ® Gel aplicada en la zona afectada una vez al día durante 14 días. Los resultados mostraron que la exposición sistémica aumentó durante el período de tratamiento. La media geométrica (CV%) del AUC0-24 fue de 15,9 (212) ng∙hr/mL el día 1 y de 60,0 (131) ng∙hr/mL el día 14. La media geométrica (CV%) de la Cmáx tras una dosis única fue de 1,40 (154) ng/mL el día 1 y de 3,81 (154) ng/mL el día 14. La fracción de dosis excretada en orina durante el periodo de tratamiento fue menor o igual al 0,003% de la dosis aplicada.
Microbiología
Mecanismo de acción
La naftifina es un antifúngico que pertenece a la clase de las alilaminas. Aunque no se conoce el mecanismo exacto de acción contra los hongos, el clorhidrato de naftifina parece interferir en la biosíntesis de esteroles mediante la inhibición de la enzima escualeno 2, 3-epoxidasa. La inhibición de la actividad enzimática por parte de esta alilamina da lugar a una disminución de las cantidades de esteroles, especialmente de ergosterol, y a la correspondiente acumulación de escualeno en las células.
Mecanismo de resistencia
Hasta la fecha, no se ha identificado un mecanismo de resistencia a la naftifina.
La naftifina ha demostrado ser activa frente a la mayoría de los aislados de los siguientes hongos, tanto in vitro como en infecciones clínicas, como se describe en la sección INDICACIONES Y USO:
- Trichophyton rubrum
- Trichophyton mentagrophytes
- Epidermophyton floccosum
Toxicología no clínica
Carcinogénesis, Mutagénesis, Alteración de la fertilidad
En un estudio de carcinogenicidad dérmica de 2 años, se administró crema de clorhidrato de naftifina a ratas Sprague-Dawley a dosis tópicas del 1%, 2% y 3% (10, 20 y 30 mg/kg/día de clorhidrato de naftifina). En este estudio no se observaron tumores relacionados con el medicamento hasta la dosis más alta evaluada en este estudio de 30 mg/kg/día (36 veces la MRHD en base a la comparación del AUC).
El clorhidrato de naftifina no reveló ninguna evidencia de potencial mutagénico o clastogénico en base a los resultados de dos pruebas de genotoxicidad in vitro (ensayo de Ames y ensayo de aberración cromosómica en células de ovario de hámster chino) y una prueba de genotoxicidad in vivo (ensayo de micronúcleos en médula ósea de ratón).
La administración oral de clorhidrato de naftifina a ratas, durante el apareamiento, la gestación, el parto y la lactancia, no demostró efectos sobre el crecimiento, la fertilidad o la reproducción, a dosis de hasta 100 mg/kg/día (12 veces la MRHD basada en la comparación de mg/m 2).
Estudios clínicos
Se ha evaluado la eficacia de NAFTIN ® Gel en dos ensayos multicéntricos aleatorizados, doble ciego, controlados con vehículo, que incluyeron 1175 sujetos con tinea pedis interdigital sintomática y con cultivos de dermatofitos positivos. Los sujetos fueron asignados al azar para recibir NAFTIN ® Gel o vehículo. Los sujetos aplicaron el gel de clorhidrato de naftifina al 2% o el vehículo en la zona afectada del pie una vez al día durante 2 semanas. Se evaluaron los signos y síntomas de la tinea pedis interdigital (presencia o ausencia de eritema, prurito y descamación) y se realizó un examen con hidróxido de potasio (KOH) y un cultivo de dermatofitos 6 semanas después del primer tratamiento.
La edad media de la población del estudio fue de 45 años; el 77% eran hombres; y el 60% eran caucásicos, el 35% eran negros o afroamericanos y el 26% eran hispanos o latinos. Al inicio del estudio, se confirmó que los sujetos tenían signos y síntomas de tinea pedis interdigital, un examen KOH positivo y un cultivo de dermatofitos confirmado. El criterio de valoración primario de la eficacia fue la proporción de sujetos con una curación completa a las 6 semanas del inicio del tratamiento (4 semanas después del último tratamiento). La curación completa se definió como una curación clínica (ausencia de eritema, prurito y descamación) y una curación micológica (cultivo de KOH y dermatofitos negativos).
Los resultados de eficacia en la semana 6, cuatro semanas después del final del tratamiento, se presentan en la Tabla 1 a continuación.
| Trial 1 | Trial 2 | |||
|---|---|---|---|---|
| Punto final | NAFTIN ® Gel, 2% N=382 n (%) |
Vehículo N=179 n (%) |
NAFTIN ® Gel, 2% N=400 n (%) |
Vehículo N=213 n (%) |
| * La curación completa es un criterio de valoración compuesto por la curación micológica y la curación clínica. La curación clínica se define como la ausencia de eritema, prurito y descamación (grado 0). † El tratamiento eficaz es una preparación de KOH negativa y un cultivo de dermatofitos negativo, grados de eritema, descamación y prurito de 0 o 1 (ausente o casi ausente). ‡ La curación micológica se define como una preparación KOH y un cultivo de dermatofitos negativos. | ||||
| Curación Completa* | 64 (17%) | 3 (2%) | 104 (26%) | 7 (3%) |
| Eficacia del tratamiento † | 207 (54%) | 11 (6%) | 203 (51%) | 15 (7%) |
| Micológico Curación ‡ | 250 (65%) | 25 (14%) | 235 (59%) | 22 (10%) |
Cómo se suministra/almacenamiento y manipulación
Cómo se suministra
NAFTIN ® Gel es un gel incoloro a amarillo que se suministra en tubos plegables en el siguiente tamaño:
45g – NDC 54766-772-45
60g – NDC 54766-772-60
Almacenamiento
Almacenar NAFTIN ® Gel a 25°C (77°F); se permiten excursiones a 15-30°C (59-86°F) .
Información al paciente
- Informe a los pacientes que NAFTIN ® Gel es sólo para uso tópico. NAFTIN ® Gel no está destinado al uso oftálmico, oral o intravaginal.
- Se debe indicar a los pacientes que se pongan en contacto con su médico si se produce irritación con el uso de NAFTIN ® Gel.
Distribuido por Sebela Pharmaceuticals Inc.
645 Hembree Parkway, Suite I, Roswell, GA 30076
www.sebelapharma.com
Llamada gratuita 1-844-732-3521
©2020 Sebela Pharmaceuticals Inc. Todos los derechos reservados.
PANEL DE PRESENTACIÓN PRINCIPAL – Tubo de 45g Cartón

NDC 54766-772-45
NAFTIN ®
(Clorhidrato de Naftifina) Gel, 2%
Sebela Pharmaceuticals Inc.
Sólo para uso tópico
No para uso oftálmico, Uso Oral o Intravaginal
45g
Sólo para uso tópico
PANEL DE PRESENTACIÓN PRINCIPAL – Tubo de cartón de 60 g

NDC 54766-772-60
NAFTIN®
(Clorhidrato de Naftifina) Gel, 2%
Sebela Pharmaceuticals Inc.
Sólo para uso tópico
No para uso oftálmico, Uso Oral o Intravaginal
60g
Sólo para uso tópico
| NAFTIN gel de clorhidrato de naftifina |
|||||||||||||||||||||||
|
|||||||||||||||||||||||
|
|||||||||||||||||||||||
|
|||||||||||||||||||||||
|
|||||||||||||||||||||||
|
|||||||||||||||||||||||
Etiquetadora – Sebela Pharmaceuticals Inc. (079104574)
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| DPT Laboratories, Ltd. | 832224526 | fabricación(54766-772), análisis(54766-772), etiquetado(54766-772) | |
Más información sobre Naftin (naftifine topical)
- Efectos secundarios
- Durante el embarazo o la lactancia
- Dosificación. Información
- Precios &Cupones
- En Español
- 3 Reseñas
- Disponibilidad genérica
- Clase de medicamentos: antifúngicos tópicos
Recursos para el consumidor
- Información para el paciente
- Naftin tópico (lectura avanzada)
Recursos profesionales
- Información para la prescripción
- Naftifina (Monografía del SAF)
Otras formulaciones
- Naftin-MP Topical
Guías de tratamiento relacionadas
- Tinea Pedis
- Tinea Corporis
- Tinea Cruris
Aviso médico