Localizada vs. deslocalizada
La distinción entre «localizada» y «deslocalizada» sólo existe cuando describimos el movimiento de los electrones utilizando la teoría de enlace de Lewis.
De acuerdo con esta teoría, los electrones localizados muestran un comportamiento normal. Un par solitario localizado permanece cerca de un átomo. Un par de enlace localizado viaja entre dos átomos.
Los híbridos de resonancia contienen necesariamente algunos electrones «anormales». Un par solitario puede parecer que tiene algunas características de enlace; en lugar de quedarse cerca de un átomo, visita dos átomos. Un par de enlace puede parecer que se mueve entre dos pares de átomos diferentes. Estos electrones se salen de los límites que la teoría de Lewis ha establecido para ellos, y los consideramos deslocalizados.
La forma más fácil de detectar electrones deslocalizados es comparar las localizaciones de los electrones en dos formas de resonancia. Si un par aparece en un lugar en una forma, y en un lugar diferente en otra forma, el par está deslocalizado.
Puedes ver el comportamiento deslocalizado en las formas de resonancia I y II a continuación. Ambas formas contienen dos pares de electrones deslocalizados. ¿Puedes encontrarlos? ¿Qué tipo de pares de electrones están deslocalizados en cada estructura?
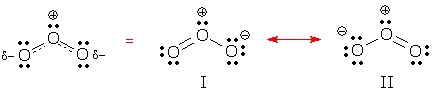
(Respuesta: estas formas contienen un par de enlace deslocalizado y un par solitario deslocalizado.)
Enlaces deslocalizados y cargas deslocalizadas
La etiqueta «deslocalizado» también se aplica a los enlaces y a las cargas.
Un enlace deslocalizado es un enlace que aparece en algunas formas de resonancia, pero no en otras. La forma de resonancia I contiene 2 enlaces localizados y 1 enlace deslocalizado.
Una carga deslocalizada es una carga formal que aparece en un átomo en algunas formas de resonancia y en otros átomos en otras formas. La carga negativa del ozono está deslocalizada sobre los dos O extremos, mientras que la carga positiva está localizada en el O central.