9.1 Terminologie des huiles végétales et des graisses animales
La graisse est un terme générique pour les lipides, une classe de composés en biochimie. Vous les connaîtriez comme des matières grasses et solides que l’on trouve dans les tissus animaux et dans certaines plantes – des huiles qui sont solides à température ambiante.
L’huile végétale est la graisse extraite de sources végétales. On peut être capable d’extraire l’huile d’autres parties d’une plante, mais les graines sont la principale source d’huile végétale. Généralement, les huiles végétales sont utilisées en cuisine et pour des usages industriels. Par rapport à l’eau, les huiles et les graisses ont un point d’ébullition beaucoup plus élevé. Cependant, certaines huiles végétales ne sont pas bonnes pour la consommation humaine, car les huiles provenant de ces types de graines nécessitent un traitement supplémentaire pour éliminer les saveurs désagréables, voire les produits chimiques toxiques. Il s’agit notamment de l’huile de colza et de l’huile de coton.
Les graisses animales proviennent de différents animaux. Le suif est la graisse de bœuf et le saindoux est la graisse de porc. Il y a aussi la graisse de poulet, la graisse de baleine, l’huile de foie de morue et le ghee (qui est une graisse de beurre). Les graisses animales ont tendance à avoir plus d’acides gras libres que les huiles végétales.
Chimiquement, les graisses et les huiles sont également appelées « triglycérides ». Elles sont des esters de glycérol, avec un mélange variable d’acides gras. La figure 9.1 montre un diagramme générique de la structure sans utiliser de formules chimiques.
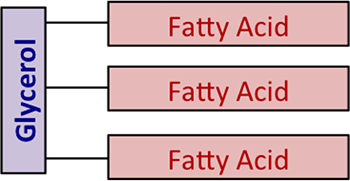
Alors, qu’est-ce que le glycérol ? Il est également connu sous le nom de glycérine/glycérine. Les autres noms du glycérol sont : 1,2,3-propane-triol, 1,2,3-tri-hydroxy-propane, glycéritol et alcool glycylique. C’est un liquide visqueux incolore, inodore, hygroscopique (c’est-à-dire qu’il attire l’eau) et au goût sucré. La figure 9.2 montre la structure chimique sous deux formes différentes.
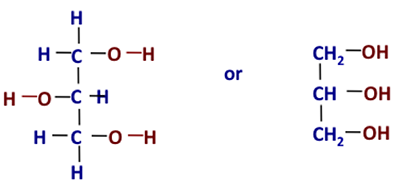
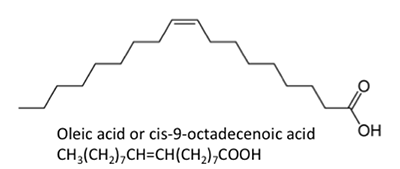
Il faut donc maintenant définir ce que sont les acides gras. Essentiellement, les acides gras sont des hydrocarbures à longue chaîne avec un acide carboxylique. La figure 9.3a montre la structure chimique générique d’un acide gras avec l’acide carboxylique dessus.

La figure 9.3b montre différentes structures chimiques d’acides gras. Les structures chimiques sont représentées sous forme de structures chimiques linéaires, où chaque point des liaisons est un atome de carbone et le nombre correct d’atomes d’hydrogène dépend de la présence d’une liaison simple ou double. Les acides gras peuvent être saturés (avec des liaisons hydrogène) ou insaturés (avec quelques doubles liaisons entre les atomes de carbone). En raison du métabolisme des plantes oléagineuses, les acides gras formés naturellement contiennent un nombre pair d’atomes de carbone. En chimie organique, les atomes de carbone ont quatre paires d’électrons disponibles à partager avec un autre atome de carbone, d’hydrogène ou d’oxygène. Les acides gras libres ne sont pas liés au glycérol ou à d’autres molécules. Ils peuvent être formés à partir de la dégradation ou de l’hydrolyse d’un triglycéride.
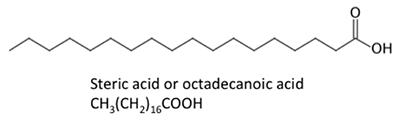
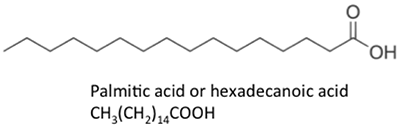
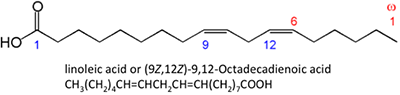
Les acides gras représentés ont des propriétés légèrement différentes. L’acide palmitique se trouve dans l’huile de palme. La figure 9.4 montre la relation de chaque acide gras avec sa taille et sa saturation. Les acides palmitique et stérique sont des acides gras saturés, tandis que les acides oléique et linoléique sont insaturés avec des quantités différentes de doubles liaisons. La figure 9.4 montre des quantités différentes d’atomes de carbone par rapport au nombre de doubles liaisons dans le composé.
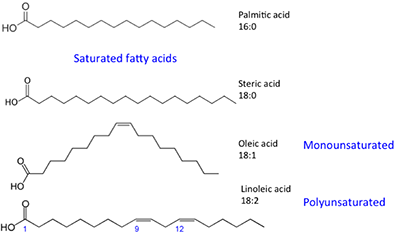
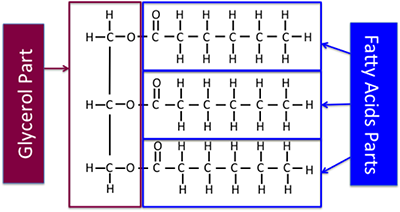
Figure 9.5a montre la partie du triglycéride qui est un acide gras et la partie qui est le glycérol, y compris les structures chimiques cette fois. La structure chimique présentée ici est un triglycéride saturé.
Donc, nous avons discuté de ce que sont les graisses et les huiles. Maintenant, qu’est-ce que le biodiesel ? Quelle en est au moins une définition ? C’est un carburant diesel qui a été généré à partir de la biomasse. Cependant, il existe différents types de biodiesel. Le type de biodiesel le plus connu est un carburant composé d’esters monoalkyliques (généralement des esters méthyliques ou éthyliques) d’acides gras à longue chaîne dérivés d’huiles végétales ou de graisses animales – ceci selon la norme ASTM D6551. Un ASTM est un document qui contient les normes relatives à des types particuliers de produits chimiques, notamment des matériaux industriels. C’est une définition verbeuse qui ne nous montre pas vraiment ce que c’est chimiquement.
Donc, quand on parle d’un groupe alkyle, c’est un radical univalent contenant uniquement des atomes de carbone et d’hydrogène dans une chaîne hydrocarbonée, avec une formule atomique générale de CnH2n+1. En voici quelques exemples :
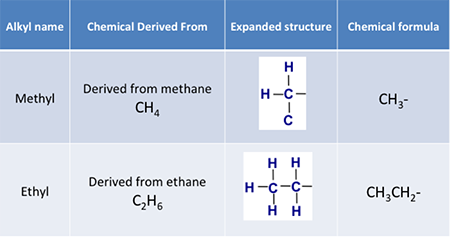
Un autre terme que nous devons connaître est un ester. Les esters sont des composés organiques où un groupe alkyle remplace un atome d’hydrogène dans un acide carboxylique. Par exemple, si l’acide est l’acide acétique et que le groupe alkyle est le groupe méthyle, l’ester résultant est appelé acétate de méthyle. La réaction de l’acide acétique avec le méthanol formera de l’acétate de méthyle et de l’eau ; la réaction est illustrée ci-dessous à la figure 9.6. L’ester formé par cette méthode est une réaction de condensation ; elle est également connue sous le nom d’estérification. Ces esters sont également appelés esters de carboxylate.
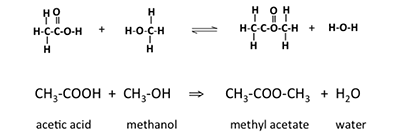
C’est la réaction de base qui aide à former le biodiesel. La figure 9.7 montre les différentes parties de la structure chimique du biodiesel, l’ester méthylique d’acide gras, ou ester méthylique d’acide gras (EMAG).
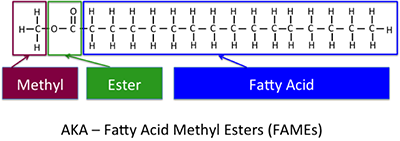
Alors, à ce stade, assurons-nous que nous savons ce dont nous avons discuté. Le biodiesel est un ester méthylique (ou éthylique) d’un acide gras. Il est fabriqué à partir d’huile végétale, mais ce n’est pas de l’huile végétale. Si nous avons du biodiesel à 100 %, il est appelé B100 – c’est une huile végétale qui a été transestérifiée pour produire du biodiesel. Il doit être conforme aux normes ASTM sur le biodiesel pour pouvoir bénéficier des garanties, être vendu comme biodiesel et bénéficier de tout crédit d’impôt. Le plus souvent, il est mélangé à du diesel à base de pétrole. S’il s’agit de B2, il contient 2 % de biodiesel et 98 % de diesel à base de pétrole. D’autres mélanges existent : B5 (5 % de biodiesel), B20 (20 % de biodiesel) et B100 (100 % de biodiesel). Nous verrons pourquoi les mélanges sont utilisés dans la section suivante. Et pour être clair : l’huile végétale est parfois utilisée dans les moteurs diesel, mais elle peut causer des problèmes de performance et détériorer les moteurs avec le temps. Parfois, l’huile végétale et l’alcool sont mélangés dans des émulsions, mais ce n’est toujours pas du biodiesel, car il a des propriétés différentes du biodiesel.
Alors, si l’huile végétale pure (SVO) peut fonctionner dans un moteur diesel, pourquoi ne pas l’utiliser ? L’huile végétale est nettement plus visqueuse (gluante est un terme non technique) et présente des propriétés de combustion plus médiocres. Elle peut provoquer des dépôts de carbone, une mauvaise lubrification du moteur, une usure du moteur et des problèmes de démarrage à froid. Les huiles végétales contiennent des gommes naturelles qui peuvent boucher les filtres et les injecteurs de carburant. Et pour un moteur diesel, le calage de l’injection est décalé et peut provoquer des cognements. Il existe des moyens d’atténuer ces problèmes, notamment : 1) mélanger avec du diesel à base de pétrole (généralement < 20%), 2) préchauffer l’huile, 3) faire des microémulsions avec des alcools, 4) « craquer » l’huile végétale, et 5) utiliser la méthode de conversion de l’OVO en biodiesel par transestérification. D’autres méthodes sont également utilisées, mais pour l’instant, nous nous concentrerons sur le biodiesel issu de la transestérification. Le tableau 9.1 présente trois propriétés du diesel n°2, du biodiesel et de l’huile végétale. Comme vous pouvez le constater, le principal changement concerne la viscosité. Le diesel n°2 et le biodiesel ont des viscosités similaires, mais les huiles végétales ont une viscosité plus importante et peuvent causer de gros problèmes par temps froid. C’est la principale raison de convertir le SVO en biodiesel.
| Carburant | Contenu énergétique (Btu/gal) |
Indice de cétane | Viscosité (centistokes) |
|---|---|---|---|
| No. 2 Diesel | 140 000 | 48 | 3 |
| Biodiesel | 130 000 | 55 | 5.7 |
| Huile végétale | 130 000 | 50 | 45 |
.