ATP, NAD ET FAD
ATP
Les cellules utilisent une molécule appelée Adénosine Triphosphate (ou ATP) comme source d’énergie (Voir figure 2). Les phosphates de cette molécule peuvent fournir de l’énergie aux substrats de nos cellules. Il existe dans nos cellules des enzymes qui peuvent retirer un phosphate de l’ATP et le fixer à une autre molécule, généralement une protéine (voir figure 3). Lorsque cela se produit, on dit que la protéine a été phosphorylée. Imaginez que le troisième phosphate est un petit sac d’énergie. Lorsqu’il est transféré à une protéine, cette énergie peut être utilisée pour faire quelque chose. Par exemple, dans la figure 3, la protéine change de forme lorsqu’elle est phosphorylée. Lorsque les protéines changent de forme, nous appelons souvent cela un changement de conformation de la structure de la protéine. Il existe de nombreuses protéines dans l’organisme qui utilisent un phosphate de l’ATP pour induire un changement de conformation. Ce changement de forme de la protéine permet finalement des choses comme la contraction musculaire, la mobilité cellulaire, le transport membranaire et l’action enzymatique. Les cellules et la vie n’existent que si un approvisionnement constant et régulier en ATP est disponible.
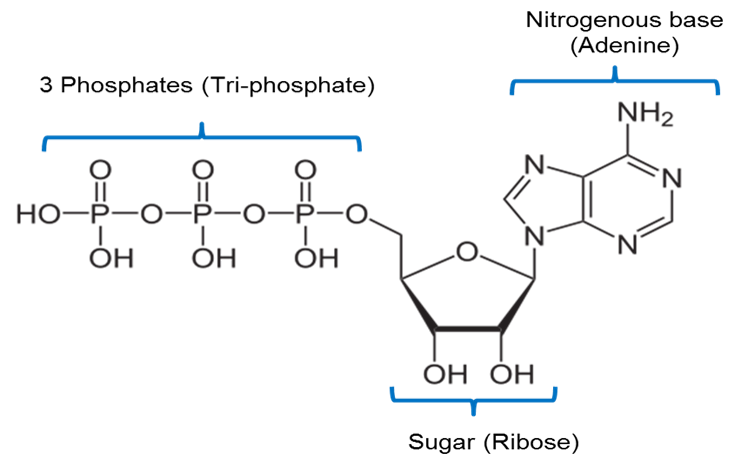
Image créée par JS à BYU Idaho F2013.
L’image ci-dessus est une représentation de la structure chimique de l’ATP. L’ATP comprend une base azotée appelée adénine jointe à un sucre à 5 carbones appelé ribose et 3 groupes phosphates.
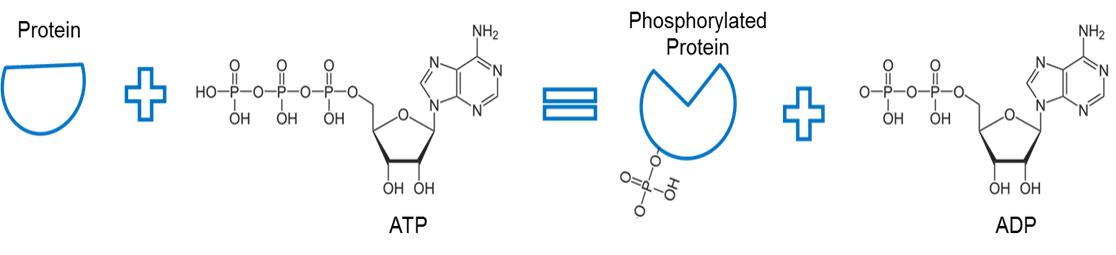
Image créée par JS à BYU Idaho F2013.
L’ATP est utilisé pour phosphoryler une protéine. Une enzyme, appelée kinase (non représentée) retire un phosphate de l’ATP et facilite une liaison entre le phosphate et une autre protéine. La liaison d’un phosphate à une protéine de cette manière est appelée phosphorylation. L’os phosphate avec la protéine a une énergie plus élevée. Remarquez que la phosphorylation utilise cette énergie pour provoquer un changement de conformation de la forme de la protéine.
NAD et FAD
Le nicotinamide adénine dinucléotide (NAD) et la flavine adénine dinucléotide (FAD) sont des coenzymes impliqués dans des réactions d’oxydation et de réduction réversibles. On dit souvent que ces composés sont des transporteurs d’électrons parce qu’ils acceptent des électrons (deviennent réduits) pendant les étapes cataboliques de la dégradation des molécules organiques telles que les glucides et les lipides. Ensuite, ces coenzymes réduits peuvent donner ces électrons à une autre réaction biochimique normalement impliquée dans un processus qui est anabolique (comme la synthèse de l’ATP).
NAD+ / NADH
Le nicotinamide adénine dinucléotide dans son état oxydé est appelé NAD+, après avoir été réduit (ou avoir accepté des électrons), il est appelé NADH. Voir la figure 4 pour une illustration moléculaire. La vitamine Niacine (également appelée B3) est utilisée pour dériver ce composé. La niacine fournit la structure du cycle organique qui participera directement au transfert d’un atome d’hydrogène et de 2 électrons. Le NAD+ se trouve souvent associé à une enzyme « déshydrogénase ». Une réaction de déshydrogénase élimine deux atomes d’hydrogène, l’un sous forme d’hydrure (:H-) (un hydrure est un atome d’hydrogène avec 2 électrons) et l’autre sous forme de cation d’hydrogène (H+) (et bien sûr, un cation d’hydrogène n’a pas d’électrons). L’hydrure se lie au NAD+ et crée un composé réduit de Nictinamide Adénine Dinucléotide (NADH). Le deuxième atome d’hydrogène (H+) est libéré dans la solution voir figure 4.
Lorsque vous examinez les réactions du métabolisme, recherchez les réactions qui produisent du NADH. Le NADH sera important car il livrera les hydrogènes et les électrons qu’il capte aux processus biochimiques qui peuvent utiliser les électrons et les hydrogènes pour fabriquer de l’ATP.
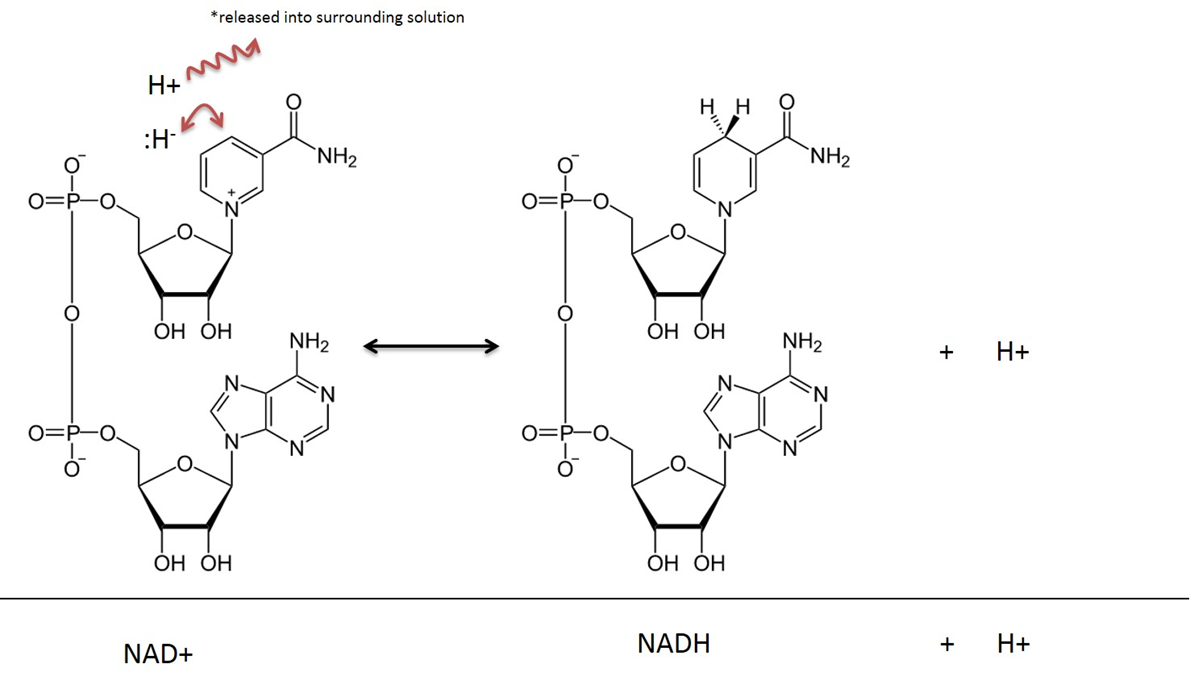
Image créée par JS à BYU Idaho F2013.
Dans les réactions métaboliques qui impliquent le NAD, deux atomes d’hydrogène et deux électrons sont retirés d’un substrat et transférés au NAD+. Le NAD+ accepte un ion hydrure (un hydrogène avec 2 électrons) et devient le Nicotinamide Adénine Dinucléotide sous la forme réduite (NADH). Le cation hydrogène qui est également capturé dans la réaction est libéré dans la solution environnante. Rappelez-vous que cette réaction est réversible.
Dans l’explication des réactions qui se produisent dans le Métabolisme, il est courant d’ignorer le H+ libéré dans la solution et ce texte représentera le résultat de la réduction du NAD comme étant simplement NADH, plutôt que NADH + H+.
FAD / FADH2
La flavine adénine dinucléotide dans son état oxydé est appelée FAD. Après avoir été réduit, il est appelé FADH2. Voir la figure 5 pour une illustration moléculaire. La vitamine, la riboflavine (ou B2) est utilisée pour dériver ce composé. La riboflavine fournit les structures cycliques qui vont participer directement au transfert de deux atomes d’hydrogène (chacun avec un électron cette fois). Comme le NAD, le FAD fonctionne en association avec une enzyme « déshydrogénase ». La réaction élimine deux atomes d’hydrogène, chacun étant un proton avec un électron. Les deux atomes d’hydrogène se lient au FAD. Cette réaction ne libère pas un H+ dans la solution comme le fait la réduction du NAD.
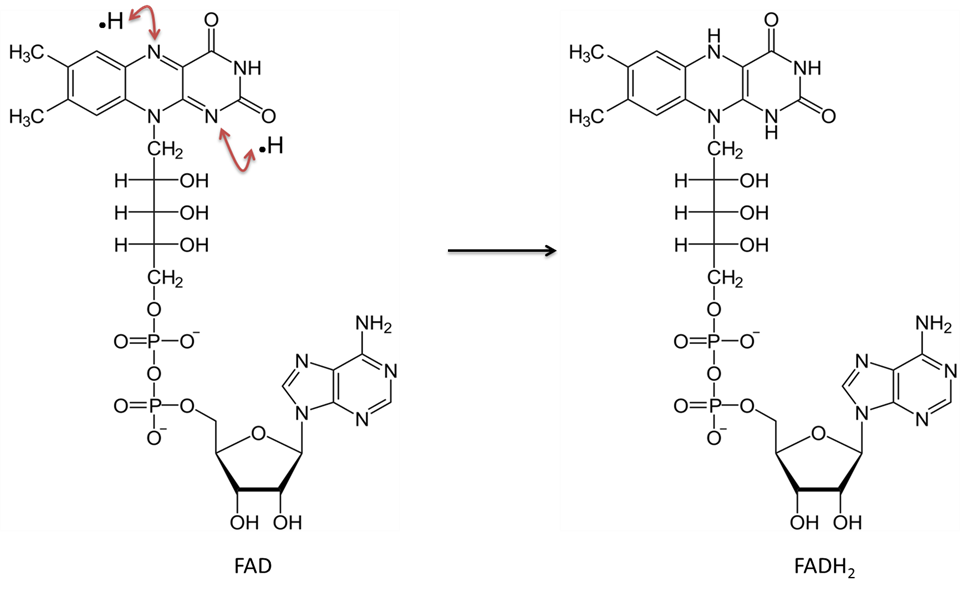
Image créée par JS à BYU Idaho F2013.
La flavine adénine dinucléotide sous la forme oxydée (FAD) accepte deux atomes d’hydrogène (chacun avec un électron) et devient FADH2.
Lorsque vous examinez les réactions du métabolisme, recherchez une réaction qui produit du FADH2. Comme le NADH, le FADH2 sera important car il livrera des hydrogènes et des électrons aux processus biochimiques qui pourront utiliser les électrons et les hydrogènes pour fabriquer de l’ATP.
**Vous pouvez utiliser les boutons ci-dessous pour passer à la lecture suivante ou précédente de ce module**

