ATP, NAD E FAD
ATP
Le cellule usano una molecola chiamata Adenosina Trifosfato (o ATP) come fonte di energia (Vedi figura 2). I fosfati in questa molecola possono fornire energia ai substrati nelle nostre cellule. Nelle nostre cellule esistono enzimi che possono rimuovere un fosfato dall’ATP e attaccarlo ad un’altra molecola, di solito una proteina (vedi figura 3). Quando questo accade, diciamo che la proteina è stata fosforilata. Pensa al terzo fosfato come a un piccolo sacco di energia. Quando viene trasferito a una proteina, questa energia può essere usata per fare qualcosa. Per esempio, nella figura 3, la proteina cambia forma quando viene fosforilata. Quando le proteine cambiano la loro forma, spesso lo chiamiamo un cambiamento conformazionale alla struttura della proteina. Ci sono molte proteine nel corpo che usano un fosfato dall’ATP per indurre un cambiamento conformazionale. Questo spostamento della forma della proteina permette alla fine cose come la contrazione muscolare, la mobilità cellulare, il trasporto di membrana e l’azione degli enzimi. Le cellule e la vita esistono solo se è disponibile una fornitura costante di ATP.
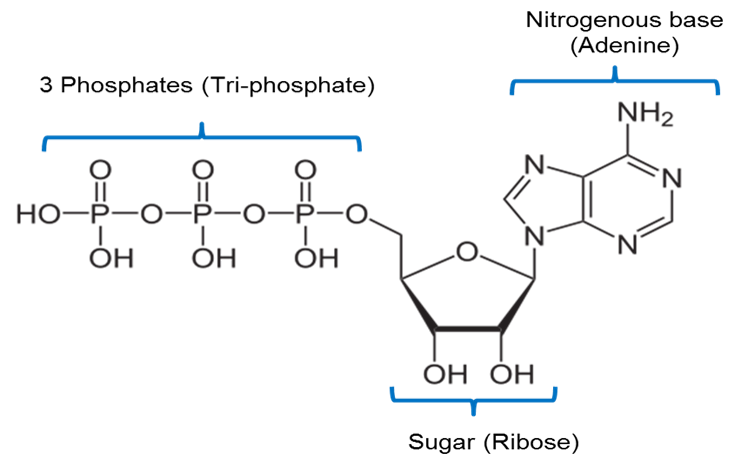
Immagine creata da JS a BYU Idaho F2013.
L’immagine sopra è una rappresentazione della struttura chimica dell’ATP. L’ATP comprende una base azotata chiamata adenina unita ad uno zucchero a 5 carboni chiamato ribosio e 3 gruppi fosfato.
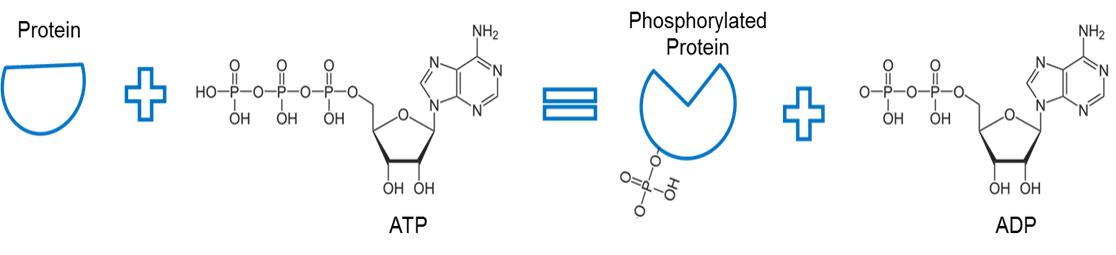
Immagine creata da JS a BYU Idaho F2013.
L’ATP è usato per fosforilare una proteina. Un enzima, chiamato chinasi (non mostrato) rimuove un fosfato dall’ATP e facilita un legame tra il fosfato e qualche altra proteina. Il legame di un fosfato con una proteina in questo modo è chiamato fosforilazione. L’osso fosfato con la proteina ha un’energia maggiore. Notate che la fosforilazione usa questa energia per causare un cambiamento conformazionale della forma della proteina.
NAD e FAD
Il nicotinamide adenina dinucleotide (NAD) e la flavina adenina dinucleotide (FAD) sono coenzimi coinvolti in reazioni reversibili di ossidazione e riduzione. Si dice spesso che questi composti sono portatori di elettroni perché accettano elettroni (si riducono) durante le fasi cataboliche nella scomposizione di molecole organiche come carboidrati e lipidi. Poi, questi coenzimi ridotti possono donare questi elettroni a qualche altra reazione biochimica normalmente coinvolta in un processo anabolico (come la sintesi di ATP).
NAD+ / NADH
Il nicotinamide adenina dinucleotide nel suo stato ossidato è chiamato NAD+, dopo essere stato ridotto (o aver accettato elettroni), è indicato come NADH. Vedere la figura 4 per un’illustrazione molecolare. La vitamina Niacina (chiamata anche B3) è usata per ottenere questo composto. La niacina fornisce la struttura organica ad anello che parteciperà direttamente al trasferimento di un atomo di idrogeno e 2 elettroni. Il NAD+ si trova spesso insieme a un enzima “deidrogenasi”. Una reazione di deidrogenasi rimuove due atomi di idrogeno; uno come idruro (:H-) (un idruro è un atomo di idrogeno con 2 elettroni) e uno come catione idrogeno (H+) (e naturalmente, un catione idrogeno non ha elettroni). L’idruro si lega con il NAD+ e crea un composto ridotto di Nictinamide Adenina Dinucleotide (NADH). Il secondo atomo di idrogeno (H+) viene rilasciato in soluzione, vedi figura 4.
Quando esamini le reazioni per il metabolismo, cerca le reazioni che producono NADH. Il NADH sarà importante perché consegnerà gli idrogeni e gli elettroni che prende ai processi biochimici che possono usare gli elettroni e gli idrogeni per fare ATP.
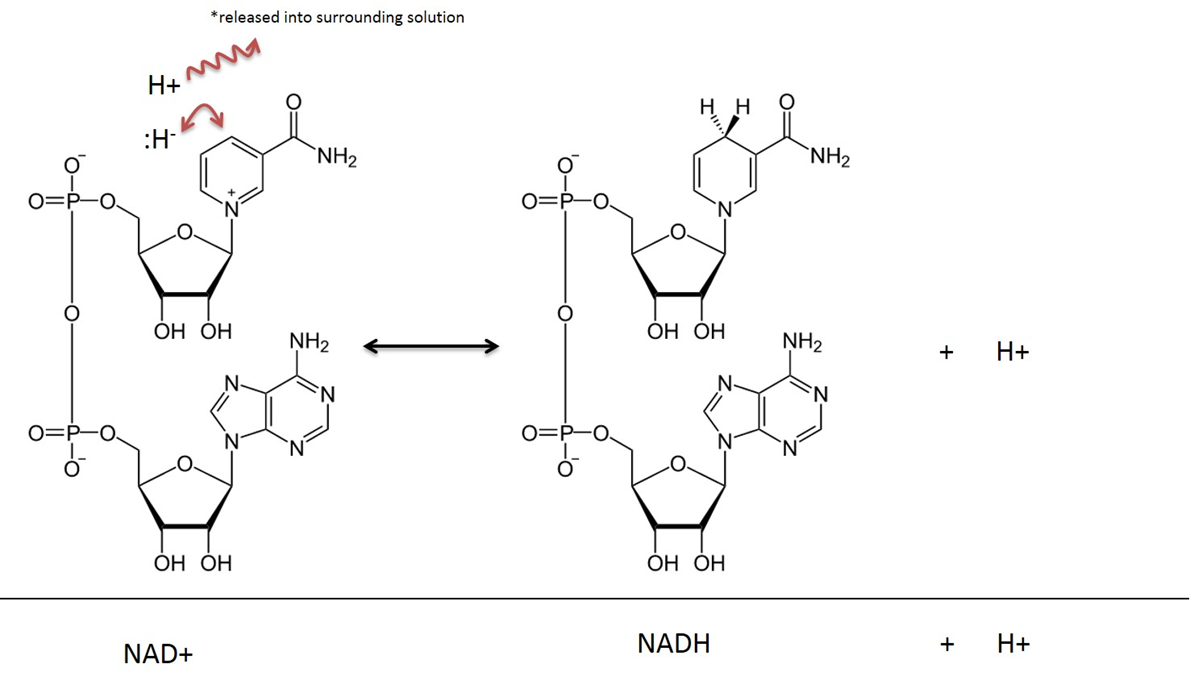
Immagine creata da JS a BYU Idaho F2013.
Nelle reazioni metaboliche che coinvolgono il NAD, due atomi di idrogeno e due elettroni sono rimossi da un substrato e trasferiti al NAD+. Il NAD+ accetta uno ione idruro (un idrogeno con 2 elettroni) e diventa Nicotinamide Adenina Dinucleotide in forma ridotta (NADH). Il catione idrogeno che viene catturato nella reazione viene rilasciato nella soluzione circostante. Ricorda che questa reazione è reversibile.
Nella spiegazione delle reazioni che avvengono nel metabolismo, è comune ignorare l’H+ rilasciato in soluzione e questo testo rappresenterà il risultato della riduzione del NAD semplicemente come NADH, piuttosto che NADH + H+.
FAD / FADH2
Il flavina adenina dinucleotide nel suo stato ossidato è chiamato FAD. Dopo essere stato ridotto, si chiama FADH2. Vedere la figura 5 per un’illustrazione molecolare. La vitamina riboflavina (o B2) è usata per ottenere questo composto. La riboflavina fornisce le strutture ad anello che parteciperanno direttamente al trasferimento di due atomi di idrogeno (ognuno con un elettrone questa volta). Simile al NAD, il FAD lavora in associazione con un enzima “deidrogenasi”. La reazione rimuove due atomi di idrogeno; ciascuno un protone con un elettrone. Entrambi gli atomi di idrogeno si legano con il FAD. Questa reazione non rilascia un H+ in soluzione come fa la riduzione del NAD.
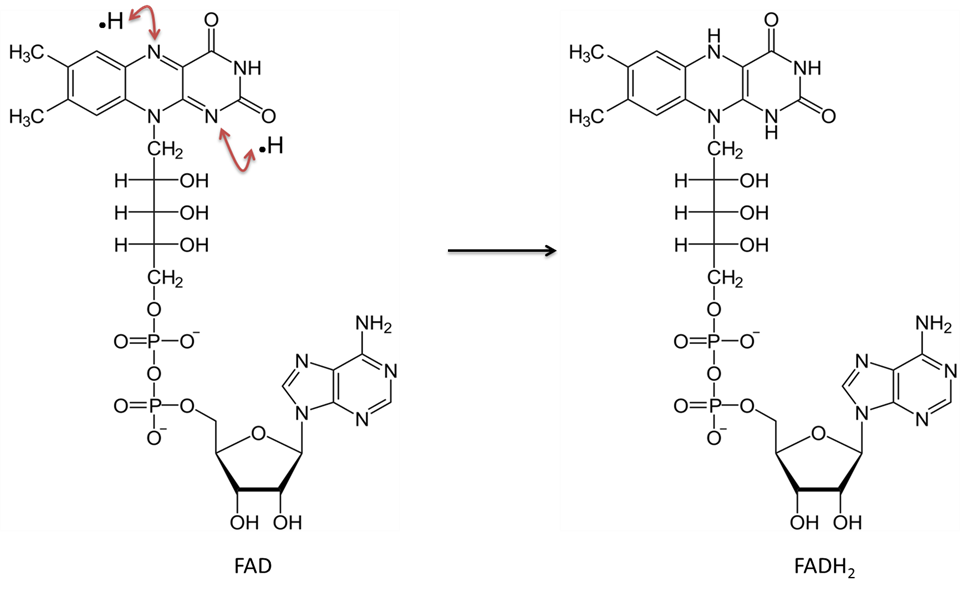
Immagine creata da JS a BYU Idaho F2013.
La flavin adenina dinucleotide nella forma ossidata (FAD) accetta due atomi di idrogeno (ciascuno con un elettrone) e diventa FADH2.
Esaminando le reazioni per il metabolismo, cerca una reazione che produca FADH2. Simile al NADH, il FADH2 sarà importante perché fornirà idrogeni ed elettroni ai processi biochimici che possono usare gli elettroni e gli idrogeni per fare ATP.
**Puoi usare i pulsanti qui sotto per andare alla lettura successiva o precedente in questo Modulo**

