ATP, NAD E FAD
ATP
Células usam uma molécula chamada Adenosina Trifosfato (ou ATP) como fonte de energia (Ver figura 2). Os fosfatos nesta molécula podem fornecer energia aos substratos das nossas células. Existem enzimas em nossas células que podem remover um fosfato de ATP e ligá-lo a uma molécula diferente – normalmente uma proteína (Veja Figura 3). Quando isto acontece, nós dizemos que a proteína foi fosforilada. Pense no terceiro fosfato como sendo um pequeno saco de energia. Quando é transferido para uma proteína, esta energia pode ser usada para fazer algo. Por exemplo, na figura 3, a proteína muda de forma quando se torna fosforilada. Quando as proteínas mudam a sua forma, muitas vezes chamamos a isto uma mudança conformacional da estrutura da proteína. Existem muitas proteínas no corpo que utilizam um fosfato de ATP para induzir uma mudança conformacional. Esta mudança de forma da proteína permite, em última análise, coisas como contração muscular, mobilidade celular, transporte de membranas e ação enzimática. As células e a vida só existem se um suprimento consistente e constante de ATP estiver disponível.
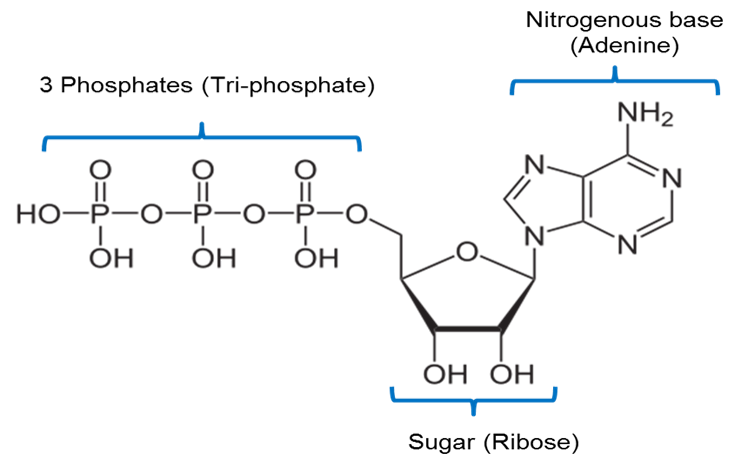
Imagem criada pelo JS na BYU Idaho F2013.
A imagem acima é uma representação da estrutura química do ATP. O ATP inclui uma base nitrogenada chamada adenina unida a 5 açúcares de carbono chamados ribose e 3 grupos de fosfato.
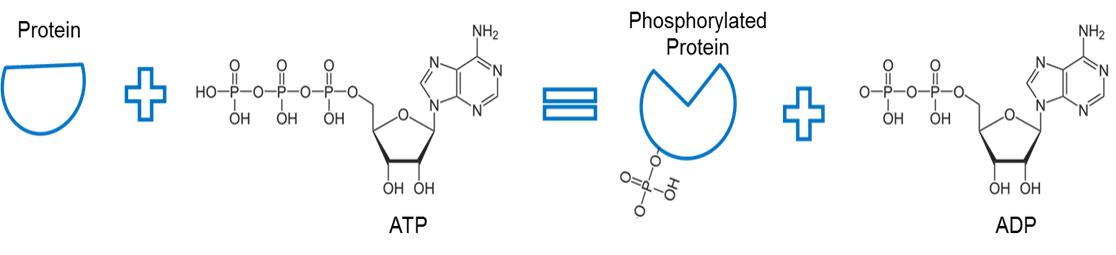
Imagem criada por JS em BYU Idaho F2013.
ATP é usada para fosforilatar uma proteína. Uma enzima, chamada cinase (não mostrada) remove um fosfato de ATP e facilita a ligação entre o fosfato e alguma outra proteína. A ligação de um fosfato a uma proteína desta forma é chamada fosforilação. O osso fosfatado com a proteína tem maior energia. Note que a fosforilação utiliza esta energia para causar uma mudança conformacional da forma da proteína.
NAD e FAD
Nicotinamida Adenina Dinucleotídeo (NAD) e Flavina Adenina Dinucleotídeo (FAD) são coenzimas envolvidas em reações de oxidação e redução reversíveis. Afirma-se frequentemente que estes compostos são portadores de electrões porque aceitam electrões (tornam-se reduzidos) durante os passos catabólicos na quebra de moléculas orgânicas como os hidratos de carbono e os lípidos. Então, estes coenzimas reduzidos podem doar estes elétrons a alguma outra reação bioquímica normalmente envolvida em um processo que é anabólico (como a síntese de ATP).
NAD+ / NADH
Nicotinamida Dinucleotídeo Adenina em seu estado oxidado é chamado de NAD+, depois de ser reduzido (ou aceitar elétrons), é chamado de NADH. Veja a figura 4 para uma ilustração molecular. A vitamina Niacina (também chamada B3) é usada para derivar este composto. A niacina fornece a estrutura do anel orgânico que irá participar diretamente na transferência de um átomo de hidrogênio e 2 elétrons. A NAD+ é frequentemente encontrada em conjunto com uma enzima “desidrogenase”. Uma reacção de desidrogenase remove dois átomos de hidrogénio; um como hidreto (:H-) (um hidreto é um átomo de hidrogénio com 2 electrões) e um como catião de hidrogénio (H+) (e claro, um catião de hidrogénio não tem electrões). O hidreto liga-se com NAD+ e cria um composto reduzido de Nictinamida Adenina Dinucleotídeo (NADH). O segundo átomo de hidrogênio (H+) é liberado em solução ver figura 4.
Ao examinar as reações para o metabolismo, procure por reações que produzem NADH. O NADH será importante pois irá fornecer os hidrogênios e elétrons que ele capta para processos bioquímicos que podem usar os elétrons e hidrogênios para fazer ATP.
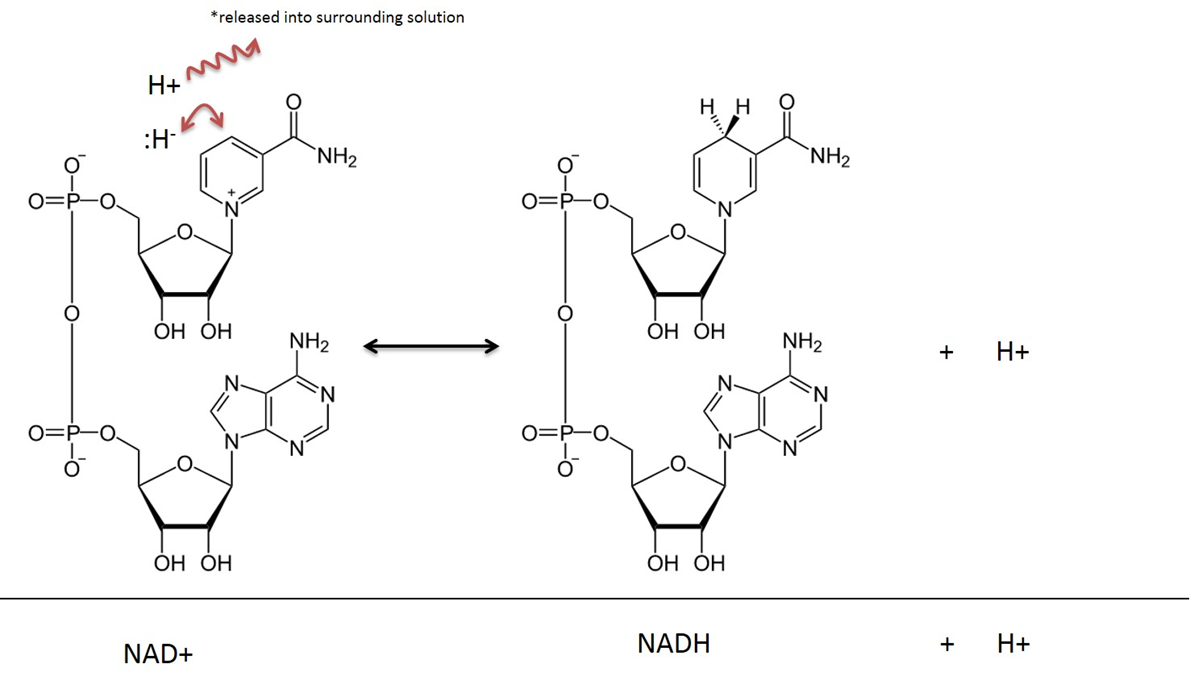
Imagem criada pelo JS na BYU Idaho F2013.
Em reações metabólicas que envolvem NAD, dois átomos de hidrogênio e dois elétrons são removidos de um substrato e transferidos para NAD+. O NAD+ aceita um íon hidreto (um hidrogênio com 2 elétrons) e se torna Nicotinamida Adenina Dinucleotídeo na forma reduzida (NADH). O cátion de hidrogênio que também é capturado na reação é liberado na solução ao redor. Lembre-se que esta reação é reversível.
Na explicação das reações que ocorrem no Metabolismo, é comum ignorar o H+ liberado em solução e este texto irá retratar o resultado da redução do NADH como simplesmente NADH, ao invés de NADH + H+.
FAD / FADH2
O dinucleotídeo adenina em seu estado oxidado é chamado de FAD. Após ser reduzido, é chamado de FADH2. Veja a figura 5 para uma ilustração molecular. A vitamina, riboflavina (ou B2) é usada para derivar este composto. A riboflavina fornece as estruturas anelares que irão participar directamente na transferência de dois átomos de hidrogénio (cada um com um electrão desta vez). Semelhante ao NAD, o FAD funciona em associação com uma enzima “desidrogenase”. A reação remove dois átomos de hidrogênio, cada um com um elétron. Ambos os átomos de hidrogênio se ligam ao DAD. Esta reacção não liberta um H+ em solução como a redução do NAD faz.
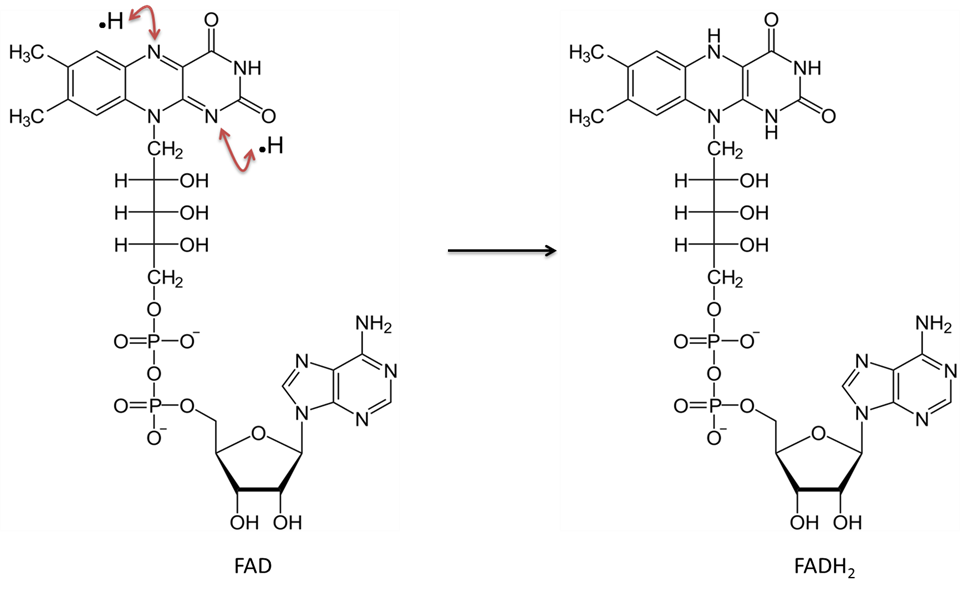
Imagem criada pelo JS na BYU Idaho F2013.
Dinucleótido adenino flamengo na forma oxidada (FAD) aceita dois átomos de hidrogénio (cada um com um electrão) e torna-se FADH2.
Ao examinar as reacções para o metabolismo, procure uma reacção que produza FADH2. Similar ao NADH, FADH2 será importante, pois irá fornecer hidrogênio e elétrons para processos bioquímicos que podem usar os elétrons e hidrogênios para fazer ATP.
**Você pode usar os botões abaixo para ir para a leitura seguinte ou anterior neste Módulo***

