ATP, NAD ȘI FAD
ATP
Celulele folosesc o moleculă numită adenozin trifosfat (sau ATP) ca sursă de energie (vezi figura 2). Fosfații din această moleculă pot furniza energie substraturilor din celulele noastre. În celulele noastre există enzime care pot îndepărta un fosfat din ATP și îl pot atașa la o altă moleculă – de obicei o proteină (Vezi figura 3). Când se întâmplă acest lucru, spunem că proteina a fost fosforilată. Gândiți-vă la cel de-al treilea fosfat ca fiind un mic sac de energie. Atunci când este transferat la o proteină, această energie poate fi folosită pentru a face ceva. De exemplu, în figura 3, proteina își schimbă forma atunci când devine fosforilată. Atunci când proteinele își schimbă forma, numim adesea acest lucru o modificare conformațională a structurii proteice. Există multe proteine în organism care folosesc un fosfat din ATP pentru a induce o schimbare conformațională. Această modificare a formei proteinei permite, în cele din urmă, lucruri precum contracția musculară, mobilitatea celulelor, transportul membranar și acțiunea enzimelor. Celulele și viața există doar dacă este disponibilă o cantitate constantă și constantă de ATP.
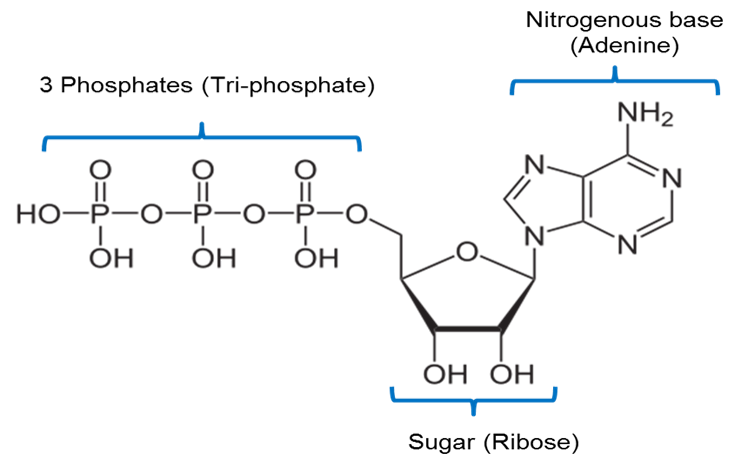
Imagine creată de JS la BYU Idaho F2013.
Imaginea de mai sus este o reprezentare a structurii chimice a ATP-ului. ATP include o bază azotată numită adenină unită cu un zahăr cu 5 atomi de carbon numit riboză și 3 grupe fosfat.
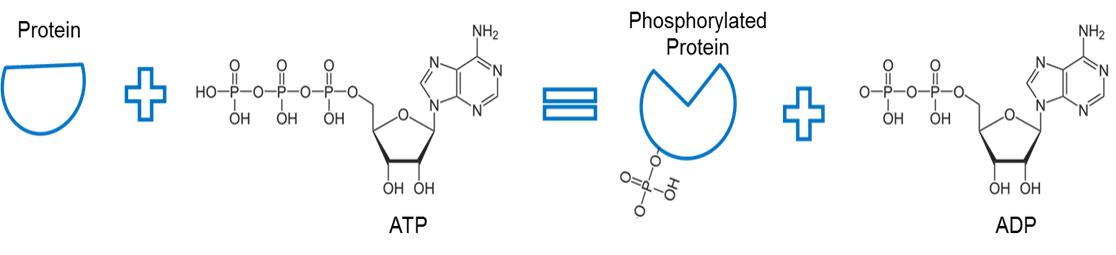
Imagine creată de JS la BYU Idaho F2013.
ATP este folosit pentru a fosforila o proteină. O enzimă, numită kinază (nu este prezentată) elimină un fosfat din ATP și facilitează o legătură între fosfat și o altă proteină. Legătura dintre un fosfat și o proteină în acest mod se numește fosforilare. Osul fosfat cu proteina are o energie mai mare. Observați că fosforilarea folosește această energie pentru a provoca o modificare conformațională a formei proteinei.
NAD și FAD
Nicotinamida adenin Dinucleotida (NAD) și Flavin Adenin Dinucleotida (FAD) sunt coenzime implicate în reacții reversibile de oxidare și reducere. Se afirmă adesea că acești compuși sunt purtători de electroni, deoarece acceptă electroni (se reduc) în timpul etapelor catabolice de descompunere a moleculelor organice, cum ar fi carbohidrații și lipidele. Apoi, aceste coenzime reduse pot dona acești electroni unei alte reacții biochimice implicate în mod normal într-un proces care este anabolic (cum ar fi sinteza de ATP).
NAD+ / NADH
Nicotinamida adenină dinucleotidă în starea sa oxidată se numește NAD+, după ce este redusă (sau acceptă electroni), se numește NADH. A se vedea figura 4 pentru o ilustrare moleculară. Vitamina Niacina (denumită și B3) este utilizată pentru a obține acest compus. Niacina asigură structura inelară organică care va participa direct la transferul unui atom de hidrogen și a 2 electroni. NAD+ se găsește adesea în combinație cu o enzimă „dehidrogenază”. O reacție de dehidrogenază elimină doi atomi de hidrogen; unul sub formă de hidridă (:H-) (o hidridă este un atom de hidrogen cu 2 electroni) și unul sub formă de cation de hidrogen (H+) (și, bineînțeles, un cation de hidrogen nu are electroni). Hidrida se leagă de NAD+ și creează un compus redus de Nictinamidă Adenină Dinucleotidă (NADH). Al doilea atom de hidrogen (H+) este eliberat în soluție, vezi figura 4.
În timp ce examinați reacțiile pentru metabolism, căutați reacțiile care produc NADH. NADH va fi important deoarece va livra hidrogenii și electronii pe care îi captează către procesele biochimice care pot folosi electronii și hidrogenii pentru a produce ATP.
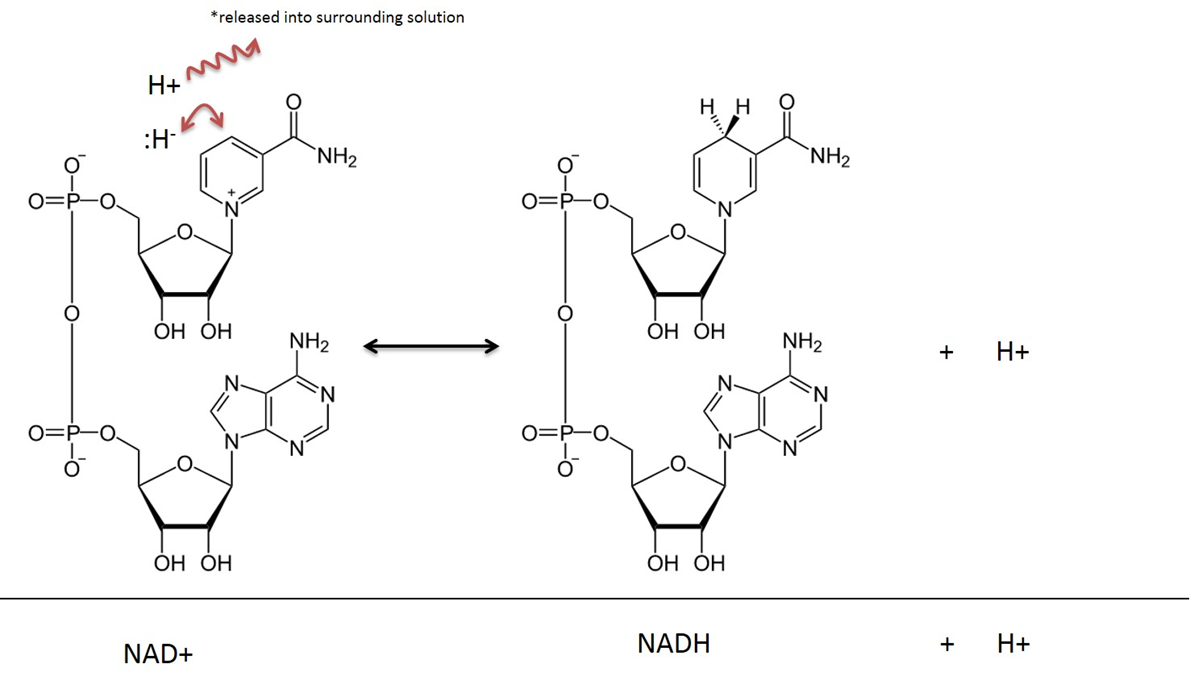
Imagine creată de JS la BYU Idaho F2013.
În reacțiile metabolice care implică NAD, doi atomi de hidrogen și doi electroni sunt îndepărtați de la un substrat și transferați la NAD+. NAD+ acceptă un ion hidrură (un hidrogen cu 2 electroni) și devine Nicotinamidă Adenină Dinucleotidă în formă redusă (NADH). Cationul de hidrogen care este, de asemenea, capturat în timpul reacției este eliberat în soluția înconjurătoare. Amintiți-vă că această reacție este reversibilă.
În explicarea reacțiilor care au loc în Metabolism, este obișnuit să se ignore H+ eliberat în soluție și acest text va descrie rezultatul reducerii NAD ca fiind pur și simplu NADH, mai degrabă decât NADH + H+.
FAD / FADH2
Flavin adenină dinucleotidă în starea sa oxidată se numește FAD. După ce este redusă, se numește FADH2. A se vedea figura 5 pentru o ilustrare moleculară. Vitamina, riboflavina (sau B2) este utilizată pentru a obține acest compus. Riboflavina furnizează structurile inelare care vor participa direct la transferul a doi atomi de hidrogen (fiecare cu câte un electron de data aceasta). Similar cu NAD, FAD funcționează în asociere cu o enzimă „dehidrogenază”. Reacția elimină doi atomi de hidrogen; fiecare un proton cu un electron. Ambii atomi de hidrogen se leagă de FAD. Această reacție nu eliberează un H+ în soluție, așa cum face reducerea NAD.
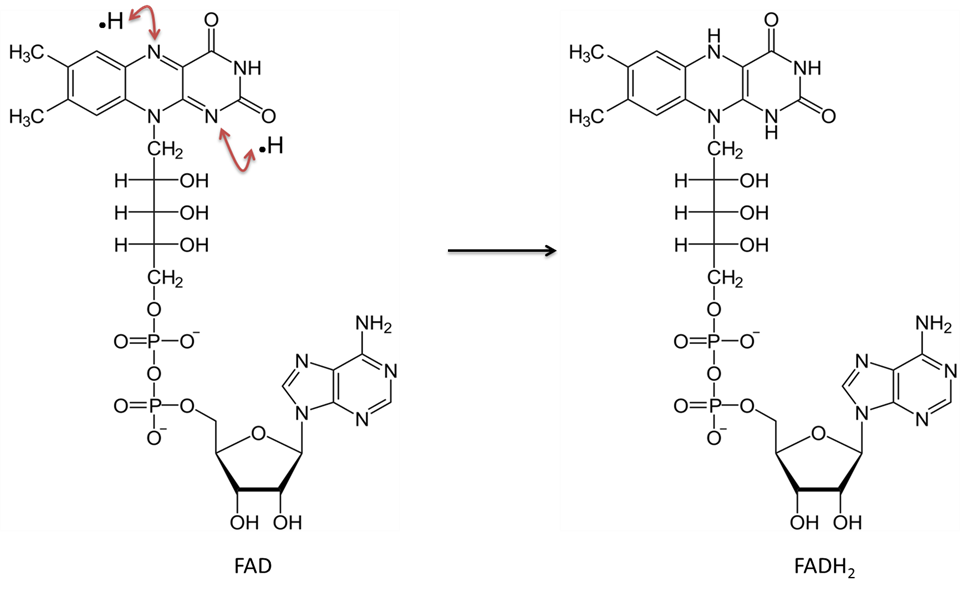
Imagine creată de JS la BYU Idaho F2013.
Flavin adenină dinucleotidă în forma oxidată (FAD) acceptă doi atomi de hidrogen (fiecare cu câte un electron) și devine FADH2.
În timp ce examinați reacțiile pentru metabolism, căutați o reacție care produce FADH2. La fel ca NADH, FADH2 va fi important deoarece va furniza hidrogeni și electroni proceselor biochimice care pot folosi electronii și hidrogenii pentru a produce ATP.
**Puteți folosi butoanele de mai jos pentru a trece la lectura următoare sau anterioară din acest modul**

