Imagine : „334 ” de Evan Blaser. Licență: CC BY-SA 2.0
- Definiții importante pentru a înțelege farmacodinamica
- Receptorii
- Efectorii
- Afinitate
- Selectivitate
- Specificitate
- Agonism
- Antagonism
- Sinergism
- Eficacitate
- Potența
- Excreție
- Eliminare
- Receptorii și efectorii
- Receptorii
- Efectorii
- Suprareglementare și subreglementare
- Suprareglementare
- Downregulation
- Curbe doză-răspuns
- Curbe de legare
- Receptorii de separare
- Toxicitate, curbe de toxicitate și raport terapeutic
Definiții importante pentru a înțelege farmacodinamica
Receptorii
Un receptor este acea componentă (macromoleculă) a unei celule (pe sau în interiorul celulei) care interacționează cu medicamentul, iar această interacțiune duce la un lanț de evenimente care modifică activitatea celulei.
Efectorii
Efectorii sunt molecule care acționează ca răspuns la medicament (sau, mai precis, la complexul medicament-receptor) și participă la lanțul de evenimente intracelulare menționat mai sus care conduc la efectele medicamentului.
Afinitate
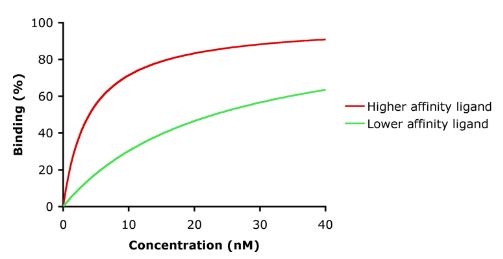
Afinitatea este măsura puterii legăturii dintre medicament și receptorul său. Afinitatea unui medicament față de receptorul său ajută la determinarea dozei de medicament: o afinitate scăzută ar indica necesitatea unei doze mai mari pentru a forma suficienți complecși medicament-receptor care să conducă la un efect semnificativ (a se vedea figura).

Selectivitate
Selectivitatea este preferința medicamentului pentru un receptor sau un subtip al acestuia (în comparație cu alți receptori sau alte subtipuri). Cu alte cuvinte, este capacitatea medicamentului de a produce un efect farmacologic în detrimentul altora. Dacă un medicament este selectiv, acesta se va lega de preferință la un singur receptor, dar se poate lega și la alții prin creșterea concentrației sale. De exemplu, verapamilul blochează în mod normal canalele Ca, dar poate bloca canalele Na la concentrații ridicate.
Specificitate
Specificitatea este capacitatea medicamentului de a se lega la un singur receptor. Atropina este specifică din punct de vedere tehnic deoarece acționează numai la receptorii de acetilcolină (ACh). Cu toate acestea, atropina nu este selectivă deoarece se leagă la toate subtipurile și provoacă o multitudine de efecte farmacologice.
Agonism
Când medicamentul interacționează cu receptorul pentru a produce o serie de evenimente care duc la un efect farmacologic, se numește agonism. De exemplu, izoprenalina este un agonist al adrenoreceptorilor β.
Antagonism
Când medicamentul interacționează cu receptorul, dar nu produce nicio serie de evenimente, „blocând” astfel acțiunea potențială (fizic sau chimic), se numește antagonism. De exemplu, propranololul este un antagonist al adrenoreceptorilor β.
Antagoniștii pot fi competitivi (prin legarea reversibilă la receptor) sau necompetitivi (se leagă ireversibil de receptor sau prin modificarea alosterică a conformației proteinei/enzimei). Acțiunea unui inhibitor competitiv poate fi inversată prin creșterea concentrației agonistului, în timp ce acest lucru nu se întâmplă în cazul inhibitorilor necompetitivi.
Sinergism
Când acțiunea unui medicament este crescută atunci când este administrat în prezența unui alt medicament, se numește sinergism. Exemple sunt aspirina și paracetamolul.
Eficacitate
Eficacitatea este proprietatea medicamentului de a produce efectul biologic (dorit). Eficacitatea este adesea utilizată atunci când se compară sau se evaluează medicamente în studiile clinice.
Potența
Potența este concentrația unui medicament necesară pentru a produce un efect de o anumită intensitate.
- Se calculează de obicei ca fiind concentrația (sau doza) necesară pentru a produce 50% din efectul maxim al medicamentului (EC>50).
- EC50 este utilizată numai în studiile in vitro. Atunci când potența unui medicament este măsurată într-o populație (studii pe animale sau populații umane), se utilizează un alt parametru numit doza mediană eficace sau ED50. ED50 este doza care produce efectul dorit (de obicei, un efect cuantic) la 50% din populație.
Când se aplică aceste concepte în mediul clinic, potența indică doar doza de medicament, în timp ce eficacitatea indică amploarea răspunsului (indiferent de doză).
Excreție
Excreția este eliminarea ireversibilă a medicamentului din organism. Excreția are loc în principal la nivelul ficatului și al rinichilor, dar pot fi implicate și alte organe (de exemplu, plămânii).
Eliminare
Eliminarea este procesul de inactivare a medicamentului cu/fără eliminarea efectivă din organism. Eliminarea poate avea loc ca urmare a excreției sau a metabolismului/biotransformării medicamentului. Astfel, în timp ce eliminarea este simpla inactivare a medicamentului, excreția este transferul fizic al medicamentului (forma activă sau inactivă a acestuia) din circulație în lichidele de excreție, cum ar fi urina și bila.
Receptorii și efectorii
Receptorii
Există cinci tipuri de bază de receptori transmembranari, care acționează, după legarea la medicament sau la ligand, în moduri diferite (vezi figurile).


- Receptorii intracelulari: Aceștia sunt receptori proteici care necesită ca medicamentul să traverseze membrana plasmatică; prin urmare, medicamentul trebuie să fie lipofil. Steroizii, de exemplu, acționează prin acest mecanism.
- Enzime transmembranare: Un medicament se leagă de componenta extracelulară a acestui receptor, care activează o reacție enzimatică în componenta intracelulară.
- Tirosin kinaza: Atunci când un medicament se leagă de componenta extracelulară a acestui receptor, acesta duce la dimerizarea celor două părți ale receptorului intracelular. Această dimerizare activează enzimele tirosin kinazei, conducând astfel la fosforilarea moleculelor de tirozină de pe proteinele țintă. Hormonii de creștere și interferonii acționează prin intermediul receptorilor JAK-STAT-kinazei.
- Canale ionice legate de liganzi: Aceste canale ionice sunt ligand-gated, adică sunt închise până când receptorul se leagă de medicament, ceea ce permite apoi trecerea unor ioni specifici. De exemplu, medicamentele care stimulează receptorii GABA de pe neuroni determină influxul de clorură (ceea ce duce la hiperpolarizare și, astfel, la inhibiție).
- Receptorii cuplați cu proteina G: Similar cu receptorii de tirozină kinază, legarea medicamentului de receptor duce la interacțiunea proteinei G cu receptorul. Această proteină G activată conduce apoi la răspunsul farmacologic dorit prin intermediul uneia sau al unei serii de molecule efectoare sau al unor mesageri secundari. Receptorii cuplați cu proteina G sunt tipuri comune de receptori în organism.
Efectorii
Transducția semnalului
Un medicament, atunci când se leagă de receptor (extracelular), acționează ca un „semnal” pentru evenimentul sau evenimentele ulterioare (intracelulare) care conduc în cele din urmă la răspunsul farmacologic. Această transmitere a semnalului se numește transducție a semnalului, iar lanțul intracelular de evenimente care sunt implicate în acest proces se numește cascade de transducție a semnalului.
Un număr de molecule (numite mesageri secundari) pot fi implicate în acest lanț de evenimente. Funcția cascadelor este de a amplifica semnalul medicamentului. După cum s-a menționat anterior, receptorii cuplați cu proteina G acționează prin intermediul unor mesageri secundari. O proteină G conține o subunitate α care leagă guanozin trifosfatul (GTP) și subunitățile β și γ care ancorează proteina în membrană.
- Subunitatea α se disociază cu celelalte două după legarea medicamentului-receptor, iar cei doi complecși disociați se pot lega de alte enzime pentru a genera cascadele.
- Un mecanism comun este legarea subunității α de enzima adenililciclază și activarea acesteia, ceea ce face ca ATP-ul din celulă să fie transformat în, este AMP ciclic (cAMP). (Activarea este cauzată de tipul Gs al proteinei G; Gi inhibă adenililciclaza). Concentrațiile crescute de fosfat anorganic se pot lega de țintă sau de alte molecule efectoare intermediare prin fosforilarea proteinelor.
Alte exemple de mesageri secundari sunt diacetilglicerolul (DAG), inositolul 1,4,5-trifosfat (IP3), ambele activate de proteina G de tip Gq; deoarece receptorii de proteină G folosesc fosforilarea ca mecanism de acțiune, aceștia sunt adesea susceptibili la fenomenul de desensibilizare.
Suprareglementare și subreglementare
Suprareglementare
Suprareglementare (de ex, creșterea numărului) de receptori apare atunci când activitatea receptorului este mai mică decât de obicei (de exemplu, din cauza administrării pe termen lung a unui antagonist). De exemplu, administrarea de beta-blocante suprareglează adrenoreceptorii β. Astfel, dacă β-blocantele sunt întrerupte brusc, se poate provoca hipertensiune arterială de revenire din cauza stimulării bruște a unui număr mare de β adrenoreceptori.
Downregulation
Downregulation (adică scăderea numărului) este inversul upreglementării. Ea apare ca urmare a administrării repetate sau pe termen lung a unui agonist. Împreună cu downregulation, poate avea loc și desensibilizarea receptorului la medicament. Aceasta este o alterare fizico-chimică a receptorului care îl face să nu mai răspundă la medicament; aceasta se mai numește și tahifilaxie și se observă, de exemplu, în cazul consumului cronic de droguri.
Curbe doză-răspuns
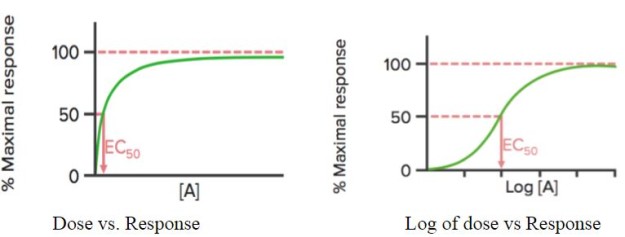

Când răspunsul medicamentului este trasat în funcție de doza sa , se observă o curbă hiperbolică; dacă se folosește logaritmul dozei (log), se observă o curbă sigmoidală.
Această curbă poate fi utilizată pentru a detecta concentrația (sau doza) eficace a medicamentului la care se obține 50% din răspunsul maxim (EC50) al medicamentului. După cum s-a menționat anterior, EC50 este utilizată pentru a calcula/compara potența medicamentelor.
Emax este concentrația (minimă) la care se observă efectul maxim al medicamentului. La Emax, toți receptorii sunt ocupați de medicament.
Curbe de legare
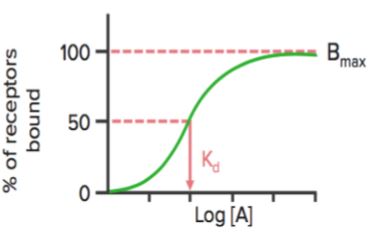

Când starea de legare a receptorilor (% de receptori legați) este reprezentată grafic în funcție de concentrația medicamentului ( sau log), aceasta prezintă o curbă hiperbolică (sau sigmoidală) similară.
Utilizând acest grafic, putem calcula concentrația efectivă la care sunt legați 50% din receptori (Kd). Kd arată afinitatea de legare a medicamentului – o valoare mare a lui Kd indică faptul că este necesară o concentrație mare de medicament pentru a lega 50% din receptori, indicând astfel o afinitate scăzută.
Bmax este legarea maximă a medicamentului. Este concentrația, exprimată în picomoli pe mg de proteină, la care toți receptorii specifici sunt legați de medicament. Ca urmare, Bmax poate fi folosită pentru a calcula densitatea situsului receptorului într-un anumit preparat.
Receptorii de separare
Când un agonist se leagă de un receptor, acesta poate produce o serie de evenimente care, în cele din urmă, conduc la răspunsul farmacologic. Această serie de evenimente poate amplifica efectul medicamentului astfel încât doar o cantitate relativ mică de complexe medicament-receptor poate fi necesară pentru a conduce la un răspuns maxim. În acest caz, atunci când se observă răspunsul maxim, un procent de receptori rămâne neocupat de medicament. Acești receptori se numesc receptori de rezervă.
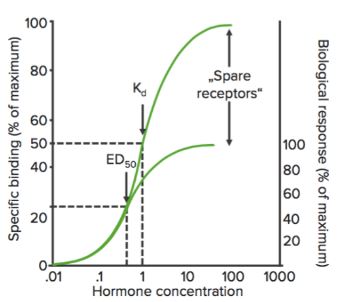

Receptorii de rezervă, cel puțin teoretic, cresc sensibilitatea medicamentului.
Toxicitate, curbe de toxicitate și raport terapeutic
Efectele adverse ale unui medicament sunt, de obicei, dependente de doză. Pentru a investiga eficacitatea și toxicitatea medicamentului, efectele sale sunt testate într-o populație și sunt reprezentate grafic în funcție de concentrație sau de doză. Se obțin curbe sigmoidale (dacă pe axa X se iau concentrații logaritmice), iar acestea pot reflecta efectele observate.
De exemplu, în figura următoare, un agent sedativ/hipnotic prezintă acțiunea sedativă la un anumit interval de concentrație și moartea dincolo de acest interval. Doza (sau concentrația) la care medicamentul prezintă efectul dorit (sedare) la 50% din populație este ED50.
Doza (sau concentrația) la care medicamentul prezintă efectele toxice (de exemplu, depresie respiratorie) la 50% din populație este TD50. Doza (sau concentrația) la care medicamentul prezintă efectul letal (moartea) la 50% din populație este LD50. (Aceasta este utilizată pentru experimentele pe animale.)
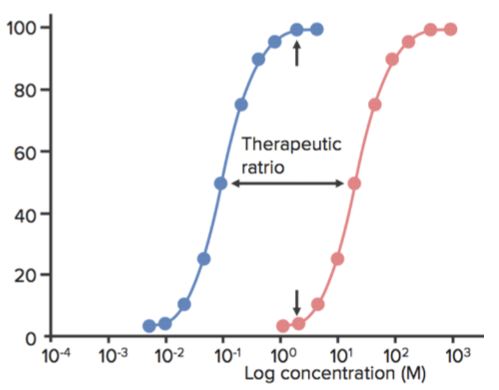

Fereastra terapeutică este intervalul de doze dintre concentrația minimă eficace și concentrația minimă toxică. Indicele terapeutic (IT) este definit ca fiind raportul dintre TD50 și ED50 sau TI=TD50/ED50.
- Acesta este uneori numit și raport terapeutic.
- Când un medicament are un IT scăzut, înseamnă că creșterea dozei sale poate produce cu ușurință efecte toxice (sau letale).
- Antidepresivele triciclice și litiul, de exemplu, au un IT scăzut și, prin urmare, doza lor trebuie monitorizată foarte atent la pacienți. Imipramina, de exemplu, poate fi fatală dacă este administrată în doze de 5-6 ori mai mari decât doza zilnică maximă.
- Cu cât TI este mai mare, cu atât medicamentul este mai sigur (exemplu este penicilina).
Învățați pentru școala medicală și comisii cu Lecturio.
- USMLE Step 1
- USMLE Step 2
- COMLEX Level 1
- COMLEX Level 2
- ENARM
- NEET
.