Hidrogenarea alchenelor în alcani este exotermă. Cantitatea de energie eliberată în timpul unei reacții de hidrogenare, cunoscută sub numele de căldura de hidrogenare, este invers legată de stabilitatea alchenei de plecare: cu cât alchena este mai stabilă, cu atât căldura sa de hidrogenare este mai mică. Examinarea căldurilor de hidrogenare pentru diferite alchene arată că stabilitatea crește odată cu gradul de substituție.
| Numele compusului | Structura | Căldura molară de hidrogenare | Gradul de substituție | ||
|---|---|---|---|---|---|
| în kJ/mol | în kcal/mol | ||||
| Etilenă | H 2 C = CH 2 {\displaystyle {\ce {H2C=CH2}}}}.
 |
137 | 32,8 | Nu substituită | |
| 1-Butena |
|
127 | 30.3 | Monosubstituit | |
| trans-2-Butena |
|
116 | 27.6 | Disubstituit | |
| 2-Methyl-2-butene |
 |
113 | 26.9 | Trisubstituit | |
| 2,3-Dimetil-2-butenă |
 |
111 | 26.6 | Tetrasubstituit | |
Creșterea stabilității asociată cu substituții suplimentare este rezultatul mai multor factori. Grupele alchil sunt donatoare de electroni prin efect inductiv și cresc densitatea de electroni pe legătura sigma a alchenei. De asemenea, grupările alchil sunt mari din punct de vedere steric și sunt mai stabile atunci când sunt departe una de cealaltă. În cazul unui alcan, separarea maximă este cea a unghiului legăturii tetraedrice, 109,5°. În cazul unei alchene, unghiul de legătură crește până aproape de 120°. Ca urmare, separarea dintre grupele alchilice este cea mai mare în alchena cea mai substituită.
Hiperconjugarea, care descrie interacțiunea stabilizatoare dintre HOMO al grupei alchilice și LUMO al dublei legături, ajută, de asemenea, la explicarea influenței substituirilor alchilice asupra stabilității alchenelor. În ceea ce privește hibridizarea orbitală, o legătură între un carbon sp2 și un carbon sp3 este mai puternică decât o legătură între doi carboni hibridizați sp3. Calculele relevă un efect dominant de hiperconjugare stabilizatoare de 6 kcal/mol per grup alchil.
Efecte stericeEdit
În reacțiile de eliminare E2, o bază absoarbe un proton care este beta la o grupare de plecare, cum ar fi o halogenură. Îndepărtarea protonului și pierderea grupării care pleacă au loc într-o singură etapă, concertată, pentru a forma o nouă legătură dublă. Atunci când se utilizează o bază mică, neîmpiedicată – cum ar fi hidroxidul de sodiu, metoxidul de sodiu sau etoxidul de sodiu – pentru o eliminare E2, produsul Zaitsev este de obicei favorizat față de alchena cel mai puțin substituită, cunoscută sub numele de produs Hofmann. De exemplu, tratarea 2-bromo-2-metilbutanului cu etoxid de sodiu în etanol produce produsul Zaitsev cu o selectivitate moderată.

Datorită interacțiunilor sterice, o bază voluminoasă – cum ar fi t-butoxidul de potasiu, trietilamina sau 2,6-lutidina – nu poate extrage cu ușurință protonul care ar conduce la produsul Zaitsev. În aceste situații, un proton mai puțin împiedicat din punct de vedere steric este abstractizat în mod preferențial. Ca urmare, produsul Hofmann este de obicei favorizat atunci când se utilizează baze voluminoase. Atunci când 2-bromo-2-metilbutanul este tratat cu t-butoxid de potasiu în loc de etoxid de sodiu, este favorizat produsul Hofmann.

Interacțiunile sterice din substrat împiedică, de asemenea, formarea produsului Zaitsev. Aceste interacțiuni intramoleculare sunt relevante pentru distribuția produselor în reacția de eliminare Hofmann, care transformă aminele în alchene. În eliminarea Hofmann, tratarea unei săruri de iodură de amoniu cuaternar cu oxid de argint produce ionul hidroxid, care acționează ca o bază și elimină amina terțiară pentru a da o alchenă.
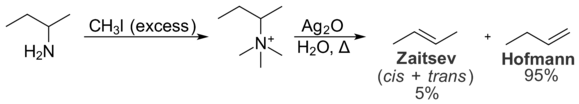
În eliminarea Hofmann, alchena cea mai puțin substituită este de obicei favorizată din cauza interacțiunilor sterice intramoleculare. Grupa de amoniu cuaternar este mare, iar interacțiunile cu grupele alchil din restul moleculei sunt nedorite. Ca urmare, conformația necesară pentru formarea produsului Zaitsev este mai puțin favorabilă din punct de vedere energetic decât conformația necesară pentru formarea produsului Hofmann. Prin urmare, produsul Hofmann se formează în mod preferențial. Eliminarea Cope este foarte asemănătoare, în principiu, cu eliminarea Hofmann, dar are loc în condiții mai blânde. Ea favorizează, de asemenea, formarea produsului Hofmann și din aceleași motive.
StereochimieEdit
În unele cazuri, stereochimia materialului de plecare poate împiedica formarea produsului Zaitsev. De exemplu, când clorura de mentol este tratată cu etoxid de sodiu, se formează exclusiv produsul Hofmann: dar cu randament foarte scăzut:

Acest rezultat se datorează stereochimiei materialului de plecare. Eliminările E2 necesită o geometrie antiperiplanară, în care protonul și grupul de plecare se află pe părți opuse ale legăturii C-C, dar în același plan. Atunci când clorura de mentol este desenată în conformație de scaun, este ușor de explicat distribuția neobișnuită a produsului.

Formarea produsului Zaitsev necesită eliminarea în poziția 2, dar gruparea izopropil – nu protonul – este antiperiplană față de gruparea clorură care pleacă; acest lucru face ca eliminarea în poziția 2 să fie imposibilă. Pentru ca produsul Hofmann să se formeze, eliminarea trebuie să aibă loc în poziția 6. Deoarece protonul din această poziție are orientarea corectă în raport cu grupul de plecare, eliminarea poate avea loc și are loc. Ca urmare, această reacție particulară produce doar produsul Hofmann.
.