Lid- und Gesichtskrämpfe können die Lebensqualität eines Patienten erheblich beeinträchtigen, doch kann es für den Arzt eine Herausforderung sein, die Ursache des Krampfes zu finden – es kann sich um eine Myokymie, einen gutartigen essentiellen Blepharospasmus oder einen hemifazialen Spasmus handeln. In diesem Artikel finden Sie Ratschläge, die Ihnen bei der Diagnose und Behandlung dieser manchmal schwierigen Zustände helfen können.
Ein Überblick
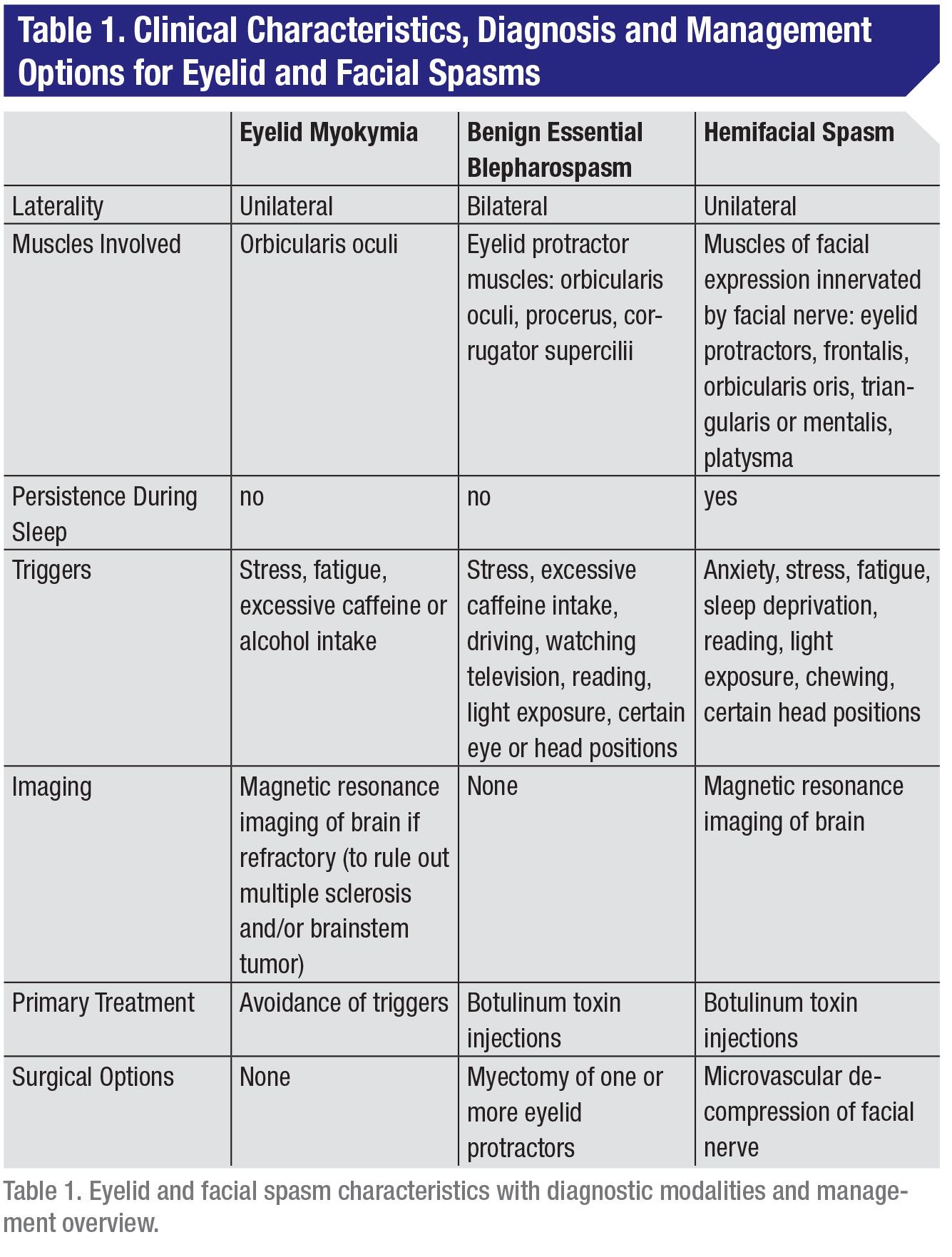
In der neurologischen und ophthalmologischen Praxis umfasst das Spektrum der Augenlid- und Gesichtskrämpfe, geordnet von der geringsten bis zur schwersten Ausprägung, die Lidmyokymie (unwillkürliche, kleine Lidkontraktionen), den gutartigen essentiellen Blepharospasmus (unwillkürliche Krämpfe, die dazu führen, dass sich das Auge teilweise oder vollständig schließt) und den hemifazialen Spasmus (Krämpfe in den Muskeln, die die Mimik steuern) (Tabelle 1). Bei all diesen Störungen handelt es sich um unwillkürliche Gesichtsbewegungen, die für die Patienten im täglichen Leben schwer zu bewältigen sind.
Augenlidmyokymie
Die häufigste unwillkürliche Bewegungsstörung im Gesicht ist die Augenlidmyokymie. Bei der Lidmyokymie kommt es zu unwillkürlichen, feinen, kontinuierlichen, wellenförmigen, nicht synchronen Kontraktionen der quergestreiften Muskelfasern der Augenlidprotraktoren. In der Elektrophysiologie ist sie durch spontane asynchrone Entladungen benachbarter motorischer Einheiten in Zweier- oder Dreiergruppen mit einer Frequenz von 30 bis 70 Hertz und Intervallen von 100 bis 200 ms zwischen den einzelnen Entladungen gekennzeichnet.2,3 Die Augenlidmyokymie gilt als gutartiger, selbstlimitierender Prozess, der einseitig und intermittierend auftritt, wobei das Unterlid stärker betroffen ist als das Oberlid. Die Episoden sind vorübergehend und dauern von einigen Tagen bis zu einigen Wochen oder Monaten, wobei die Krämpfe mit Unterbrechungen über den Tag verteilt bis zu mehreren Stunden am Stück auftreten.4
Zu den auslösenden Faktoren gehören Stress, Erschöpfung, übermäßiger Koffein- oder Alkoholkonsum und körperliche Anstrengung.5 Es wird empfohlen, diese Auslöser im Rahmen der Behandlung zu beseitigen. Die Augenlidmyokymie ist meist auf den Musculus orbicularis oculi beschränkt, kann sich aber auch auf weitere Muskeln einer oder beider Gesichtsseiten ausbreiten. In diesem Fall spricht man von einer Gesichtsmyokymie.2
Die Gesichtsmyokymie wird durch eine Schädigung des Gesichtsnervenkerns in der Pons aufgrund von demyelinisierenden Erkrankungen wie Multipler Sklerose oder einer Kompression durch Hirnstammtumore verursacht. In seltenen Fällen wurde eine persistierende Augenlidmyokymie als Symptom einer Multiplen Sklerose oder eines Hirnstammtumors berichtet.3 Wenn die Erkrankung chronisch ist, auf die Beseitigung der auslösenden Faktoren nicht anspricht und die Lebensqualität des Patienten beeinträchtigt, können Botulinumtoxin-Injektionen eine erfolgreiche Behandlung darstellen. Der Mechanismus und die Wirksamkeit von Botulinumtoxin-Injektionen werden im folgenden Abschnitt ausführlich erläutert. Eine anhaltende Lidmyokymie, die auf die oben genannten Behandlungen nicht anspricht, sollte den Verdacht auf eine Hirnstammläsion, wie oben beschrieben, erwecken und rechtfertigt eine Analyse mittels Magnetresonanztomographie.
Benigner essentieller Blepharospasmus
BEB wurde erstmals 1857 als eine Störung mit unwillkürlichen Spasmen der Lidspreizmuskeln beschrieben, die zu einem teilweisen oder vollständigen Lidschluss führt. BEB tritt mit einer Häufigkeit von 1,4 bis 13,3 Fällen pro 100.000 Einwohner auf, betrifft Frauen dreimal häufiger als Männer und tritt am häufigsten im fünften bis siebten Lebensjahrzehnt auf.7,8 BEB tritt in den meisten Fällen sporadisch auf, aber 27 Prozent der Patienten haben Berichten zufolge ein Familienmitglied mit Dystonie, was auf eine mögliche genetische Komponente hindeutet.1
Die Pathophysiologie von BEB ist nicht gut verstanden. Studien mit Positronen-Emissions-Tomographie und funktioneller Magnetresonanztomographie haben eine Aktivierung von Hirnregionen gezeigt, die an der Kontrolle und Regulierung der für das Blinzeln verantwortlichen Muskeln beteiligt sind, darunter der Thalamus, das Striatum, der anteriore visuelle Kortex, der primäre motorische Kortex und das obere Kleinhirn.7,9Tierstudien haben gezeigt, dass eine Dopaminverarmung in der Substantia nigra die Hemmung des trigeminalen Blinzelreflexes verringert, was zu einer Überempfindlichkeit dieses Reflexes als Reaktion auf Licht und Trockenheit führt.10 Zu den auslösenden Faktoren für BEB gehören Stress, übermäßiger Koffeinkonsum, Autofahren, Fernsehen, Lesen, helles Licht, verschmutzte Luft, Wind, Lärm und bestimmte Augen- und Kopfbewegungen.11,12
Das klinische Bild der BEB besteht aus beidseitigen unwillkürlichen Krämpfen eines oder mehrerer Augenlidspannmuskeln, einschließlich des Orbicularis oculi, des Procerus und des Corrugatormuskels, mit Symptomen, die von einer leicht erhöhten Blinzelrate bis hin zu einem gewaltsamen Lidschluss reichen, der zu funktioneller Blindheit führen kann.1 Die BEB-Symptome bleiben während des Schlafs nicht bestehen, und es handelt sich um eine fortschreitende Erkrankung, bei der im Laufe der Zeit weitere Muskeln beteiligt sind.7 Bei einer Untergruppe von Patienten können Spasmen im mittleren oder unteren Gesichtsbereich auftreten, ein Zustand, der als Meige-Syndrom bezeichnet wird.1 Eine weitere Untergruppe von Patienten kann eine Apraxie des Augenlidöffnens entwickeln, bei der es zu einem Verlust der gemeinsamen Hemmung von Lidspreizern und -rückholern kommt, was zu einer nichtparalytischen Unfähigkeit führt, die Augenlider ohne Muskelspasmus zu öffnen.1
Die Patienten klagen auch häufig über das sensorische Symptom der Photophobie. Zu den vorgeschlagenen Mechanismen für die Photophobie gehört eine sympathisch aufrechterhaltene Schmerzstörung, bei der Blöcke des Ganglion cervicalis superior in früheren Berichten Linderung verschafft haben.11 Zu den zusätzlichen Behandlungsoptionen zur Kontrolle der Photophobie gehören die photochromatische Modulation mit FL-41-gefärbten Linsen oder sklerale Kontaktlinsen mit Fluorescein im Flüssigkeitsreservoir, die beide die Lichtintensität erhöhen, die von BEB-Patienten toleriert wird.13
Die Behandlung der Wahl für BEB ist die Injektion von Botulinumtoxin in die betroffenen Lidspreizmuskeln. Botulinumtoxin hemmt die Freisetzung von Acetylcholin aus dem präsynaptischen Terminal der neuromuskulären Verbindung und blockiert so die Fähigkeit des injizierten Muskels, sich zusammenzuziehen. Es gibt sieben Serotypen von Botulinumtoxin (A bis G). Die Typen A und B sind von der US Food and Drug Administration für die klinische Anwendung in den Vereinigten Staaten zugelassen. OnabotulinumtoxinA (Botox) wurde 1989 von der FDA für die BEB-Behandlung zugelassen und ist die am häufigsten verwendete Formulierung, obwohl auch IncobotulinumtoxinA, AbobotulinumtoxinA und RimabotulinumtoxinB zur Verwendung zugelassen sind.14 Injektionen sind etwa alle drei bis vier Monate erforderlich.11 Die FDA empfiehlt eine Anfangsdosis von 1,25 bis 2,5 Einheiten, die in jede betroffene Stelle injiziert werden, mit einer Höchstdosis von 15 Einheiten und drei Injektionsstellen pro Seite.14 Umfragen haben jedoch gezeigt, dass Augenchirurgen dazu neigen, BEB mit einer durchschnittlichen Anfangsdosis von 22,5 ±9,5 Einheiten zu behandeln.14
Typischerweise werden fünf bis acht Stellen um jedes Auge herum injiziert, wobei an jeder Stelle nicht mehr als 0,1 ml Botulinumtoxin injiziert wird, um eine Diffusion des Medikaments in benachbarte Muskeln zu verhindern.12 Bei der Behandlung des prätarsalen Teils des Musculus orbicularis oculi an den Oberlidern muss der Arzt darauf achten, dass er medial und lateral injiziert, um eine Injektion in den Musculus levator palpebrae superioris zu vermeiden, die zu einer Ptosis führen kann. Bei den Unterlidern werden die Injektionen zentral und seitlich vorgenommen, um eine Injektion in den Musculus obliquus inferior zu vermeiden, die zu einer Diplopie führen würde. Die Inzidenz von unerwünschten Wirkungen von Botulinumtoxin-Injektionen bei BEB-Patienten wurde mit etwa 20 Prozent angegeben, darunter Ekchymosen an der Injektionsstelle, trockenes Auge, Tränenfluss, Fremdkörpergefühl, Lagophthalmus, Diplopie und Ptosis.7
Zu den weiteren Medikamenten, die zur Behandlung von BEB eingesetzt werden, gehören Antipsychotika, Antiepileptika, Anxiolytika, Antidepressiva, Antihistaminika, Sedativa und Stimulanzien, von denen sich jedoch keine als langfristig wirksam erwiesen haben.15 Insbesondere Dopaminagonisten und Dopaminaufnahmehemmer haben sich als wirksam bei der Verringerung von Lidkrämpfen erwiesen, da Dopaminmangel in die Pathogenese von BEB einbezogen wurde.11 Methylphenidat, das die präsynaptische Wiederaufnahme von Dopamin und Noradrenalin blockiert, verringert nachweislich die Lidkrämpfe und die Bewertung der Behinderung.11 BEB-Patienten haben teilweise auf Gamma-Aminobuttersäure-Agonisten wie Benzodiazepine angesprochen, deren Einsatz jedoch durch die Nebenwirkung der Schläfrigkeit eingeschränkt ist.11
Wenn BEB auf eine medikamentöse Behandlung nicht anspricht oder ein Patient Botulinumtoxin-Injektionen nicht verträgt, kann ein chirurgischer Eingriff mit Myektomie in Betracht gezogen werden. Die primären Ziele dieses Eingriffs sind die Verringerung des Schweregrads der Spasmen und die Verlängerung des Zeitintervalls zwischen den Botulinum-Injektionen.11 Bei der chirurgischen Myektomie werden ein oder mehrere der Protraktormuskeln reseziert. Bei einer begrenzten Myektomie wird nur ein Teil des Musculus orbicularis oculi im Oberlid entfernt, während bei einer erweiterten Myektomie zusätzlich der Corrugator supercilii und der Protraktor entfernt werden.15
Zu den unerwünschten Wirkungen der Operation gehören eine schlechte Kosmese und die Notwendigkeit weiterer Operationen. Das Wiederauftreten von Symptomen nach einer chirurgischen Myektomie wurde in 30 bis 50 Prozent der Fälle nach sechs Monaten berichtet.12 Ein alternatives Verfahren ist die Durchtrennung des Nervus facialis, die die Lidprotraktoren effektiv denerviert, aber sekundär zu einer Lähmung des Nervus facialis führt und daher selten angewendet wird.15

Hemifazialer Spasmus
Schließlich handelt es sich bei HFS um eine einseitige, unwillkürliche Gesichtsbewegungsstörung, bei der die vom Nervus facialis innervierten Muskeln des Gesichtsausdrucks verkrampfen. Die geschätzte Inzidenz liegt bei etwa 10 Fällen pro 100.000, basierend auf Studien in Minnesota und Norwegen.16,17 HFS tritt in der Regel im vierten oder fünften Lebensjahrzehnt auf, wobei Frauen zwei- bis dreimal häufiger betroffen sind als Männer und Asiaten häufiger als Kaukasier.18 Bis zu einem Drittel der Patienten berichten über erschwerende Faktoren für HFS, darunter Angst, Stress, Müdigkeit, Schlafmangel, Lesen, Lichteinwirkung, Kauen oder bestimmte Kopfhaltungen.18 HFS wird häufig fälschlicherweise als funktionelle oder psychogene Erkrankung (in 38 Prozent der Fälle), als Tics (in 29 Prozent) und als Fazialisparese (in 9 Prozent) diagnostiziert.19 Die klinische Präsentation umfasst anfängliche Spasmen des Orbicularis oculi, die im Laufe der Zeit allmählich fortschreiten oder sich ausbreiten, um andere Muskeln einer Gesichtshälfte wie den Frontalis, Orbicularis oris, Triangularis oder Mentalis und sogar den Platysma-Muskel mit einzubeziehen.7,18 Die Symptome von HFS können während des Schlafs anhalten, während sie bei BEB nicht auftreten.
Die Pathophysiologie des HFS beinhaltet eine Kompression des Nervus facialis an seiner Wurzelaustrittszone (REZ) aus dem Hirnstamm, die erstmals 1947 beschrieben wurde.20 Die Kompression kann durch aberrante Gefäße verursacht werden, darunter die Arteria cerebellaris anterior inferior, die Arteria cerebellaris posterior inferior, die Arteria basilaris, die Arteria vertebralis, arteriovenöse Malformationen und sehr selten durch Tumore wie Akustikusschwannome, Meningeome, Ohrspeicheldrüsentumore und pilozytäre Astrozytome.7 Obwohl die Diagnose des HFS in erster Linie klinisch gestellt wird, sollte immer eine MRT-Untersuchung durchgeführt werden, um eine Kompression des Nervus facialis wie oben beschrieben auszuschließen. Eine elektromyographische Untersuchung kann auch durchgeführt werden, um eine pathognomonische seitliche Ausbreitungsreaktion von Impulsen zwischen benachbarten Fasern des Gesichtsnervs („ephaptische Übertragung“) nachzuweisen.20
Die Hauptstütze der Behandlung von HFS sind Botulinumtoxin-Injektionen, wie sie oben für BEB beschrieben wurden. Bei HFS werden fünf bis zehn Stellen auf der betroffenen Gesichtsseite mit einer Gesamtdosis von 10 bis 34 Einheiten OnabotulinumtoxinA pro Behandlung injiziert.20 Die endgültige Behandlung von HFS ist die neurochirurgische mikrovaskuläre Dekompression (MVD), um die Kompression des Gesichtsnervs an seinem REZ zu beheben. In früheren Studien erzielten etwa 95 Prozent der Patienten, die sich bei HFS einer MVD unterzogen, gute oder sogar ausgezeichnete Ergebnisse. Zu den unerwünschten Wirkungen gehörten Gesichtsnervenlähmungen in 19 Prozent, Hörverluste in 7 Prozent und Lähmungen der unteren Hirnnerven in 2,8 Prozent.21 In Anbetracht der Invasivität und der Risiken, die mit einem neurochirurgischen Eingriff verbunden sind, ist es äußerst wichtig, mit den Patienten ein offenes Gespräch über die Risiken und Vorteile der MVD gegenüber Botulinumtoxin-Injektionen oder einer Kombination aus beiden zur Behandlung von HFS zu führen.
Die definitive Behandlung des hemifazialen Spasmus ist die neurochirurgische mikrovaskuläre Dekompression (MVD), um die Kompression des Gesichtsnervs an seiner Wurzelaustrittszone zu lösen.
Zusammenfassend lässt sich sagen, dass Augenlid- und Gesichtsspasmen ein Spektrum von unwillkürlichen Gesichtsbewegungsstörungen darstellen, die die Lebensqualität und das psychische Wohlbefinden der Patienten stark beeinträchtigen können. Während bei der Behandlung die Vermeidung auslösender Faktoren empfohlen wird, haben sich Botulinumtoxin-Injektionen insbesondere bei BEB und HFS als Mittel der ersten Wahl erwiesen. In refraktären Fällen oder bei Patienten, die Botulinumtoxin-Injektionen nicht vertragen, kann jedoch eine chirurgische Therapie für BEB und HFS durchgeführt werden. In Anbetracht der häufigen Fehldiagnosen dieser Erkrankungen ist es wichtig, dass Ärzte mit den häufigsten Anzeichen und Symptomen vertraut sind, damit sie diese Patienten zur weiteren Untersuchung und Behandlung an Neurologen oder Augenärzte weiterleiten können. REVIEW
Dr. Gervasio ist Facharzt für Augenheilkunde am Wills Eye Hospital. Dr. Moster ist behandelnder Arzt in der neuro-ophthalmologischen Abteilung des Wills Eye Hospital und Professor für Neurologie und Augenheilkunde an der Thomas Jefferson University in Philadelphia. Er ist Vorsitzender der Neuroophthalmologie am Einstein Medical Center in Philadelphia.
1. Hwang CJ, Eftekhari K. Benign essential blepharospasm: What we know and what we don’t. Int Ophthalmol Clin 2018;58:1:11-24.
2. Miller NR. Eyelid myokymia. Surv Ophthalmol 2011;56:3:277-8.
3. Barmettler A, Dinkin MJ, Lelli GJ. Eyelid myokymia: Not always benign. Orbit 2011;30:6:289-90.
4. Jordan DR, Anderson RL, Thiese SM. Intractable orbicularis myokymia: Treatment alternatives. Ophthalmic Surg 1989;20:4:280-3.
5. Horowitz SH. Hemifazialer Spasmus und faziale Myokymie: Electrophysiological findings. Muscle Nerve 1987;10:422-427.
6. Mackenzie W. Case of intense and long-continued photophobia and blepharospasm, relieved by the inhalation of chloroform. Med Chir Trans 1857;40:175-178.
7. Ozzello DJ, Giacometti JN. Botulinumtoxine zur Behandlung von essentiellem Blepharospasmus und hemifazialem Spasmus. Int Ophthalmol Clin 2018;58:1:49-61.
8. Bradley EA, Hodge DO, Bartley GB. Benigner essentieller Blepharospasmus bei Einwohnern von Olmsted County, Minnesota, 1976-1995: Eine epidemiologische Studie. Ophthal Plast Reconstr Surg 2003;19:177-181.
9. Baker RS, Andersen AH, Morecraft RJ, et al. A functional magnetic resonance imaging study in patients with benign essential blepharospasm. J Neuroophthalmol 2003;23:11-15.
10. Schicatano EJ, Basso MA, Evinger C. Animal model explains the origins of the cranial dystonia benign essential blepharospasm. J Neurophysiol 1997;77:2842-2846.
11. Yen MT. Entwicklungen in der Behandlung des gutartigen essentiellen Blepharospasmus. Curr Opin Ophthalmol 2018;29:440-44.
12. Coscarelli JM. Essential blepharospasm. Semin Ophthalmol 2010;25:3:104-8.
13. Herz NL, Yen MT. Modulation der sensorischen Photophobie bei essentiellem Blepharospasmus mit chromatischen Linsen. Ophthalmology 2005;112:2208-2211.
14. Broadbent TJ, Wesley RE, Mawn LA. Eine Umfrage über aktuelle Blepharospasmus-Behandlungsmuster unter Augenchirurgen. Ophthalmic Plast Reconstr Surg 2016;32:1:24-7.
15. Ben Simon GJ, McCann JD. Benign essential blepharospasm. Int Ophthalmol Clin 2005;45:49-75.
16. Auger RG, Whisnant JP. Hemifazialer Spasmus in Rochester und Olmsted County, Minnesota, 1960 bis 1984. Arch Neurol 1990;47:1233-34.
17. Nilsen B, Le KD, Dietrichs E. Prävalenz von hemifazialem Spasmus in Oslo, Norwegen. Neurology 2004;63:1532-33.
18. Lefaucheur JP, Daamer NB, Sangla S, Guerinel CL. Diagnostik des primären hemifazialen Spasmus. Neurochiurgie 2018;64:2:82-86.
19. Martinez AR, Nunes MD, Immich ND, et al. Misdiagnosis of hemifacial spasm is a frequent event in the primary care setting. Arq Neuropsiquiatr 2014;72:119-22.
20. Campbell E, Keedy C. Hemifacial spasm: A note on the etiology in two cases. J Neurosurg 1947;4:342-47.
21. Huh R, Han IB, Moon JY, et al. Microvascular decompression for hemifacial spasm: Analyse der operativen Komplikationen bei 1582 konsekutiven Patienten. Surg Neurol 2008;69:153-57.