Generikus név: phendimetrazine tartrate
Adagolási forma: tabletta
Medically reviewed by Drugs.com. Utolsó frissítés: 2020. június 22.
- Áttekintés
- Mellékhatások
- Adagolás
- Szakmai
- Ellenyomások
- Még
Kizárólag RX
A Bontril Slow Release márkanév megszűnt az Egyesült Államokban.S. Ha ennek a terméknek a generikus változatait az FDA engedélyezte, előfordulhat, hogy rendelkezésre állnak generikus egyenértékű készítmények.
- Bontril leírása
- Bontril – Klinikai farmakológia
- A Bontril javallatai és alkalmazása
- Ellenejavallatok
- Figyelmeztetések
- Figyelmeztetések
- Kölcsönhatások
- Karcinogenezis, mutagenezis, a termékenység károsodása
- Reprodukció
- Alkalmazás terhesség alatt
- Szoptató anyák
- GYermekeknél történő alkalmazás
- Mellékhatások
- Droggal való visszaélés és függőség
- Ellenőrzött anyag
- Függőség
- Túladagolás
- Bontril adagolás és alkalmazás
- A szokásos felnőtt adagolás
- Hogyan kerül forgalomba a Bontril
- FELIRATKOZAT – 35 mg-os tabletta palackcímke
- Tovább a Bontril Slow Release (phendimetrazine)
- Fogyasztói források
- Szakmai források
- Kapcsolódó kezelési útmutatók
Bontril leírása
A fenimetrazin-tartarát, mint a dextro-izomer kémiai neve (2S,3S)-3,4-dimetil-2-fenilmorfolin L-(+)-tartarát (1:1).
Szerkezeti képlete:
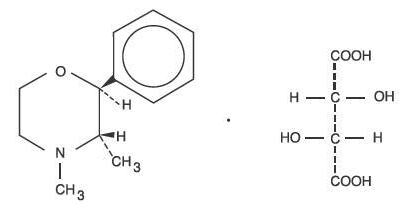
C12H17NO-C4H6O6 M.W. 341,36
A fenimetrazin-tartarát fehér, szagtalan kristályos por. Vízben szabadon oldódik; meleg alkoholban gyengén oldódik, kloroformban, acetonban, éterben és benzolban nem oldódik.
Mellett a következő inaktív összetevőket tartalmazza: Sajtolható cukor, cukrászcukor, D&C sárga #10, FD&C kék #1, FD&C sárga #6, izopropil-alkohol, vízmentes laktóz, magnézium-sztearát, mikrokristályos cellulóz, povidon, tisztított víz, nátrium-keményítő-glikolát.
Bontril – Klinikai farmakológia
A fenimetrazin-tartarát egy szimpatomimetikus amin, amelynek farmakológiai aktivitása hasonló az elhízásban használt, ebbe az osztályba tartozó gyógyszerek prototípusához, az amfetaminokhoz. Hatásai közé tartozik a központi idegrendszeri stimuláció és a vérnyomás emelkedése. Tachyphylaxist és toleranciát mutattak ki az ebbe az osztályba tartozó összes olyan gyógyszerrel, amelyeknél ezeket a jelenségeket keresték.
Az elhízásban használt, ebbe az osztályba tartozó gyógyszereket általában “anorectikumok” vagy “anorexigenikumok” néven ismerik. Nem bizonyított azonban, hogy az ilyen gyógyszerek hatása az elhízás kezelésében elsősorban az étvágycsökkentés lenne. Más központi idegrendszeri hatások vagy metabolikus hatások is szerepet játszhatnak például.
A diétás kezelésre oktatott és anorexiás gyógyszerekkel kezelt felnőtt elhízott személyek átlagosan többet fogynak, mint a placebóval és diétával kezeltek, amint azt viszonylag rövid távú klinikai vizsgálatokban megállapították.
A gyógyszerrel kezelt betegek nagyobb súlyvesztésének mértéke a placebóval kezelt betegekéhez képest csak heti egy font töredéke. A súlycsökkenés mértéke a kezelés első heteiben a legnagyobb mind a gyógyszerrel, mind a placebóval kezelt alanyok esetében, és a következő hetekben csökkenő tendenciát mutat. A különböző gyógyszerhatásokból eredő fokozott testsúlycsökkenés lehetséges eredete nem állapítható meg. Az anorexiás gyógyszerek alkalmazásával összefüggő testsúlycsökkenés mértéke vizsgálatról vizsgálatra változik, és úgy tűnik, hogy a fokozott testsúlycsökkenés részben az előírt gyógyszerektől eltérő változókkal függ össze, mint például a vizsgáló orvos, a kezelt populáció és az előírt étrend. A vizsgálatok nem engednek következtetéseket a gyógyszer és a nem gyógyszeres tényezők súlycsökkenésre gyakorolt relatív jelentőségére vonatkozóan.
Az elhízás természetes lefolyását években mérik, míg az idézett vizsgálatok néhány hetes időtartamra korlátozódnak; így a gyógyszer okozta súlycsökkenés teljes hatását a kizárólag diéta által okozotthoz képest klinikailag korlátozottnak kell tekinteni.
A kiválasztás fő útja a vesén keresztül történik, ahol a gyógyszer és a metabolitok nagy része kiválasztódik. A gyógyszer egy része fenmetrazin és fenmetrazin-N-oxiddá metabolizálódik. Az átlagos eliminációs felezési idő kontrollált körülmények között vizsgálva körülbelül 3,7 óra mind az elnyújtott, mind az azonnali felszabadulású formák esetében. A hatóanyag felszívódási felezési ideje a 35 mg-os, azonnali hatóanyag-leadású fenimetrazin tablettából érezhetően gyorsabb, mint a hatóanyag felszívódási sebessége az elnyújtott hatóanyag-leadású formulából.
A Bontril javallatai és alkalmazása
A Bontril®PDM (phendimetrazine tartrát) az exogén elhízás kezelésére javallt, rövid távú (néhány hetes) kiegészítésként egy kalóriaszűkítésen alapuló testsúlycsökkentő kezelésben olyan betegeknél, akiknek kezdeti testtömegindexe (BMI) 30 kg/m2 vagy magasabb, és akik nem reagáltak a megfelelő testsúlycsökkentő kezelésre (diéta és/vagy testmozgás) önmagában. Az alábbiakban a különböző testmagasságok és testsúlyok alapján számított testtömegindex (BMI) táblázat található. A BMI-t úgy számítják ki, hogy a beteg kilogrammban (kg) kifejezett testsúlyát elosztják a beteg méterben (m) kifejezett magasságának négyzetével. A metrikus átváltások a következők: font ÷ 2,2 = kg; hüvelyk x 0,0254 = méter.
| BODY MASS INDEX (BMI), kg/m2 magasság (láb, |
|||||||
|---|---|---|---|---|---|---|---|
| Súly (font) |
5’0″ | 5’3″ | 5’6″ | 5’6″ | 5’9″ | 6’0″ | 6’3″ |
| 140 | 27 | 25 | 23 | 21 | 19 | 18 | |
| 150 | 29 | 27 | 24 | 22 | 20 | 19 | |
| 160 | 31 | 28 | 26 | 24 | 22 | 20 | |
| 170 | 33 | 30 | 28 | 25 | 23 | 21 | |
| 180 | 35 | 32 | 29 | 27 | 25 | 23 | |
| 190 | 37 | 34 | 31 | 28 | 26 | 24 | |
| 200 | 39 | 36 | 32 | 30 | 27 | 25 | |
| 210 | 41 | 37 | 34 | 31 | 29 | 26 | |
| 220 | 43 | 39 | 36 | 33 | 30 | 28 | |
| 230 | 45 | 41 | 37 | 34 | 31 | 29 | |
| 240 | 47 | 43 | 39 | 36 | 33 | 30 | |
| 250 | 49 | 44 | 40 | 37 | 34 | 31 | |
A fendimetrazintartarát kizárólag monoterápiaként javallott.
Ellenejavallatok
Szimpatomimetikumokkal szembeni ismert túlérzékenység vagy idioszinkráziás reakciók.
Előrehaladott érelmeszesedés, tüneteket okozó szív- és érrendszeri betegség, mérsékelt és súlyos magas vérnyomás, pajzsmirigy túlműködés és glaukóma.
Nagyon ideges vagy izgatott betegek.
Múltban kábítószerrel visszaélő betegek.
Más CNS-stimulánsokat, beleértve a monoamino-oxidáz gátlókat is szedő betegek.
Figyelmeztetések
A fendimetrazintartarát nem alkalmazható más anorexiás szerekkel együtt, beleértve a felírt gyógyszereket, vény nélkül kapható készítményeket és növényi termékeket.
Egy eset-kontroll epidemiológiai vizsgálatban az anorexiás szerek, köztük a fendimetrazintartarát alkalmazása a pulmonális hipertónia, egy ritka, de gyakran halálos kimenetelű betegség kialakulásának fokozott kockázatával volt összefüggésben. Az anorexiás szerek három hónapnál hosszabb ideig történő alkalmazása a pulmonális hipertónia kialakulásának kockázatának 23-szoros növekedésével járt együtt. Nem zárható ki a pulmonális hipertónia megnövekedett kockázata az ismételt terápia során.
A terheléses nehézlégzés kezdete vagy súlyosbodása, illetve az angina pectoris, a syncope vagy az alsó végtagok ödémájának megmagyarázhatatlan tünetei a pulmonális hipertónia előfordulásának lehetőségére utalnak. Ilyen körülmények között a fendimetrazin-tartarátot azonnal abba kell hagyni, és a beteget ki kell vizsgálni a pulmonális hipertónia lehetséges jelenléte szempontjából.
Számoltak egyes anorexiás szerek, például fenfluramin és dexfenfluramin alkalmazásával összefüggő billentyűs szívbetegségről. A lehetséges hozzájáruló tényezők közé tartozik a hosszabb ideig tartó alkalmazás, az ajánlottnál nagyobb adag és/vagy más anorexiás gyógyszerekkel kombinált alkalmazás. A fenimetrazintartarát önmagában történő alkalmazásakor azonban nem számoltak be ilyen valvulopátiás esetekről.
A lehetséges súlyos mellékhatások, mint a szívbillentyű-betegség és a pulmonális hipertónia lehetséges kockázatát gondosan mérlegelni kell a testsúlycsökkenés lehetséges előnyeivel szemben. A phendimetrazin-kezelés megkezdése előtt meg kell fontolni a kardiológiai alapvizsgálatot a már meglévő szívbillentyű-betegségek vagy a pulmonális hipertónia kimutatására. A fendimetrazin-tartarát nem ajánlott ismert szívzörejben vagy billentyűs szívbetegségben szenvedő betegeknél. A kezelés alatt és után végzett echokardiográfia hasznos lehet az esetlegesen előforduló billentyűbetegségek kimutatására. Az indokolatlan expozíció és kockázatok csökkentése érdekében a fendimetrazin-tartarát kezelés csak akkor folytatható, ha a beteg a kezelés első 4 hetében kielégítő súlycsökkenést mutat (azaz legalább 4 font súlycsökkenés, vagy az orvos és a beteg által meghatározott módon).
A fendimetrazin anorexiás hatásával szemben néhány héten belül kialakul a tolerancia. Ha ez bekövetkezik, alkalmazását abba kell hagyni; a maximális ajánlott adagot nem szabad túllépni.
A fendimetrazin-tartarát monoamino-oxidáz-gátlók adását követő 14 napon belüli alkalmazása hipertóniás krízist eredményezhet.
A tartósan magas adagolást követően az alkalmazás hirtelen abbahagyása extrém fáradtságot és depressziót eredményez. A központi idegrendszerre gyakorolt hatása miatt a fendimetrazin-tartarát ronthatja a beteg képességét olyan potenciálisan veszélyes tevékenységek végzésére, mint a gépek kezelése vagy gépjárművezetés; a beteget ezért ennek megfelelően figyelmeztetni kell.
A fendimetrazin-tartarát nem ajánlott olyan betegek számára, akik az előző évben bármilyen anorexiás szert használtak.
Figyelmeztetések
A fendimetrazin felírásakor még enyhe hipertóniában szenvedő betegeknél is óvatosan kell eljárni.
A diabetes mellitusban az inzulinigény megváltozhat a fendimetrazin-tartarát alkalmazása és a kísérő diétás kezelés kapcsán.
A fendimetrazin-tartarát csökkentheti a guanetidin vérnyomáscsökkentő hatását. Egyszerre a lehető legkisebb mennyiséget kell felírni vagy kiadni a túladagolás lehetőségének minimalizálása érdekében.
Kölcsönhatások
A fendimetrazin-tartarát és más anorexiás szerek hatékonyságát nem vizsgálták, és az együttes alkalmazás súlyos szívproblémákat okozhat.
Karcinogenezis, mutagenezis, a termékenység károsodása
A fenimetrazin-tartaráttal végzett vizsgálatok nem értékelték a karcinogén, mutagén potenciált vagy a termékenységre gyakorolt hatást.
Reprodukció
C kategóriájú terhesség
A fenimetrazin-tartaráttal nem végeztek reprodukciós vizsgálatokat állatokon. Az sem ismert, hogy a fenimetrazin-tartarát okozhat-e magzati károsodást, ha terhes nőnek adják, vagy befolyásolhatja-e a reprodukciós képességet.
Alkalmazás terhesség alatt
A terhesség alatti biztonságos alkalmazás nem bizonyított. Amíg több információ nem áll rendelkezésre, a fendimetrazin-tartarátot nem szedhetik azok a nők, akik terhesek vagy terhesek lehetnek, kivéve, ha az orvos véleménye szerint a lehetséges előnyök meghaladják a lehetséges veszélyeket.
Szoptató anyák
Nem ismert, hogy ez a gyógyszer kiválasztódik-e az emberi tejbe. Mivel számos gyógyszer kiválasztódik az emberi tejbe, a fendimetrazin-tartarátot szoptató nők nem szedhetik, kivéve, ha az orvos véleménye szerint a lehetséges előnyök meghaladják a lehetséges veszélyeket.
GYermekeknél történő alkalmazás
A biztonságosság és hatékonyság gyermekbetegeknél nem bizonyított.
Mellékhatások
Kardiovaszkuláris: Palpitáció, tachycardia, emelkedett vérnyomás, iszkémiás események.
Szívbántalmakról számoltak be egyes anorexiás szerek, mint a fenfluramin és a dexfenfluramin alkalmazásával kapcsolatban, mind önállóan, mind különösen más anorexiás szerekkel együtt alkalmazva. Azonban nem számoltak be ilyen szívbillentyűbetegségről, amikor a fenimetrazin-tartarátot önmagában alkalmazták.
Központi idegrendszer: Túlstimuláció, nyugtalanság, álmatlanság, izgatottság, kipirulás, remegés, izzadás, szédülés, fejfájás, pszichotikus állapot, homályos látás.
Gasztrointesztinális: Szájszárazság, hányinger, hasmenés, székrekedés, gyomorfájdalom.
Húgyháztartás: Vizeletürítési gyakoriság, dysuria, a libidó megváltozása.
Droggal való visszaélés és függőség
Ellenőrzött anyag
Aontril® PDM (phendimetrazine tartrate) az lll. jegyzékben szereplő ellenőrzött anyag.
Függőség
A phendimetrazine tartrate kémiailag és farmakológiailag az amfetaminokkal rokon. Az amfetaminokkal és a rokon stimulánsokkal széles körben visszaéltek, és a fenimetrazin visszaélés lehetőségét szem előtt kell tartani, amikor értékeljük, hogy kívánatos-e a gyógyszer bevonása egy testsúlycsökkentő program részeként. Az amfetaminokkal és a rokon drogokkal való visszaélés intenzív pszichológiai függőséggel és súlyos szociális működési zavarokkal járhat. Vannak beszámolók olyan betegekről, akik az ajánlott dózis többszörösére emelték az adagot. A nagy dózisok tartós alkalmazását követő hirtelen abbahagyás extrém fáradtságot és mentális depressziót eredményez; az alvási EEG-n is megfigyelhetőek változások. Az anorexiás szerekkel történő krónikus mérgezés megnyilvánulásai közé tartoznak a súlyos dermatózisok, a kifejezett álmatlanság, az ingerlékenység, a hiperaktivitás és a személyiségváltozás. A krónikus mérgezések legsúlyosabb megnyilvánulása a pszichózis, amely klinikailag gyakran megkülönböztethetetlen a skizofréniától.
Túladagolás
A fendimetrazintartarát akut túladagolása a következő jelekben és tünetekben nyilvánulhat meg: szokatlan nyugtalanság, zavartság, harciasság, hallucinációk és pánikállapotok. A központi stimulációt általában fáradtság és depresszió követi. A kardiovaszkuláris hatások közé tartoznak a ritmuszavarok, a magas vérnyomás vagy a hipotenzió és a keringési összeomlás. A gasztrointesztinális tünetek közé tartozik a hányinger, hányás, hasmenés és hasi görcsök. A mérgezés görcsökhöz, kómához és halálhoz vezethet.
A túladagolás kezelése nagyrészt tüneti kezelés. Magában foglalja a barbituráttal történő nyugtatást. Ha a magas vérnyomás kifejezett, nitrát vagy gyors hatású alfa-receptor-blokkoló szer alkalmazását kell megfontolni. A hemodialízissel vagy peritoneális dialízissel kapcsolatos tapasztalatok nem elegendőek ahhoz, hogy ajánlásokat lehessen tenni az alkalmazásra vonatkozóan.
Bontril adagolás és alkalmazás
A szokásos felnőtt adagolás
1 tabletta (35 mg) naponta kétszer vagy háromszor egy órával étkezés előtt.
Az adagolást egyénre kell szabni, hogy a legalacsonyabb hatásos adaggal megfelelő választ lehessen elérni. Egyes esetekben ½ tabletta (17,5 mg) adagonként elegendő lehet. Az adagolás nem haladhatja meg a napi háromszor 2 tablettát.
Hogyan kerül forgalomba a Bontril
Háromrétegű, zöld, fehér és sárga színű tabletta, a bemetszett oldalon “B 35”, a másik oldalon “V” betűvel. A Bontril® PDM 35 mg fendimetrazin-tartarátot tartalmazó tabletta 100 (NDC 0187-0497-01) és 1000 (NDC 0187-0497-02) üvegben kapható.
25°C-on (77°F) tárolható; 15°C-30°C-ra (59°F-86°F) való eltérés megengedett.
DEA megrendelőlap szükséges.
A forgalmazó:
Valeant Pharmaceuticals North America
One Enterprise
Aliso Viejo, CA 92656 USA
Hozója:
Mallinckrodt, Inc.
Hobart, NY 13788
Elelmiszeripari minőségű tintával nyomtatva.
MG #20886
Rev. 10/07
Part No. L2BB01
FELIRATKOZAT – 35 mg-os tabletta palackcímke
NDC 0187-0497-02
RX Only
CIII
Bontril® PDM
(phendimetrazine tartrate tabletta, USP)
35 mg
Minden három rétegű
zöld, fehér és sárga
tabletta 35 mg
fendimetrazin
tartarátot
1000
tablettát
VALEANT™
| Bontril PDM fendimetrazin tartalmaz. tartrát tabletta |
||||||||||||||||||||||||||
|
||||||||||||||||||||||||||
|
||||||||||||||||||||||||||
|
||||||||||||||||||||||||||
|
||||||||||||||||||||||||||
|
||||||||||||||||||||||||||
|
||||||||||||||||||||||||||
Címkéző – Valeant Pharmaceuticals International (042230623)
| Egység | |||
| Név | Cím | ID/FEI | Működés |
| MALLINCKRODT INC | 957414238 | MANUFACTURE(0187-0497) | |
Tovább a Bontril Slow Release (phendimetrazine)
- Side Hatásai
- Terhesség alatt
- Adagolási információk
- Képek
- Kölcsönhatások
- 35 Vélemények
- A gyógyszercsoport:
Fogyasztói források
- Betegtájékoztatás
- Bontril (Korszerű olvasás)
- Bontril lassú-Release (Advanced Reading)
Szakmai források
- Receptköteles információk
- Phendimetrazin (AHFS monográfia)
Egyéb márkák Fendique ER
Kapcsolódó kezelési útmutatók
- Obesitás
Egészségügyi nyilatkozat