Az alkének alkánokká történő hidrogénezése exoterm. A hidrogénezési reakció során felszabaduló energia mennyisége, amelyet hidrogénezési hőnek nevezünk, fordítottan arányos a kiindulási alkén stabilitásával: minél stabilabb az alkén, annál kisebb a hidrogénezési hője. A különböző alkének hidrogénezési hőinek vizsgálata azt mutatja, hogy a stabilitás a szubsztitúció mennyiségével nő.
| Vegyület neve | Szerkezet | Moláris hidrogénezési hő | Szubsztitúciós fok | |
|---|---|---|---|---|
| in kJ/mol | in kcal/mol | |||
| Etiol | H 2 C = CH 2 {\displaystyle {\ce {\ce {H2C=CH2}}}
 |
137 | 32.8 | Subsztituálatlan |
| 1-Butén |
|
127 | 30.3 | Monoszubsztituált |
| transz-2-butén |
|
116 | 27.6 | Diszubsztituált |
| 2-metil-2-butén |
 |
113 | 26.9 | Triszubsztituált |
| 2,3-Dimetil-2-butén |
 |
111 | 26.6 | Tetraszubsztituált |
A további helyettesítésekkel járó stabilitásnövekedés több tényező eredménye. Az alkilcsoportok induktív hatásuk révén elektrondonorok, és növelik az elektronsűrűséget az alkén szigma kötésén. Emellett az alkilcsoportok sztérikusan nagyok, és akkor a legstabilabbak, ha távol vannak egymástól. Egy alkánban a legnagyobb távolság a tetraéderes kötésszög, 109,5°. Az alkénben a kötésszög 120° közelébe nő. Ennek eredményeként az alkilcsoportok közötti elválasztás a leginkább szubsztituált alkénben a legnagyobb.
A hiperkonjugáció, amely az alkilcsoport HOMO-ja és a kettős kötés LUMO-ja közötti stabilizáló kölcsönhatást írja le, szintén segít megmagyarázni az alkilszubsztituációk hatását az alkének stabilitására. Az orbitális hibridizáció tekintetében egy sp2 és egy sp3 szén közötti kötés erősebb, mint két sp3-hibridizált szén közötti kötés. A számítások egy domináns stabilizáló hiperkonjugációs hatást mutatnak ki, amely alkilcsoportonként 6 kcal/mol.
Szterikus hatásokSzerkesztés
Az E2 eliminációs reakciókban egy bázis elvon egy protont, amely béta egy távozó csoporthoz, például egy halogenidhez. A proton eltávolítása és a távozó csoport elvesztése egyetlen, összehangolt lépésben történik egy új kettős kötés kialakulásához. Ha egy kis, akadálymentes bázist – például nátrium-hidroxidot, nátrium-metoxidot vagy nátrium-etoxidot – használunk az E2 eliminációhoz, a Zaitsev-termék jellemzően előnyben részesül a legkevésbé szubsztituált alkénnel szemben, amelyet Hofmann-terméknek nevezünk. Például a 2-brom-2-metil-bután kezelése nátrium-etoxiddal etanolban mérsékelt szelektivitással a Zaitsev-terméket eredményezi.

A sztérikus kölcsönhatások miatt egy terjedelmes bázis – például kálium-t-butoxid, trietilamin vagy 2,6-lutidin – nem tudja könnyen elvonni a protont, amely a Zaitsev-termékhez vezetne. Ezekben a helyzetekben egy kevésbé sztérikusan akadályozott proton absztrahálódik helyette. Ennek eredményeképpen a Hofmann-termék jellemzően előnyben részesül, ha terjedelmes bázisokat használunk. Ha a 2-brom-2-metil-butánt nátrium-etoxid helyett kálium-t-butoxiddal kezeljük, a Hofmann-termék előnyben részesül.

A szubsztráton belüli sztérikus kölcsönhatások szintén megakadályozzák a Zaitsev-termék kialakulását. Ezek az intramolekuláris kölcsönhatások fontosak a termékek eloszlása szempontjából a Hofmann-eliminációs reakcióban, amely az aminokat alkénekké alakítja át. A Hofmann-elimináció során egy kvaterner ammónium-jodid só ezüst-oxiddal történő kezelése során hidroxidion keletkezik, amely bázisként viselkedik és eliminálja a tercier amint, így alkén keletkezik.
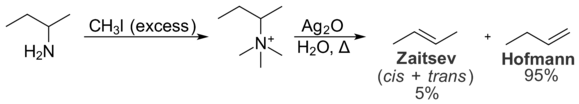
A Hofmann-elimináció során az intramolekuláris sztérikus kölcsönhatások miatt jellemzően a legkevésbé szubsztituált alkén kerül előnybe. A kvaterner ammóniumcsoport nagy, és a molekula többi részén lévő alkilcsoportokkal való kölcsönhatások nem kívánatosak. Ennek eredményeként a Zaitsev-termék kialakulásához szükséges konformáció energetikailag kevésbé kedvező, mint a Hofmann-termék kialakulásához szükséges konformáció. Ennek eredményeként a Hofmann-termék előnyben részesül. A Cope-elimináció elvileg nagyon hasonló a Hofmann-eliminációhoz, de enyhébb körülmények között történik. Ez is előnyben részesíti a Hofmann-termék képződését, és ugyanazokból az okokból.
SztereokémiaSzerkesztés
Egyes esetekben a kiindulási anyag sztereokémiája megakadályozhatja a Zaitsev-termék képződését. Például, ha mentil-kloridot nátrium-etoxiddal kezelünk, kizárólag a Hofmann-termék keletkezik: de nagyon alacsony hozammal:

Ez az eredmény a kiindulási anyag sztereokémiájának köszönhető. Az E2 eliminációhoz antiperiplanáris geometria szükséges, amelyben a proton és a kilépő csoport a C-C kötés ellentétes oldalán, de ugyanabban a síkban helyezkedik el. Ha a mentil-kloridot székkonformációban rajzoljuk meg, könnyen megmagyarázható a szokatlan termékeloszlás.

A Zaitsev-termék kialakulásához a 2-helyzetben történő elimináció szükséges, de az izopropilcsoport – nem a proton – antiperiplanáris a klorid kilépő csoportjával; ez lehetetlenné teszi a 2-helyzetben történő eliminációt. Ahhoz, hogy a Hofmann-termék létrejöjjön, az eliminációnak a 6-pozícióban kell megtörténnie. Mivel a proton ebben a pozícióban a megfelelő orientációval rendelkezik a kilépő csoporthoz képest, az elimináció megtörténhet és meg is történik. Ennek eredményeképpen ebben a reakcióban csak a Hofmann-termék keletkezik.