アジドイオン。 構造、性質、および置換反応
アジドイオン (N3- ) は、見た目が奇妙な化学物質の 1 つであります。

- 3つの窒素が並んでいるか? チェック
- 2つの負の電荷と正の電荷で、純電荷は-1? チェック
- 安定しているか? チェック(優しく扱う限りは)。
アジドイオンは求核置換反応においてC-N結合を形成するのに非常に有用であることがわかりました。
目次
- アジドイオンは偉大な求核剤
- 「覆面」アミンとしての有機アジド
- 発射台での爆発
- アジド塩による求核的アシル置換反応。 アシルアジド
- アシルアジドの転位。 Curtius転位
- アジド求核剤の他の例。 エポキシド開環と共役付加
- 注
- (上級)参考文献と参考図書
1. アジドイオンはSN2反応における優れた求核剤
アジドイオンはヒドラゾ酸(HN3)の共役塩基であり、アジ化したアジドイオンはSN2反応における求核剤として働く。 弱塩基性であるにもかかわらず(HN3のpKaはわずか4.6)、N3は非常に優れた求核性であり、ある指標によれば、どのアミンよりも求核性があります(投稿:Nucleophilicity of aminesを参照)。 このことは、考えてみればすぐにわかることだ。 4つの求核性ローンペアが非常に小さな体積に閉じ込められているため、親電子物質と衝突して反応が起こる可能性が、かさ高いアルキル基を持つアミンの場合よりもはるかに高くなるのです。
SN2反応では、1次および2次アルキルハライドとスルホン酸塩はN3-によって容易に置換され、アルキルアジドが生成します。
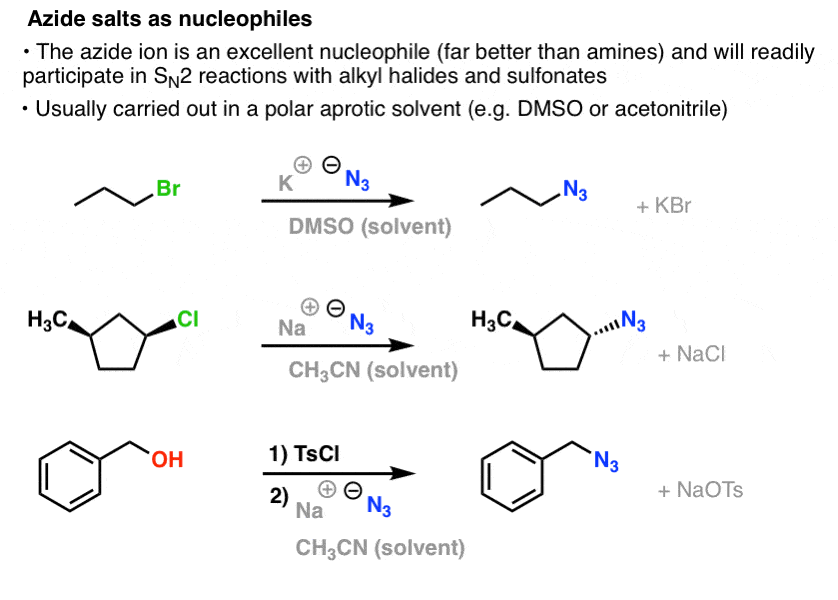
通常の手順は、アセトニトリル(CH3CN)やジメチルスルホキシド(DMSO)などの極性非沸点溶剤中で適切なアルキルハライドとNaN3またはKN3などのアジド塩を使用することです。
有機アジド化合物は、見た目が少し変でも、それなりに安定である。 中には医薬品(右下のAZTなど)や、化学生物学の研究に有用なプローブとして利用されているものもある。
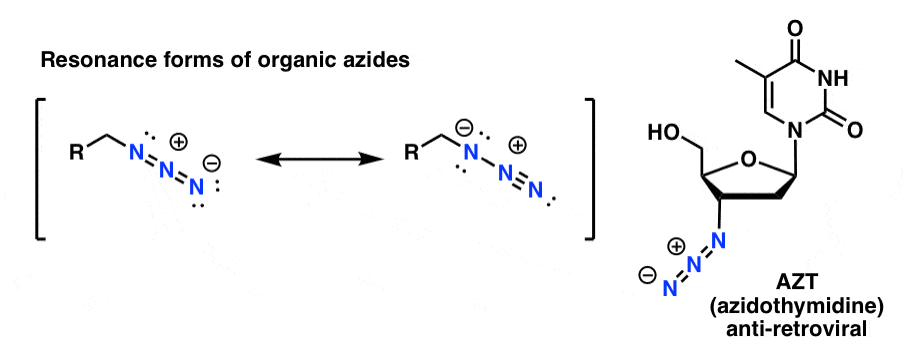
我々の目的にとって、有機アジドの最も有用な特性は、「覆面」アミンとして機能することである
2. マスクドアミンとしての有機アジド」
窒素-窒素三重結合を持つ上記の共鳴形態に注目する。 LiAlH4などの還元剤、あるいは触媒的水素化(Pd/C , H2)で処理すると、有機アジドは一次アミンに還元され、その過程で窒素を放出することができます。
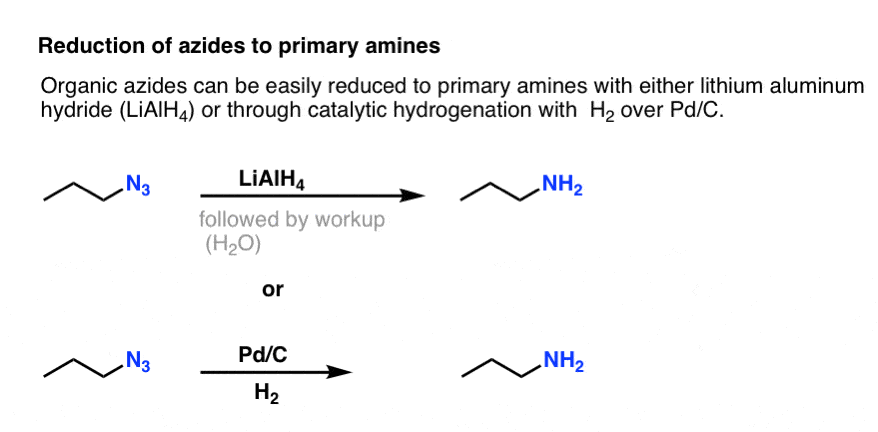
私たちは以前、一級アミンへのルートとしてガブリエル合成を調査しましたが、このルートは、アジドが穏やかな条件 (水素化など) でアミンに還元できる点で優れています。
また、ハロゲン化アルキルをNH3で直接処理して一級アミンを作ることは、しばしば目的の生成物につながらないことを見ました。これは、アミンの生成物が反応物よりも求核性である傾向があるので、アミンがハロゲン化アルキルを1回だけむさぼることに止まらないというクッキーモンスター(Cookie-Monster)に似た傾向があるためです。
Exploding On The Launchpad
上でコメントしたように、N3が「窒素チップ付きミサイル」だとすると、ミサイルが注意深く扱われないとどうなるか、それは本質的に爆弾であることを思い出す価値があると思います。
NaN3 や KN3 は白い粉末で、室温で無期限に保存でき、ベンチですくい取ることも問題ない。
しかし加熱したりショックを与えたりすると、すべてが水の泡となる。 また、これらのアジド塩を酸にさらすと、爆発性のあるHN3が生成される。
そしてNaN3やKN3は素晴らしいアジドである。 鉛、水銀、カドミウム、亜鉛、または銀の金属塩と混合すると、さらに爆発性の高いアジド化合物が生成されることがある。 これらの金属アジドは接触爆薬であり、中には誰かが3m先でオナラをしたら爆発するような敏感なものもある。 4735>
NaN3 と KN3 は適度に希薄な濃度で、分取スケールでブラストシールドの後ろに置いて使用すべきであり、ちなみに CH2Cl2 溶媒では使用しないでください。 皆さんは、気づかないうちにアジ化ナトリウムの近くで一日を過ごしているかもしれません。 加速度センサーが作動すると、NaN3は時速200マイル以上で窒素ガスを放出し、1/25秒でバッグを膨らませることができるのです。
Yay for azide salts!
via GIPHY
(ただし、この人にはならないように):
via GIPHY
肝心な点です。 ハロゲン化アルキルまたはスルホン酸塩とアジドとの間の SN2 反応は、おそらくハロゲン化アルキルから一級アミンを合成する唯一最良の方法である。 ガブリエル合成より確実に優れている。 アジド塩を用いた求核的アシル置換はアシルアジドを作る
SN2反応だけが私たちが探求してきた置換反応のタイプではありません。 求核的なアシル置換反応もあります。 4735>
機構の第一段階では、求核剤(Nu)がカルボニル炭素を攻撃し、C-Nuを形成してC-O(π)を切断します。 これにより四面体の中間体が生成する。 第2段階ではC-Oπ結合が再び形成され、炭素-(脱離基)結合が切断され、求核性アシル置換体が得られる。
ここで酸クロライドとN3イオンとの求核性アシル置換反応によりアシルアジドが得られる例を示す。 アシルアジドの転位。 Curtius転位
アシルアジドの最も一般的な用途は、加熱すると転位してイソシアナートを与えるCurtius転位と呼ばれる反応である。
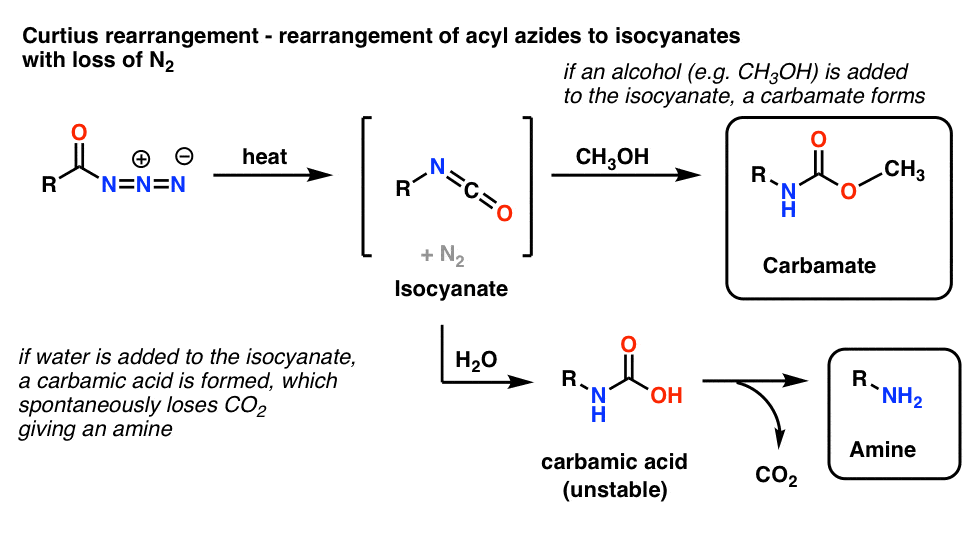
- メタノールなどのアルコール存在下で Curtius を行うと、カルバメートが生成します。
- 代わりに水を加えると、不安定なカルバミン酸が短時間生成し、これが二酸化炭素を失って 1級アミンを生成します。
芳香族カルボン酸を作る方法はたくさんありますが、芳香族環にC-N結合を形成する素晴らしい方法はそう多くありません。 例えば、安息香酸(p-メチル安息香酸など)を持っていて、(保護された)芳香族アミンを形成する必要があるとします。 Curtius プロトコルは、ニトロ化+還元に頼ることなく、環上に新しい C-N 結合を形成する良い方法です。
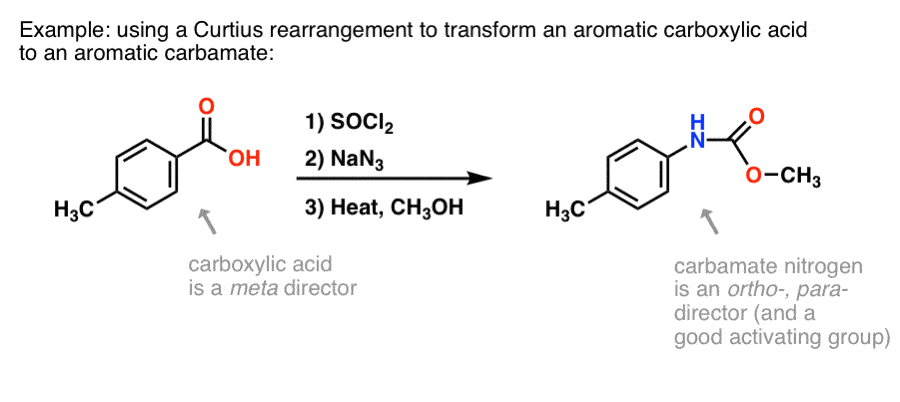
(この方法では、Baeyer-Villiger 酸化の窒素に相当するものと多少似ています。 )
アジド求核剤の他の例。 エポキシドの開口と共役付加
求核剤としてのアジドイオンのもう2つの応用には、エポキシドの開口(本質的にはSN2プロセスである-配置の反転に注意)と、α、β不飽和ケトンへの共役付加があります:
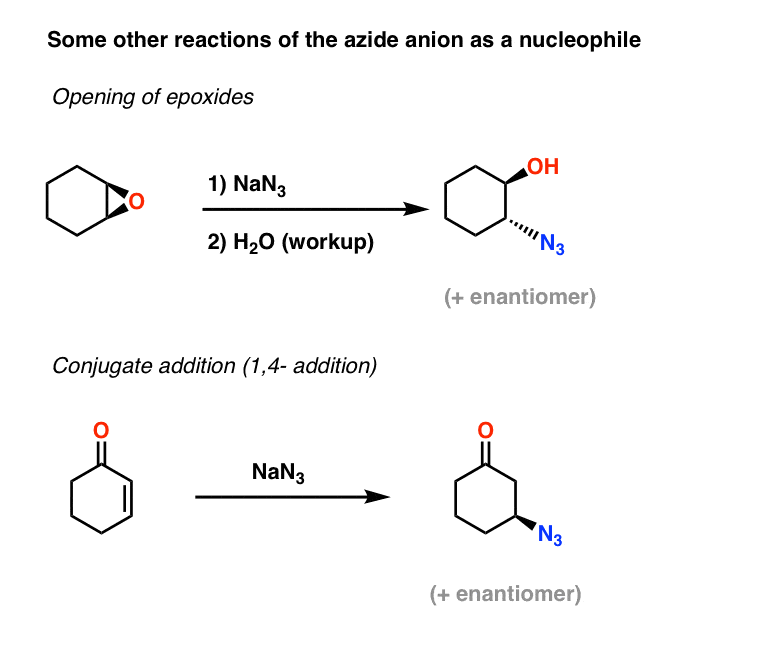
結果として生じるアルキルアジドは、上で説明した方法で1級アミンに還元することが可能です。
注記
脚注:アジド-アルキン環化付加反応、別名。 「クリック」化学
有機アジドの興味深く有用なアプリケーションは、まだ有機化学入門の教科書には載っていませんが (近い将来載るでしょう)、技術的には「銅触媒によるアジド-アルキン環化付加反応」と呼ばれ、より一般的には「アルキン-アジド クリック反応」と呼ばれている過程です。
末端アルキンを有機アジドの存在下で銅触媒で処理すると、速やかに環化付加反応が起こり、1,2,3-トリアゾールの生成につながる。
詳細は省きますが、この環形成反応は 6 個のπ電子を含み、ディールス アルダー反応と同類です (銅触媒版は技術的には協奏的プロセスではないが、非触媒版はそうであることを、お堅い人は正しく指摘するでしょう)
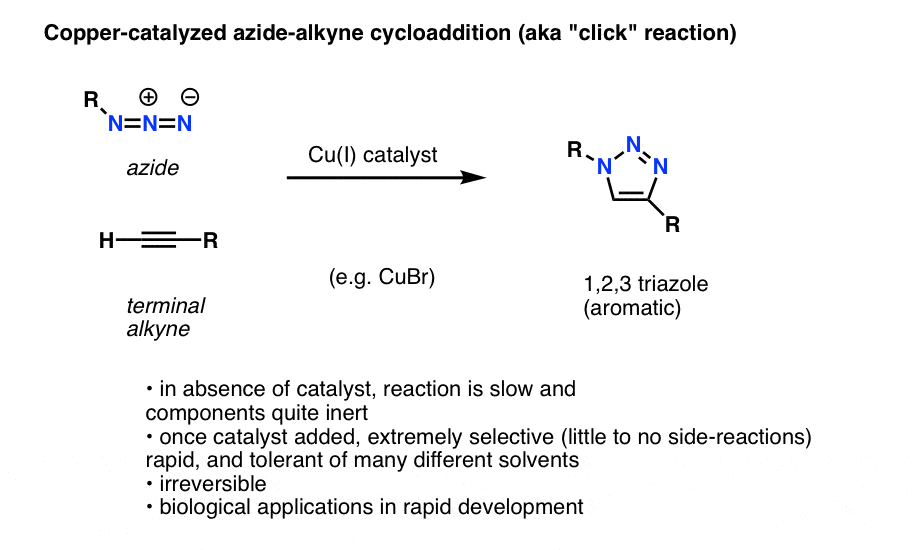
この反応はいくつかの理由で注目されています。
- 反応パートナー (末端アルキンと有機アジド) は、ほとんどの条件下で触媒がない場合、比較的不活性である。
- 銅を添加すると、穏やかな条件下で、さまざまな溶媒(水を含む)中で非常に速く反応が起こります。
- この条件下では、アルキンとアジドのパートナーは互いにのみ反応し、不可逆的に反応します。
- 生成物であるトリアゾール環は芳香族で安定である
これは、化学者が持つ反応の中で最も近いものの1つであり、2つの補完的なレゴブロックがスムーズに「一緒にクリック」するように反応するので、その考案者の1人、バリー・シャープレスによって「クリック」反応と呼ばれています。
この反応を最近特に有用にしているのは、アジドとアルキンのパートナーを生物学的に興味深い分子に設置し、必要なときに「クリック」して結合させることができる点です。
たとえば、
- 糖の 5′ 位置にアセチレンを、3′ 位置にアジドを置くことは、トリアゾールが有機リン酸を置き換える「クリックした」 DNA を作るために使用されています。
- 信じられないことに、あるグループは「クリックされた」DNAを作り、それを人間の細胞に入れ、メッセンジャーRNAで転写させることに成功しました。
- アジドを含むAZT(上)は、転写機構を混乱させることで機能します。 アジド・アルキンクリック反応を高速ゲノム解読に応用する方法を発見した賢い人たちがいる。
タカタは1990年代初頭にアジ化ナトリウムを使用し、その後テトラゾール、硝酸アンモニウムに移行しました。
硝酸アンモニウムはテトラゾールの約10分の1の価格だったと、業界の特許を見直したUphamは述べています。 しかし、硝酸アンモニウムには決定的な欠陥があり、それが他のエアバッグメーカーに見切りをつけさせることになったと彼は言う。 硝酸アンモニウムは、密度の異なる5つの相があり、長期間の安定性を保つのが難しいのだ。 硝酸アンモニウムを使った推進剤は、温度変化で膨張と収縮を繰り返し、最終的にはタブレットが粉になってしまうのです。 水や湿気があると、この過程が早くなる。 粉末は錠剤よりも早く燃えるので、推進剤が崩れたエアバッグは強引に展開される可能性が高い。 制御された爆発は、単なる爆発に終わってしまうのだ。 1990年代からエアバッグ業界を追い続け、現在はJSC Automotive Consultingのマネージングディレクターであるヨッヘン・シーベルトは、「誰もがある道を進み、タカタだけが別の道を進んだ」と語る。 1990年からエアバッグ業界を追い続け、現在はJSC Automotive Consultingのマネージングディレクターを務めるヨッヘン・シーベルトは、「当時の学会誌を読むと、”ダメだ、やめたほうがいい “と言っている人たちが実際にいることがわかる。 危険だ』と。 “
欠陥のあるエアバッグの破片により、世界中で13人が死亡、100人以上が負傷した。”
2017年6月25日、110億ドル以上の負債に直面したタカタは、破産を申請した。
Primary amine synthesis “Do’s and Don’ts” :
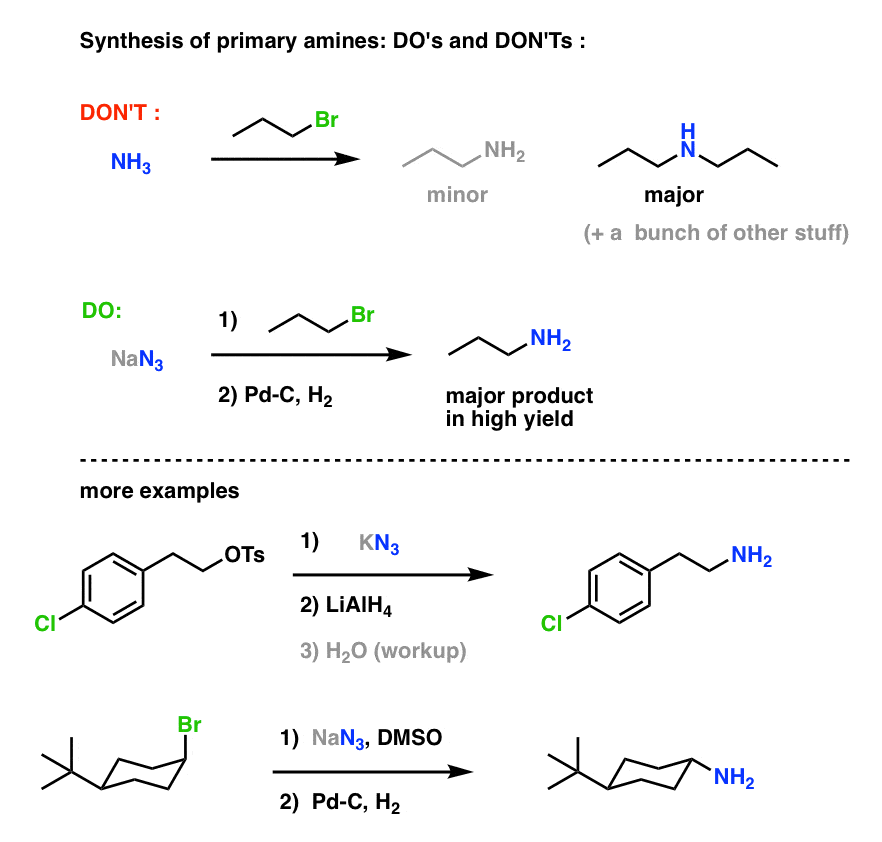
(Advanced) References and Further Read
Azide is useful in organic synthesis, and azide chemistry highlights are given in the reference below.は、有機合成においてアジド化合物が有用であることを示している。
- Nucleophilic reactivity of the azide ion in various solvents
Thanh Binh Phan, Herbert Mayr
Phys.Org.No. Chem. 2006, 19 (11), 706-713
DOI: 10.1002/poc.1063
ヘルベルト・マイヤー教授(LMU、ミュンヘン、ドイツ)は、親電子性、求核性の定量化、さまざまな求核剤、求電子剤の反応性を比較する尺度の開発など、基礎物理有機化学に貢献することにそのキャリアを費やしてきました。 - The SN2 displacements at 2-norbornyl brosylates
Klaus Banert and Wolfgang Kirmse
Journal of the American Chemical Society 1982, 104 (13), 3766-3767
DOI: 1021/ja00377a057 - An Improved Synthesis of Azidothymidine
I. Balagopala, A. P. Ollapally, & H. J. Lee
Nucleosides, Nucleotides & Nucleic Acids 1996, 4, 899-906
DOI: 10.1080/07328319608002136
Azides は SN2 反応における求核剤として使用することが可能です。 Ref. #3は、AZT(アジドチミジン)の合成にアジドイオンを用いた例である。 1から3を経由して5への変換はref. #7286> - Reduction of Organic Azides to Primary Amines with Lithium Aluminum Hydride
H. Boyer
Journal of the American Chemical Society 1951, 73 (12), 5865-5866
DOI: 10.1021/ja01156a507
The reduction of organic azides to primary amines is a convenient method for synthesis which is otherwise difficult to synthesively by standard methods. - The explosive sensitivity of the metal azides to impact
P. G. Fox
J. Solid State Chem. 1970, 2 (4), 491-502
DOI: 10.1016/0022-4596(70)90043-5
An investigation of the shock sensitivity of NaN3, TlN3, and Pb(N3)2.The Curtius Reaction
Smith, P. A. S. React. 1946, 3, 336
DOI: 10.1002/0471264180.or003.09
この転位の発見の歴史、基質範囲、限界、他の類似反応との比較、実験手順など、古いがCurtius反応の総合レビューである。 121. ヨウ化亜鉛触媒によるアロイルクロライドとトリメチルシリルアジドからのアロイルアジドの調製
K. Surya Prakash, Pradeep S. Iyer, Massoud Arvanaghi, and George A. Olah
The Journal of Organic Chemistry 1983 48 (19), 3358-3359
DOI: 10.1021/jo00167a051b
Nobel Laureate Professor George A. Olahから芳香族アリールアジドを容易に準備する手順を紹介したものです。 7286>
Epoxide opening and conjugate addition:
- CYCLOHEXENE IMINE (7-AZA-BICYCLOHEPTANE)
Iain D. G. Watson, Nicholas Afagh and Andrei K. Yudin
Org.No. Synth. 2010, 87, 161-169
DOI: 10.15227/orgsyn.087.0161
エポキシドをNH-アジリジン(エポキシドの窒素アナログ)に変換するシュタウディンガー反応であるため、特に有用な手順となります。 合成は厄介ですが、Organic Syntheses.の手順に合うように、ここで多くの詳細が提供されているので、再現可能です。 - Amine-Catalyzed Addition of Azide Ion to α,β-Unsaturated Carbonyl Compounds
David J. この論文は、初期の有機分子触媒反応であり、イミンまたはイミニウムイオン中間体を介して進行する可能性が高いため、興味深い内容となっています。 残念ながら、この用語は論文のどこにも使われていません。この著者らは、MacMillan教授を打ち負かすことができたはずです。 この論文では、イミン、イミウムイオン中間体という用語がどこにも使われていないのが残念です。 Int. Ed. 2001, 40 (11), 2004-2021
DOI: 10.1002/1521-3773(20010601)40:11<2004::AID-ANIE2004>3.0.CO;2-5
Cu触媒によるアジドとアルキンの付加環化は、ノーベル賞受賞教授によって「クリック反応」と呼ばれるようになった。 その簡便さ、高い収率、速い反応速度、幅広い条件と基質への適合性から、K. Barry Sharpless教授(The Scripps Research Institute, La Jolla, CA)により「クリック」反応と呼ばれています。 また、歪んだアルキン(例:シクロオクティン)を用いれば、銅を用いない反応も可能です。