9.1 Terminologie voor plantaardige oliën en dierlijke vetten
Vet is een algemene term voor lipiden, een klasse van verbindingen in de biochemie. U kent ze als vettige, vaste stoffen die u aantreft in dierlijke weefsels en in sommige planten – oliën die bij kamertemperatuur vaste stoffen zijn.
Groenteolie is het vet dat wordt gewonnen uit plantaardige bronnen. Wij kunnen olie uit andere delen van een plant halen, maar zaden zijn de belangrijkste bron van plantaardige olie. Plantaardige oliën worden meestal gebruikt bij het koken en voor industrieel gebruik. Vergeleken met water hebben oliën en vetten een veel hoger kookpunt. Er zijn echter plantaardige oliën die niet geschikt zijn voor menselijke consumptie, omdat de oliën uit deze soorten zaden een extra bewerking vereisen om onaangename smaken of zelfs giftige chemicaliën te verwijderen. Deze omvatten koolzaad- en katoenzaadolie.
Dierlijke vetten zijn afkomstig van verschillende dieren. Talg is rundvet en reuzel is varkensvet. Er is ook kippenvet, blubber (van walvissen), levertraan, en ghee (dat is een botervet). Dierlijke vetten hebben de neiging meer vrije vetzuren te bevatten dan plantaardige oliën.
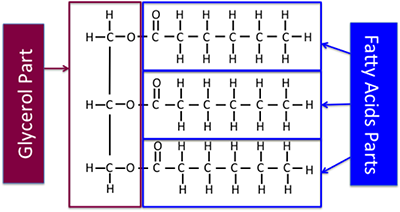
Chemisch worden vetten en oliën ook wel “triglyceriden” genoemd. Het zijn esters van glycerol, met een wisselend mengsel van vetzuren. Figuur 9.1 toont een algemeen diagram van de structuur zonder gebruik te maken van chemische formules.
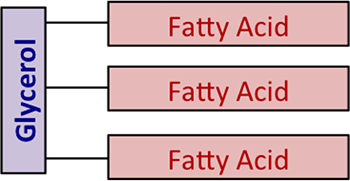
Wat is glycerol dan? Het is ook bekend als glycerine/glycerine. Andere namen voor glycerol zijn: 1,2,3-propaan-triol, 1,2,3-tri-hydroxy-propaan, glyceritol, en glycyl alcohol. Het is een kleurloze, reukloze, hygroscopische (d.w.z. trekt water aan), en zoet smakende viskeuze vloeistof. Figuur 9.2 toont de chemische structuur in twee verschillende vormen.
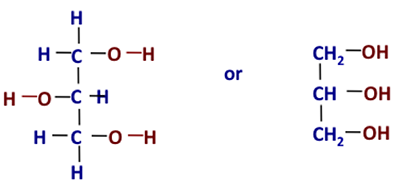
Nu moeten we dus definiëren wat de vetzuren zijn. In wezen zijn vetzuren lange-keten koolwaterstoffen met een carbonzuur. Figuur 9.3a toont de generieke chemische structuur van een vetzuur met het carbonzuur erop.

Figuur 9.3b toont verschillende chemische structuren van vetzuren. De chemische structuren worden weergegeven als lijnchemische structuren, waarbij elk punt op de schakels een koolstofatoom is en het juiste aantal waterstofatomen afhangt van de vraag of er sprake is van een enkele of dubbele binding. Vetzuren kunnen verzadigd (met waterstofbruggen) of onverzadigd (met enkele dubbele bindingen tussen koolstofatomen) zijn. Door de stofwisseling van oliehoudende gewassen bevatten natuurlijk gevormde vetzuren een even aantal koolstofatomen. In de organische scheikunde hebben koolstofatomen vier elektronenparen beschikbaar om te delen met een ander koolstof-, waterstof- of zuurstofatoom. Vrije vetzuren zijn niet gebonden aan glycerol of andere moleculen. Zij kunnen worden gevormd bij de afbraak of hydrolyse van een triglyceride.
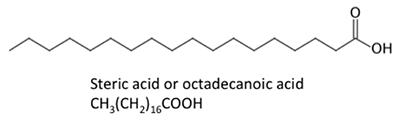
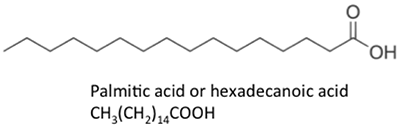
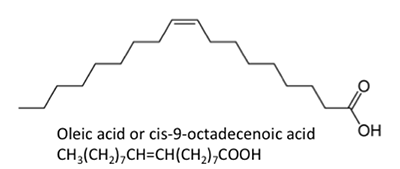
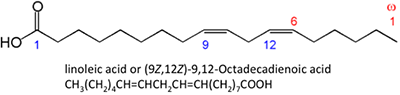
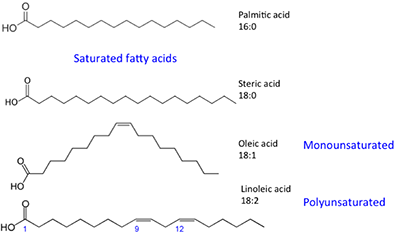
De afgebeelde vetzuren hebben enigszins verschillende eigenschappen. Palmitinezuur komt voor in palmolie. Figuur 9.4 toont het verband van elk vetzuur met zijn grootte en verzadiging. Palmitinezuur en sterinezuur zijn verzadigde vetzuren, terwijl oliezuur en linolzuur onverzadigde vetzuren zijn met verschillende hoeveelheden dubbele bindingen. Figuur 9.4 toont de verschillende hoeveelheden koolstofatomen ten opzichte van het aantal dubbele bindingen in de verbinding.
Figuur 9.5a toont het deel van de triglyceride dat een vetzuur is en het deel dat glycerol is, deze keer inclusief chemische structuren. De hier getoonde chemische structuur is een verzadigde triglyceride.
Zo, we hebben besproken wat vetten en oliën zijn. Nu, wat is biodiesel? Wat is ten minste één definitie? Het is een dieselbrandstof die is gemaakt van biomassa. Er zijn echter verschillende soorten biodiesel. Het meest bekende type biodiesel is een brandstof die bestaat uit monoalkylesters (meestal methyl- of ethylesters) van vetzuren met lange keten, afkomstig van plantaardige oliën of dierlijke vetten – dit is volgens ASTM D6551. Een ASTM is een document dat de normen bevat voor bepaalde soorten chemicaliën, met name industriële materialen. Dit is een breedsprakige definitie die ons niet echt laat zien wat het chemisch is.
Dus als we het over een alkylgroep hebben, is dat een eenwaardig radicaal dat alleen koolstof- en waterstofatomen in een koolwaterstofketen bevat, met een algemene atoomformule van CnH2n+1. Voorbeelden zijn:
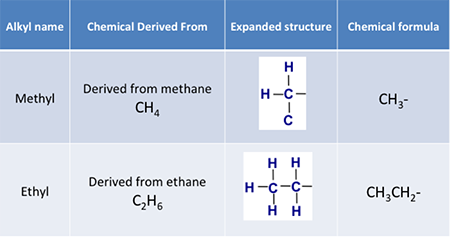
Een andere term die we moeten kennen is een ester. Esters zijn organische verbindingen waarbij een alkylgroep een waterstofatoom vervangt in een carbonzuur. Bijvoorbeeld, als het zuur azijnzuur is en de alkylgroep de methylgroep, dan wordt de resulterende ester methylacetaat genoemd. Bij de reactie van azijnzuur met methanol ontstaan methylacetaat en water; de reactie is hieronder weergegeven in figuur 9.6. Een ester die op deze wijze wordt gevormd is een condensatiereactie; deze wordt ook wel verestering genoemd. Deze esters worden ook wel carboxylaatesters genoemd.
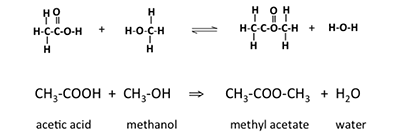
Dit is de basisreactie die helpt om biodiesel te vormen. Figuur 9.7 toont de verschillende onderdelen van de chemische structuur van de biodiesel, de methylester vetzuur, of vetzuurmethylester (FAME).
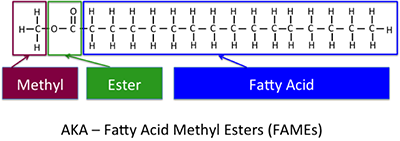
Zo, op dit punt, laten we ervoor zorgen dat we weten waar we het over hebben gehad. Biodiesel is een methyl- (of ethyl-)ester van een vetzuur. Het wordt gemaakt van plantaardige olie, maar het is geen plantaardige olie. 100% biodiesel staat bekend als B100 – het is een plantaardige olie die is omgeësterd om biodiesel te maken. Het moet voldoen aan de ASTM-biodieselnormen om in aanmerking te komen voor garanties en als biodiesel te worden verkocht en in aanmerking te komen voor eventuele belastingvoordelen. Meestal wordt het gemengd met diesel op petroleumbasis. Als het B2 is, bestaat het voor 2% uit biodiesel en voor 98% uit diesel op aardoliebasis. Andere mengsels zijn: B5 (5% biodiesel), B20 (20% biodiesel), en B100 (100% biodiesel). We zullen in het volgende hoofdstuk bespreken waarom mengsels worden gebruikt. En voor alle duidelijkheid: soms wordt plantaardige olie gebruikt in dieselmotoren, maar die kan na verloop van tijd prestatieproblemen veroorzaken en de motor aantasten. Soms worden plantaardige olie en alcohol gemengd in emulsies, maar dat is nog steeds geen biodiesel, omdat het andere eigenschappen heeft dan biodiesel.
Dus, als zuivere plantaardige olie (SVO) in een dieselmotor zal lopen, waarom zou je het dan niet gebruiken? Plantaardige olie is aanzienlijk viskeuzer (kleverig is een niet-technische term) en heeft slechtere verbrandingseigenschappen. Het kan leiden tot: koolaanslag, slechte smering in de motor, motorslijtage, en het heeft koude start problemen. Plantaardige oliën hebben natuurlijke gommen die verstoppingen in filters en brandstofinjectoren kunnen veroorzaken. En bij een dieselmotor wordt de injectietiming verstoord, wat kloppen van de motor kan veroorzaken. Er zijn manieren om deze problemen te verminderen, waaronder: 1) mengen met diesel op petroleumbasis (gewoonlijk < 20%), 2) de olie voorverwarmen, 3) microemulsies maken met alcoholen, 4) de plantaardige olie “kraken”, en 5) de methode gebruiken om SVO om te zetten in biodiesel met behulp van transesterificatie. Er worden ook andere methoden gebruikt, maar voor nu zullen wij ons richten op biodiesel uit omestering. Tabel 9.1 toont drie eigenschappen van dieselolie nr. 2, biodiesel en plantaardige olie. Zoals u kunt zien, is de belangrijkste verandering de viscositeit. No. 2 diesel en biodiesel hebben viscositeiten die vergelijkbaar zijn, maar plantaardige oliën hebben veel viscositeit en kunnen bij koud weer grote problemen veroorzaken. Dit is de belangrijkste reden om de SVO om te zetten in biodiesel.
| brandstof | Energie-inhoud (Btu/gal) |
Cetaangetal | Viscositeit (centistokes) |
|---|---|---|---|
| No. 2 Diesel | 140.000 | 48 | 3 |
| Biodiesel | 130.000 | 55 | 5.7 |
| Groenteolie | 130.000 | 50 | 45 |