Generieke naam: phendimetrazine tartraat
Doseringsvorm: tablet
Medisch beoordeeld door Drugs.com. Laatst bijgewerkt op 22 juni 2020.
- Overzicht
- Bijwerkingen
- Dosering
- Professioneel
- Interacties
- Meer
Rx only
De merknaam Bontril Slow Release is in de V.S. niet meer verkrijgbaar.S. Als generieke versies van dit product door de FDA zijn goedgekeurd, zijn er mogelijk generieke equivalenten beschikbaar.
- Bontril Beschrijving
- Bontril – Klinische farmacologie
- Indicaties en gebruik voor Bontril
- Contra-indicaties
- Waarschuwingen
- Voorzorgsmaatregelen
- Gedrugsinteracties
- Carcinogenese, mutagenese, aantasting van de vruchtbaarheid
- Pregatie
- Gebruik tijdens de zwangerschap
- Zorgende moeders
- Pediatrisch gebruik
- Bijwerkingen
- Drugsmisbruik en -afhankelijkheid
- Gereguleerde stof
- Dependence
- Overdosering
- Bontril Dosering en Toediening
- Gebruikelijke dosering voor volwassenen
- Hoe wordt Bontril geleverd
- PRINCIPAL DISPLAY PANEL – 35 mg Tablet Label
- Meer over Bontril Slow Release (phendimetrazine)
- Consumer resources
- Professionele hulpbronnen
- Gerelateerde behandelingsgidsen
Bontril Beschrijving
Phendimetrazine-tartraat, als dextro-isomeer, heeft als chemische naam (2S,3S)-3,4-dimethyl-2-fenylmorfoline L-(+)-tartraat (1:1).
De structuurformule is:
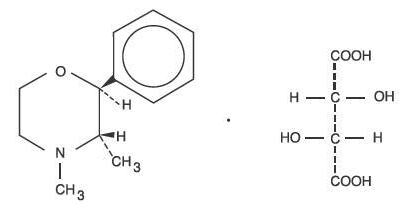
C12H17NO-C4H6O6 M.W. 341.36
Phendimetrazine-tartraat is een wit, reukloos kristallijn poeder. Het is goed oplosbaar in water; slecht oplosbaar in warme alcohol, onoplosbaar in chloroform, aceton, ether en benzeen.
Daarnaast zijn de volgende inactieve bestanddelen aanwezig: Samendrukbare Suiker, Suiker van de suikerbakker, D&C Geel #10, FD&C Blauw #1, FD&C Geel #6, Isopropyl Alcohol, Lactose Watervrij, Magnesium Stearaat, Microkristallijne Cellulose, Povidon, Gezuiverd Water, Natriumzetmeel Glycolaat.
Bontril – Klinische farmacologie
Phendimetrazine-tartraat is een sympathomimetisch amine met een farmacologische activiteit die vergelijkbaar is met die van de prototype-geneesmiddelen van deze klasse die bij obesitas worden gebruikt, de amfetaminen. De werking omvat stimulering van het centrale zenuwstelsel en verhoging van de bloeddruk. Tachyphylaxis en tolerantie zijn aangetoond bij alle geneesmiddelen van deze klasse waarbij naar deze verschijnselen is gezocht.
Drugs van deze klasse die bij zwaarlijvigheid worden gebruikt, staan algemeen bekend als “anorectica” of “anorexigenica”. Het staat echter niet vast, dat de werking van dergelijke geneesmiddelen bij de behandeling van zwaarlijvigheid in de eerste plaats een onderdrukking van de eetlust is. Andere werkingen van het centrale zenuwstelsel of metabolische effecten kunnen bijvoorbeeld een rol spelen.
Volwassen zwaarlijvige personen die een dieet volgen en met anorexigene geneesmiddelen worden behandeld, verliezen gemiddeld meer gewicht dan degenen die met placebo en dieet worden behandeld, zoals is vastgesteld in relatief kortlopende klinische trials.
De omvang van het toegenomen gewichtsverlies van met geneesmiddelen behandelde patiënten ten opzichte van met placebo behandelde patiënten is slechts een fractie van een pond per week. Het gewichtsverlies is het grootst in de eerste weken van de behandeling bij zowel geneesmiddelen als placebo’s en neemt in de daaropvolgende weken af. De mogelijke oorzaak van het toegenomen gewichtsverlies als gevolg van de verschillende medicijneffecten is niet vastgesteld. De hoeveelheid gewichtsverlies die gepaard gaat met het gebruik van een anorectisch geneesmiddel varieert van proef tot proef, en het toegenomen gewichtsverlies lijkt gedeeltelijk verband te houden met andere variabelen dan het voorgeschreven geneesmiddel, zoals de arts-onderzoeker, de behandelde populatie, en het voorgeschreven dieet. De studies laten geen conclusies toe over het relatieve belang van de medicamenteuze en niet-medicamenteuze factoren op het gewichtsverlies.
De natuurlijke geschiedenis van zwaarlijvigheid wordt gemeten in jaren, terwijl de aangehaalde studies beperkt zijn tot een paar weken; derhalve moet het totale effect van door medicatie veroorzaakt gewichtsverlies boven dat van een dieet alleen als klinisch beperkt worden beschouwd.
De belangrijkste eliminatieroute is via de nieren, waar het grootste deel van het medicijn en metabolieten worden uitgescheiden. Een deel van het geneesmiddel wordt gemetaboliseerd tot fenmetrazine en ook phendimetrazine-N-oxide. De gemiddelde eliminatiehalfwaardetijd bij onderzoek onder gecontroleerde omstandigheden is ongeveer 3,7 uur voor zowel de verlengde als de onmiddellijke afgiftevorm. De absorptiehalfwaardetijd van het geneesmiddel uit de onmiddellijk afgevende 35 mg phendimetrazine-tabletten is aanmerkelijk sneller dan de absorptiesnelheid van het geneesmiddel uit de verlengde-afgifteformulering.
Indicaties en gebruik voor Bontril
Bontril®PDM (phendimetrazine-tartraat) is geïndiceerd bij de behandeling van exogene zwaarlijvigheid als kortdurend adjunct (enkele weken) in een regime van gewichtsvermindering op basis van calorische restrictie bij patiënten met een aanvankelijke body mass index (BMI) van 30 kg/m2 of hoger die niet hebben gereageerd op een geschikte gewichtsverminderende behandeling (dieet en/of lichaamsbeweging) alleen. Hieronder staat een tabel met de Body Mass Index (BMI) gebaseerd op verschillende lichaamslengtes en gewichten. De BMI wordt berekend door het gewicht van de patiënt, in kilogram (kg), te delen door de lengte van de patiënt, in meter (m), in het kwadraat. Metrische conversies zijn als volgt: pounds ÷ 2,2 = kg; inches x 0,0254 = meter.
| BODY MASS INDEX (BMI), kg/m2 Hoogte (voeten, inches) |
||||||
|---|---|---|---|---|---|---|
| Gewicht (pounds) |
5’0″ | 5’3″ | 5’6″ | 5’9″ | 6’0″ | 6’3″ |
| 140 | 27 | 25 | 23 | 21 | 19 | 18 |
| 150 | 29 | 27 | 24 | 22 | 20 | 19 |
| 160 | 31 | 28 | 26 | 24 | 22 | 20 |
| 170 | 33 | 30 | 28 | 25 | 23 | 21 |
| 180 | 35 | 32 | 29 | 27 | 25 | 23 |
| 190 | 37 | 34 | 31 | 28 | 26 | 24 |
| 200 | 39 | 36 | 32 | 30 | 27 | 25 |
| 210 | 41 | 37 | 34 | 31 | 29 | 26 |
| 220 | 43 | 39 | 36 | 33 | 30 | 28 |
| 230 | 45 | 41 | 37 | 34 | 31 | 29 |
| 240 | 47 | 43 | 39 | 36 | 33 | 30 |
| 250 | 49 | 44 | 40 | 37 | 34 | 31 |
Phendimetrazine tartraat is alleen geïndiceerd voor gebruik als monotherapie.
Contra-indicaties
Bekende overgevoeligheid of idiosyncratische reacties op sympathomimetica.
Vergevorderde arteriosclerose, symptomatische cardiovasculaire aandoeningen, matige en ernstige hypertensie, hyperthyreoïdie en glaucoom.
Zeer nerveuze of geagiteerde patiënten.
Patiënten met een voorgeschiedenis van drugsmisbruik.
Patiënten die andere CNS-stimulantia innemen, waaronder monoamine oxidase remmers.
Waarschuwingen
Phendimetrazine tartraat dient niet te worden gebruikt in combinatie met andere anorectische middelen, waaronder voorgeschreven geneesmiddelen, receptvrije preparaten en kruidenproducten.
In een case-control epidemiologische studie werd het gebruik van anorectische middelen, waaronder phendimetrazine tartraat, in verband gebracht met een verhoogd risico op het ontwikkelen van pulmonale hypertensie, een zeldzame, maar vaak fatale aandoening. Het gebruik van anorectica gedurende meer dan drie maanden werd in verband gebracht met een 23-voudige toename van het risico op het ontwikkelen van pulmonale hypertensie. Een verhoogd risico op pulmonale hypertensie bij herhaalde kuren kan niet worden uitgesloten.
Het ontstaan of verergeren van inspanningsdyspneu, of onverklaarbare symptomen van angina pectoris, syncope, of oedeem van de onderste extremiteiten wijzen op de mogelijkheid van het optreden van pulmonale hypertensie. Onder deze omstandigheden dient fendimetrazine tartraat onmiddellijk te worden gestaakt, en dient de patiënt te worden geëvalueerd op de mogelijke aanwezigheid van pulmonale hypertensie.
Valvulaire hartziekte geassocieerd met het gebruik van sommige anorectica zoals fenfluramine en dexfenfluramine is gerapporteerd. Mogelijke bijdragende factoren zijn gebruik gedurende langere perioden, hoger dan de aanbevolen dosis, en/of gebruik in combinatie met andere anorectische geneesmiddelen. Er zijn echter geen gevallen van deze valvulopathie gemeld wanneer fendimetrazine-tartraat alleen is gebruikt.
Het potentiële risico van mogelijke ernstige bijwerkingen zoals valvulaire hartziekte en pulmonale hypertensie dient zorgvuldig te worden afgewogen tegen het potentiële voordeel van gewichtsverlies. Een baseline cardiale evaluatie dient te worden overwogen om reeds bestaande valvulaire hartziekten of pulmonale hypertensie op te sporen vóór de start van de behandeling met fendimetrazine. Phendimetrazine tartraat wordt niet aanbevolen bij patiënten met bekende hartruis of valvulaire hartaandoeningen. Echocardiogram tijdens en na de behandeling zou nuttig kunnen zijn voor het opsporen van eventuele valvulaire aandoeningen die kunnen optreden. Om ongerechtvaardigde blootstelling en risico’s te beperken, mag de behandeling met fendimetrazine-tartraat alleen worden voortgezet als de patiënt binnen de eerste 4 weken van de behandeling een bevredigend gewichtsverlies heeft (d.w.z. een gewichtsverlies van ten minste 4 pond, of zoals bepaald door de arts en de patiënt).
Tolerantie voor het anorectische effect van fendimetrazine ontwikkelt zich binnen enkele weken. Wanneer dit optreedt, moet het gebruik worden gestaakt; de maximaal aanbevolen dosis mag niet worden overschreden.
Gebruik van phendimetrazine-tartraat binnen 14 dagen na toediening van monoamine-oxidaseremmers kan leiden tot een hypertensieve crisis.
Onmiddellijk staken van de toediening na langdurige hoge dosering resulteert in extreme vermoeidheid en depressie. Vanwege het effect op het centrale zenuwstelsel kan fendimetrazine-tartraat het vermogen van de patiënt aantasten om deel te nemen aan potentieel gevaarlijke activiteiten zoals het bedienen van machines of het besturen van een motorvoertuig; de patiënt moet daarom dienovereenkomstig worden gewaarschuwd.
Phendimetrazine-tartraat wordt niet aanbevolen voor patiënten die in het voorafgaande jaar anorectische middelen hebben gebruikt.
Voorzorgsmaatregelen
Voorzichtigheid is geboden bij het voorschrijven van fendimetrazine aan patiënten met zelfs lichte hypertensie.
Insulinebehoefte bij diabetes mellitus kan worden gewijzigd in samenhang met het gebruik van fendimetrazine tartraat en het gelijktijdige dieetregime.
Phendimetrazine tartraat kan het hypotensieve effect van guanethidine verminderen. De minst haalbare hoeveelheid dient in één keer te worden voorgeschreven of verstrekt om de kans op overdosering te minimaliseren.
Gedrugsinteracties
De werkzaamheid van fendimetrazine tartraat met andere anorectische middelen is niet onderzocht en het gecombineerde gebruik kan de mogelijkheid van ernstige cardiale problemen hebben.
Carcinogenese, mutagenese, aantasting van de vruchtbaarheid
Er zijn geen studies met fendimetrazine-tartraat uitgevoerd om de carcinogene potentie, de mutagene potentie of de effecten op de vruchtbaarheid te evalueren.
Pregatie
Zwangerschapscategorie C
Er is geen onderzoek gedaan naar de voortplanting bij dieren met fendimetrazine-tartraat. Het is ook niet bekend of fendimetrazine tartraat schade aan de foetus kan veroorzaken wanneer het wordt toegediend aan een zwangere vrouw of het voortplantingsvermogen kan beïnvloeden.
Gebruik tijdens de zwangerschap
Veilig gebruik tijdens de zwangerschap is niet vastgesteld. Totdat meer informatie beschikbaar is, dient fendimetrazine-tartraat niet te worden ingenomen door vrouwen die zwanger zijn of zwanger kunnen worden, tenzij, naar de mening van de arts, de mogelijke voordelen opwegen tegen de mogelijke gevaren.
Zorgende moeders
Het is niet bekend of dit geneesmiddel wordt uitgescheiden in de moedermelk. Omdat veel geneesmiddelen worden uitgescheiden in de moedermelk, dient fendimetrazine-tartraat niet te worden ingenomen door vrouwen die borstvoeding geven, tenzij naar de mening van de arts de mogelijke voordelen opwegen tegen de mogelijke gevaren.
Pediatrisch gebruik
De veiligheid en werkzaamheid bij pediatrische patiënten zijn niet vastgesteld.
Bijwerkingen
Cardiovasculair: Palpitatie, tachycardie, verhoogde bloeddruk, ischemische voorvallen.
Valvulaire hartaandoeningen geassocieerd met het gebruik van sommige anorectische middelen zoals fenfluramine en dexfenfluramine, zowel onafhankelijk als vooral bij gebruik in combinatie met andere anorectische middelen, zijn gerapporteerd. Er is echter geen geval van deze valvulopathie gemeld wanneer fendimetrazine-tartraat alleen is gebruikt.
Centraal Zenuwstelsel: Overstimulatie, rusteloosheid, slapeloosheid, agitatie, blozen, tremor, zweten, duizeligheid, hoofdpijn, psychotische toestand, vertroebeling van het gezichtsvermogen.
Gastro-intestinaal: Droogheid van de mond, misselijkheid, diarree, constipatie, maagpijn.
Genitourinair: Urinefrequentie, dysurie, veranderingen in libido.
Drugsmisbruik en -afhankelijkheid
Gereguleerde stof
Bontril® PDM (phendimetrazine-tartraat) is een Gereguleerde stof van Schedule lll.
Dependence
Phendimetrazine-tartraat is chemisch en farmacologisch verwant aan de amfetamines. Amfetaminen en verwante stimulerende middelen zijn op grote schaal misbruikt, en de mogelijkheid van misbruik van fendimetrazine moet in gedachten worden gehouden bij het evalueren van de wenselijkheid om een middel op te nemen als onderdeel van een programma voor gewichtsvermindering. Misbruik van amfetaminen en verwante drugs kan gepaard gaan met een sterke psychologische afhankelijkheid en ernstig sociaal disfunctioneren. Er zijn meldingen van patiënten die de dosering hebben verhoogd tot vele malen de aanbevolen dosering. Abrupt stoppen na langdurige toediening van hoge doses leidt tot extreme vermoeidheid en mentale depressie; er worden ook veranderingen waargenomen op het slaap EEG. Manifestaties van chronische intoxicatie met anorectica zijn onder meer ernstige dermatosen, uitgesproken slapeloosheid, prikkelbaarheid, hyperactiviteit en persoonlijkheidsveranderingen. De ernstigste manifestatie van chronische intoxicaties is psychose, klinisch vaak niet te onderscheiden van schizofrenie.
Overdosering
Een acute overdosering met fendimetrazine-tartraat kan zich uiten door de volgende tekenen en symptomen: ongewone rusteloosheid, verwardheid, opvliegendheid, hallucinaties, en paniektoestanden. Vermoeidheid en depressie volgen gewoonlijk op de centrale stimulatie. Cardiovasculaire effecten zijn onder meer hartritmestoornissen, hypertensie of hypotensie en collaps van de bloedsomloop. Gastro-intestinale symptomen zijn misselijkheid, braken, diarree en buikkrampen. Vergiftiging kan leiden tot convulsies, coma en de dood.
De behandeling van overdosering is grotendeels symptomatisch. Het omvat sedatie met een barbituraat. Bij duidelijke hypertensie moet het gebruik van een nitraat of een snelwerkend alfa-receptorblokkerend middel worden overwogen. De ervaring met hemodialyse of peritoneale dialyse is onvoldoende om aanbevelingen voor het gebruik ervan te kunnen doen.
Bontril Dosering en Toediening
Gebruikelijke dosering voor volwassenen
1 tablet (35 mg) tweemaal daags of driemaal daags een uur voor de maaltijd.
Dosering dient te worden geïndividualiseerd om een adequate respons te verkrijgen met de laagste effectieve dosering. In sommige gevallen kan een ½ tablet (17,5 mg) per dosis voldoende zijn. De dosering mag niet hoger zijn dan 2 tabletten driemaal daags.
Hoe wordt Bontril geleverd
Drievoudig groen, wit en geel tablet met “B 35” op de gescoorde zijde en de letter “V” op de andere. Bontril® PDM-tabletten met 35 mg fendimetrazine-tartraat zijn verkrijgbaar in flesjes van 100 (NDC 0187-0497-01) en 1000 (NDC 0187-0497-02).
Opslaan bij 25°C (77°F); uitstappen toegestaan tot 15°C-30°C (59°F-86°F).
DEA Bestelformulier vereist.
Gedistribueerd door:
Valeant Pharmaceuticals North America
One Enterprise
Aliso Viejo, CA 92656 USA
Gebereid door:
Mallinckrodt, Inc.
Hobart, NY 13788
Gedrukt met inkt van levensmiddelenkwaliteit.
MG #20886
Rev. 10/07
Part No. L2BB01
PRINCIPAL DISPLAY PANEL – 35 mg Tablet Label
NDC 0187-0497-02
RX Only
CIII
Bontril® PDM
(phendimetrazine tartraat tabletten, USP)
35 mg
Elke drielagige
groene, wit en geel
tablet bevat 35 mg
fendimetrazine
tartraat
1000
tabletten
VALEANT™
| Bontril PDM fendimetrazine tartraat tablet |
||||||||||||||||||||||||||
|
||||||||||||||||||||||||||
|
||||||||||||||||||||||||||
|
||||||||||||||||||||||||||
|
||||||||||||||||||||||||||
|
||||||||||||||||||||||||||
|
||||||||||||||||||||||||||
Etiketteerder – Valeant Pharmaceuticals International (042230623)
| Establishment | |||
| Name | Adres | ID/FEI | Operations |
| MALLINCKRODT INC | 957414238 | MANUFACTURE(0187-0497) | |
Meer over Bontril Slow Release (phendimetrazine)
- Side Effecten
- Tijdens Zwangerschap
- Doseringsinformatie
- Gebruiksafbeeldingen
- Gebruiksinteracties
- 35 Reviews
- Gebruiksklasse: anorexiants
Consumer resources
- Patient Information
- Bontril (Advanced Reading)
- Bontril Slow-(Advanced Reading)
Professionele hulpbronnen
- Voorschrijfinformatie
- Phendimetrazine (AHFS Monograph)
Andere merken Fendique ER
Gerelateerde behandelingsgidsen
- Obesitas
Medische disclaimer