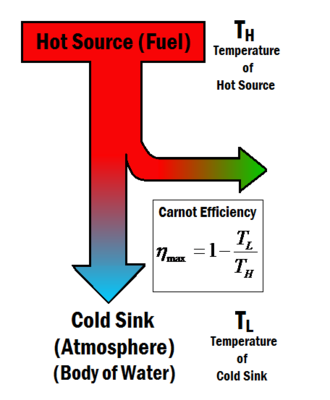
Figuur 1: Een hete bron levert de energie die nodig is om arbeid te produceren in een thermodynamisch proces. Het Carnot-rendement hangt alleen af van de temperatuur van de hete bron en de koude put.
Het Carnot-rendement beschrijft het maximale thermische rendement dat een warmtemotor kan bereiken, zoals toegestaan door de tweede wet van de thermodynamica. De wet werd in 1824 door Sadi Carnot afgeleid. Carnot dacht na over het idee van het maximale rendement in een warmtemotor en vroeg zich af of het rendement van een warmtemotor 100% kan benaderen, of dat er een bovengrens is die niet kan worden overschreden. Het antwoord bleek te zijn dat er een maximumwaarde is, en Carnot ontwikkelde een ideale motor die theoretisch dit rendement zou geven, bekend als de Carnotmotor. Het maximale rendement, bekend als het Carnotrendement , is alleen afhankelijk van de temperaturen van de hete bron en de koude gootsteen en , zoals weergegeven in figuur 1, en wordt gegeven door de onderstaande vergelijking
(1)
De tweede wet vereist dat afvalwarmte wordt geproduceerd in een thermodynamisch proces waarbij arbeid wordt verricht door een warmtebron. Een dergelijk proces wordt gegeven door de vergelijking
(2)
Met een thermisch rendement van
(3)
Waar:
- de warmte is die aan het systeem wordt geleverd door een brandstof
- de warmte is die door het systeem wordt afgegeven aan de koudeput die bekend staat als afvalwarmte
- de nuttige arbeid is die door het systeem wordt verricht
Het Carnotrendement geeft dus een maximaal haalbare hoeveelheid arbeid van een willekeurige warmtemotor. Uit vergelijking 1 blijkt dat het rendement kan worden verhoogd of verlaagd door het te verhogen of te verlagen. Idealiter zou men daarom de temperatuur van de koudeput gelijk willen stellen aan het absolute nulpunt, maar het is bekend dat dit onmogelijk is. In werkelijkheid is de koudeput de omgeving van de aarde. Dit betekent dat de “cold sink” een temperatuur heeft van ongeveer 280-300 Kelvin, en dat de hete bronnen afkomstig zijn van brandstoffen die branden bij een temperatuur van ongeveer 1100 Kelvin (hoewel onderzoek steeds probeert die temperatuur hoger te krijgen). Deze temperaturen geven een Carnot rendementswaarde van ongeveer.
Carnotmotor
Een Carnotmotor is een geïdealiseerde motor, die gebruik maakt van processen die omkeerbare mechanische en thermische interacties hebben. Dit betekent dat de motor zijn bewegingen kan doormaken en naar zijn begintoestand kan terugkeren zonder toename van entropie (zonder energieverlies). Om de motor in staat te stellen naar zijn begintoestand terug te keren zonder dat de entropie toeneemt, moet de motor gedurende zijn gehele cyclus in thermisch evenwicht zijn. De voorwaarden voor het bestaan van een dergelijke motor zijn:
- Mechanische interacties: er gaat geen energie verloren in de vorm van wrijving, daarom is er geen warmteoverdracht tijdens deze mechanische processen (), bekend als een adiabatisch proces.
- Thermische interacties: de warmteoverdracht is oneindig traag (bekend als een quasi-statisch). Dit betekent dat het temperatuurverschil tussen het systeem en de toegevoerde/afgevoerde warmte vrijwel gelijk is, waardoor de warmteoverdracht in oneindig lange tijd plaatsvindt. Deze uitwisselingen moeten plaatsvinden door de inwendige temperatuur van het systeem constant te houden, wat bekend staat als een isotherm proces.
Een motor die alleen deze eigenschappen bezit, staat bekend als een Carnot-motor, die een “perfect omkeerbare motor” is, en het maximale thermische rendement () en, indien hij als een koelkast werkt, prestatiecoëfficiënt () vertoont. Hoewel een dergelijke motor de efficiëntie zou maximaliseren, is hij in termen van doeltreffendheid vreselijk onpraktisch omdat de geïdealiseerde processen zoveel tijd vergen om een aanzienlijke hoeveelheid werk te leveren. Zoals Schroeder het stelt, “doe geen moeite om een Carnot motor in je auto te installeren; hoewel het je brandstofverbruik zou verhogen, zou je voorbij worden gelopen door voetgangers”.
Om meer te weten te komen over de Carnot motor, bezoek NASA of hyperphysics.