Spasmele palpebrale și faciale pot avea un impact semnificativ asupra calității vieții unui pacient, dar ajungerea la cauza principală a spasmului – poate fi miokimie, blefarospasm esențial benign sau spasm hemifacial – poate fi o provocare pentru clinician. În acest articol, vă vom oferi sfaturi care vă pot ajuta să diagnosticați și să gestionați aceste afecțiuni uneori dificile.
O privire de ansamblu
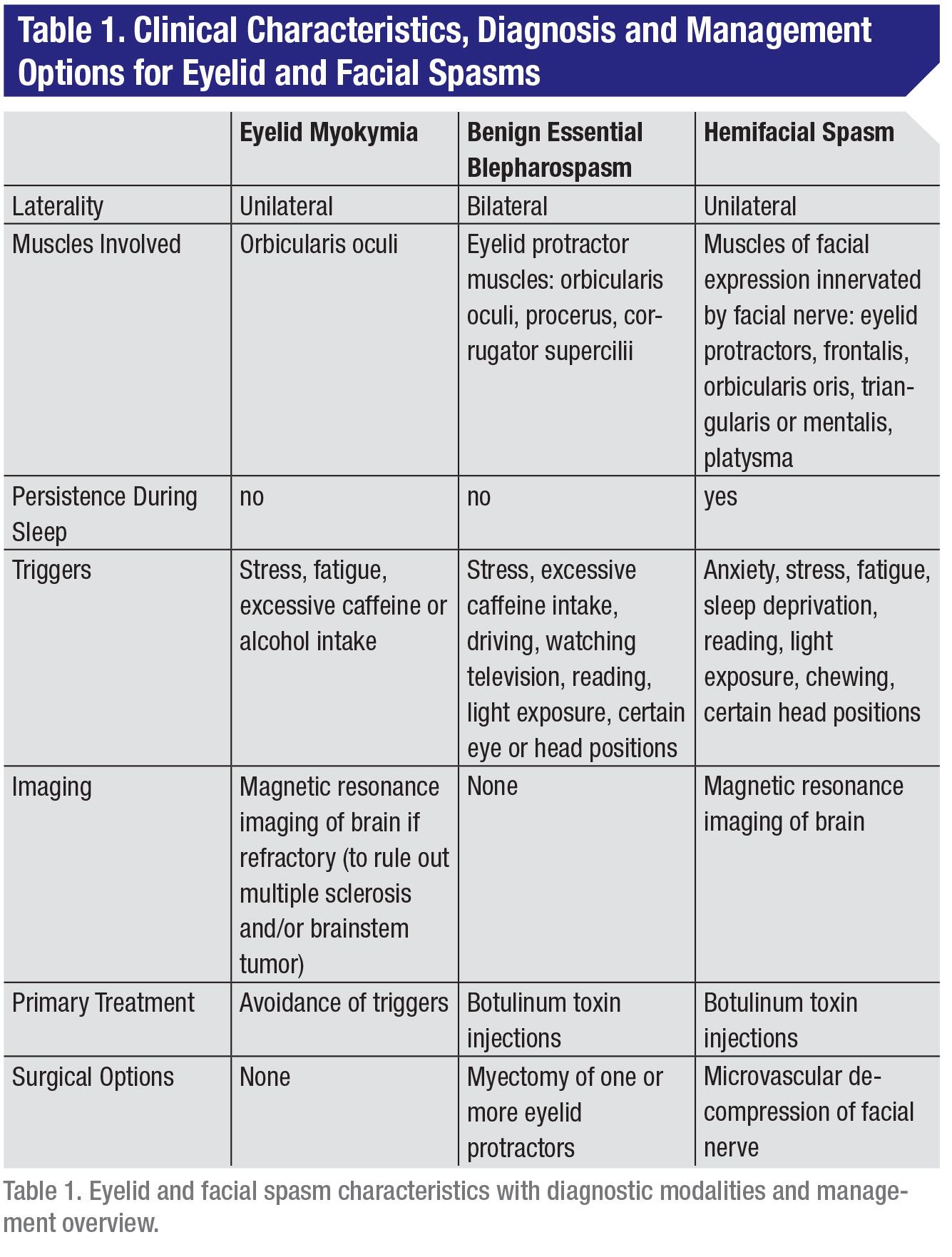
În cadrul practicii neurologice și oftalmologice, clasificat de la cel mai puțin la cel mai grav, spectrul spasmelor palpebrale și faciale include miokimia palpebrală (contracții involuntare, mici, ale pleoapei), blefarospasmul esențial benign (spasme involuntare care determină închiderea parțială sau completă a ochiului) și spasmul hemifacial (spasme la nivelul mușchilor care controlează expresiile faciale) (Tabelul 1). Toate aceste tulburări constau în mișcări faciale involuntare care pot fi dificil de gestionat de către pacienți în viața de zi cu zi.
Miochimia pleoapelor
Cea mai frecventă tulburare de mișcare facială involuntară este miochimia pleoapelor. Miochimia pleoapelor constă în contracții involuntare, fine, continue, ondulatorii, nesincronizate, ale fibrelor musculare striate ale protractorilor pleoapelor. În electrofiziologie, se caracterizează prin descărcarea spontană asincronă a unităților motorii adiacente în dublete sau triplete la o rată de 30 până la 70 Hertz, cu intervale de 100 până la 200 ms care separă descărcările individuale.2,3 Miokimia palpebrală este considerată un proces benign, autolimitat, care este unilateral și intermitent, cu pleoapa inferioară afectată mai mult decât cea superioară. Episoadele sunt tranzitorii, durând de la câteva zile până la câteva săptămâni sau luni, spasmele apărând intermitent pe parcursul zilei, până la câteva ore la un moment dat.4
Factorii declanșatori includ stresul, epuizarea, consumul excesiv de cofeină sau de alcool și efortul fizic.5 Eliminarea acestor factori declanșatori este recomandată ca parte a tratamentului. Miokimia palpebrală este cel mai frecvent izolată la mușchiul orbicularis oculi, dar se poate răspândi la mușchii suplimentari ai uneia sau ambelor părți ale feței, caz în care este denumită miokimie facială.2
Miokimia facială este cauzată de leziuni ale nucleului nervului facial din pons în urma unor boli demielinizante, cum ar fi scleroza multiplă, sau de compresia cauzată de tumori ale trunchiului cerebral. Rareori, miokimia persistentă a pleoapelor a fost raportată ca semn de prezentare a sclerozei multiple sau a unei tumori de trunchi cerebral.3 Dacă afecțiunea este cronică, refractară la eliminarea factorilor declanșatori și afectează calitatea vieții pacientului, injecțiile cu toxină botulinică pot avea succes în tratament. Mecanismul și eficacitatea injecțiilor cu toxină botulinică sunt discutate pe larg în secțiunea următoare. Miokimia persistentă a pleoapelor, refractară la tratamentele de mai sus, trebuie să ridice suspiciunea pentru o leziune a trunchiului cerebral, așa cum a fost descrisă mai sus, și justifică o analiză cu ajutorul imagisticii prin rezonanță magnetică.
Blefarospasmul esențial benign
BEB a fost descris pentru prima dată în 1857 ca o tulburare de spasme involuntare ale mușchilor protractori ai pleoapelor care are ca rezultat închiderea parțială sau completă a pleoapelor. BEB are o incidență de 1,4 până la 13,3 cazuri la 100.000, afectează femeile de trei ori mai des decât bărbații și apare cel mai adesea în deceniile cinci-șapte de viață.7,8 BEB este cel mai frecvent o tulburare sporadică, dar s-a raportat că 27 la sută dintre pacienți au un membru al familiei cu distonie, sugerând o posibilă componentă genetică.1
Patofiziologia BEB nu este bine înțeleasă. Studiile de tomografie cu emisie de pozitroni și de imagistică prin rezonanță magnetică funcțională au arătat activarea regiunilor cerebrale implicate în controlul și reglarea mușchilor responsabili de clipit, inclusiv talamusul, striatum, cortexul vizual anterior, cortexul motor primar și cerebelul superior.7,9Studiile pe animale au arătat că epuizarea dopaminei în substantia nigra scade inhibiția reflexului trigemenului de clipit, ceea ce duce la o hipersensibilitate a acestui reflex ca răspuns la lumină și la uscăciune.10 Factorii care incită la BEB includ stresul, consumul excesiv de cofeină, condusul, privitul la televizor, cititul, luminile puternice, aerul poluat, vântul, zgomotul și anumite mișcări ale ochilor și ale capului.11,12
Prezentarea clinică a BEB constă în spasme involuntare bilaterale ale unuia sau mai multora dintre mușchii protractori ai pleoapelor, inclusiv mușchii orbicularis oculi, procerus și corrugator, cu simptome care variază de la o rată ușor crescută a clipitului până la închiderea forțată a pleoapelor care poate duce la orbire funcțională.1 Simptomele BEB nu persistă în timpul somnului și este o afecțiune progresivă în care mușchi suplimentari sunt implicați în timp.7 Un subgrup de pacienți poate prezenta spasme la nivelul feței medii sau inferioare, o afecțiune denumită sindromul Meige.1 Un subgrup suplimentar de pacienți poate dezvolta apraxia deschiderii pleoapelor, în care există o pierdere a coinhibiției între protractorii și retractorii pleoapelor, ceea ce duce la o incapacitate neparalitică de a deschide pleoapele în absența spasmului muscular.1
Pacienții se plâng, de asemenea, adesea de simptomul senzorial de fotofobie. Mecanismele propuse pentru fotofobie includ o tulburare de durere întreținută simpatic, pentru care blocurile ganglionare cervicale superioare au oferit ușurare în rapoarte anterioare.11 Opțiunile suplimentare de management pentru controlul fotofobiei includ modularea fotocromatică cu lentile colorate FL-41 sau lentile de contact sclerale cu fluoresceină în rezervorul de lichid, ambele crescând intensitatea luminii tolerate de pacienții BEB.13
Tratamentul de elecție pentru BEB este reprezentat de injecțiile cu toxină botulinică în mușchii protractori ai pleoapelor afectați. Toxina botulinică inhibă eliberarea de acetilcolină de la terminalul presinaptic al joncțiunii neuromusculare, blocând capacitatea unui mușchi injectat de a se contracta. Există șapte serotipuri de toxină botulinică (de la A la G). Tipurile A și B sunt aprobate de Administrația pentru Alimente și Medicamente a SUA pentru utilizare clinică în Statele Unite. OnabotulinumtoxinaA (Botox) a fost aprobată de FDA pentru tratamentul BEB în 1989 și este cea mai frecvent utilizată formulare, deși incobotulinumtoxinaA, abobotulinumtoxinaA și rimabotulinumtoxinaB sunt, de asemenea, autorizate pentru utilizare.14 Injecțiile sunt necesare aproximativ la fiecare trei până la patru luni.11 FDA recomandă o doză inițială de 1,25 până la 2,5 unități injectate în fiecare situs afectat, cu o doză maximă de 15 unități și trei situsuri de injectare pe fiecare parte.14 Cu toate acestea, sondajele au arătat că chirurgii oculoplasticieni au tendința de a trata BEB cu o doză inițială medie de 22,5 ±9,5 unități.14
În mod obișnuit, se injectează între cinci și opt locuri în jurul fiecărui ochi, fără a se injecta mai mult de 0,1 ml de toxină botulinică în fiecare loc pentru a preveni difuzarea medicamentului în mușchii adiacenți.12 Clinicienii trebuie să aibă grijă să injecteze medial și lateral atunci când tratează porțiunea pretarsală a mușchiului orbicularis oculi din pleoapele superioare, pentru a evita injectarea în mușchiul levator palpebrae superioris, ceea ce poate duce la ptoză. În mod similar, la nivelul pleoapei inferioare, injecțiile sunt efectuate central și lateral pentru a evita injectarea în oblicul inferior, ceea ce ar duce la diplopie. Incidența efectelor adverse ale injecțiilor cu toxină botulinică pentru pacienții BEB a fost raportată ca fiind de aproximativ 20 la sută, incluzând echimoze la locul de injectare, ochi uscat, lăcrimare, senzație de corp străin, lagoftalmie, diplopie și ptoză.7
Alte medicamente care au fost utilizate în tratamentul BEB includ antipsihotice, antiepileptice, anxiolitice, antidepresive, antihistaminice, sedative și stimulente, deși niciunul nu s-a dovedit a avea o eficacitate pe termen lung.15 În special, agoniștii dopaminei și inhibitorii recaptării dopaminei s-au dovedit a fi eficienți în reducerea spasmelor pleoapelor, dat fiind faptul că deficitul de dopamină a fost implicat în patogeneza BEB.11 Metilfenidatul, care blochează recaptarea presinaptică a dopaminei și a norepinefrinei, s-a dovedit a reduce spasmele pleoapelor și scorul de dizabilitate.11 Pacienții cu BEB au prezentat un răspuns parțial la agoniști ai acidului gama-aminobutiric, cum ar fi benzodiazepinele, dar utilizarea lor este limitată de efectul secundar de somnolență.11
Când BEB este refractar la tratamentul medical sau când un pacient nu poate tolera injecțiile cu toxină botulinică, poate fi luată în considerare intervenția chirurgicală cu miectomie. Obiectivele principale ale acestei proceduri sunt reducerea severității spasmului și creșterea intervalului de timp necesar între injecțiile cu botulinum.11 În cazul miectomiei chirurgicale, unul sau mai mulți mușchi protractori sunt rezecați. O miectomie limitată implică rezecția doar a unei părți a mușchiului orbicularis oculi din pleoapa superioară, față de o miectomie extinsă în care corrugatorul supercilii și protractorul sunt îndepărtați suplimentar.15
Efectele adverse ale intervenției chirurgicale includ o cosmesis slabă și necesitatea unor intervenții chirurgicale suplimentare. Recurența simptomelor după miectomia chirurgicală a fost raportată ca variind între 30 și 50 la sută din cazuri după șase luni.12 O procedură alternativă implică secționarea nervului facial, care denervează în mod eficient protractorii pleoapelor, dar are ca rezultat secundar paralizia nervului facial și, prin urmare, este rar utilizată.15

Spasmul semifacial
În sfârșit, HFS este o tulburare involuntară unilaterală a mișcărilor faciale care implică spasme ale mușchilor de expresie facială inervați de nervul facial. Incidența estimată este de aproximativ 10 cazuri la 100.000, pe baza unor studii din Minnesota și Norvegia.16,17 HFS tinde să apară în deceniul patru sau cinci al vieții, femeile fiind afectate de două până la trei ori mai des decât bărbații, iar populațiile asiatice mai frecvent afectate decât cele caucaziene.18 Până la o treime dintre pacienți raportează factori agravanți pentru HFS, inclusiv anxietatea, stresul, oboseala, privarea de somn, cititul, expunerea la lumină, mestecatul sau anumite poziții ale capului.18 HFS este adesea diagnosticat greșit ca fiind funcțional sau psihogenic (în 38% din cazuri), ticuri (în 29%) și paralizie a nervului facial (în 9%).19 Prezentarea clinică implică spasme inițiale ale mușchiului orbicularis oculi, care progresează sau se răspândesc treptat în timp pentru a implica alți mușchi de pe o jumătate a feței, cum ar fi mușchiul frontal, orbicularis oris, triangularis sau mentalis și chiar mușchiul platysma.7,18 Simptomele HFS pot persista în timpul somnului, în timp ce cele ale BEB nu.
Patofiziologia HFS implică compresia nervului facial la nivelul zonei de ieșire a rădăcinii sale (REZ) din trunchiul cerebral, care a fost descrisă pentru prima dată în 1947.20 Compresia poate fi cauzată de vase aberante, inclusiv artera cerebelară inferioară anterioară, artera cerebelară inferioară posterioară, artera bazilară, artera vertebrală; malformații arteriovenoase; și, foarte rar, de tumori, cum ar fi schwannomii acustice, meningioamele, tumorile glandei parotide și astrocitoamele pilocite.7 În timp ce diagnosticul de HFS este în primul rând clinic, RMN trebuie obținut întotdeauna pentru a exclude compresia nervului facial, așa cum s-a descris mai sus. Testele electromiografice pot fi, de asemenea, efectuate pentru a demonstra un răspuns patognomonic de răspândire laterală a impulsurilor între fibrele vecine ale nervului facial („transmisie efaptică”).20
Principalul tratament pentru HFS sunt injecțiile cu toxină botulinică, așa cum a fost descris mai sus pentru BEB. Pentru HFS, se injectează cinci până la 10 locuri pe partea afectată a feței, cu doze totale de onabotulinumtoxinăA variind între 10 și 34 de unități pe tratament.20 Tratamentul definitiv pentru HFS este decompresia microvasculară neurochirurgicală (MVD) pentru a ușura compresia nervului facial la nivelul REZ al acestuia. În studiile anterioare, aproximativ 95 la sută dintre pacienții care au fost supuși MVD pentru HFS au obținut rezultate bune sau chiar excelente, cu efecte adverse incluzând paralizia nervului facial la 19 la sută, deficite de auz la 7 la sută și paralizii ale nervilor cranieni inferiori la 2,8 la sută.21 Având în vedere caracterul invaziv și riscurile asociate cu efectuarea unei intervenții neurochirurgicale, este extrem de important să aveți o discuție sinceră cu pacienții cu privire la riscurile și beneficiile MVD față de injecțiile cu toxină botulinică, sau o combinație a celor două, pentru gestionarea HFS.
Tratamentul definitiv pentru spasmul hemifacial este decompresia microvasculară neurochirurgicală (MVD) pentru a ușura compresia nervului facial în zona de ieșire a rădăcinii sale.
În concluzie, spasmele palpebrale și faciale reprezintă un spectru de tulburări involuntare ale mișcărilor faciale care pot avea un impact sever asupra calității vieții și bunăstării psihologice a pacienților. În timp ce evitarea factorilor incitanți este recomandată în management, injecțiile cu toxină botulinică au apărut ca tratament de primă linie, în special pentru BEB și HFS. Cu toate acestea, terapia chirurgicală pentru BEB și HFS poate fi urmărită în cazurile refractare sau la pacienții intoleranți la injecțiile cu toxină botulinică. Având în vedere diagnosticarea frecventă eronată a acestor afecțiuni, este important ca medicii să fie familiarizați cu cele mai frecvente semne și simptome de prezentare pentru a pune în legătură acești pacienți cu neurologii sau oftalmologii pentru o evaluare și un tratament mai amănunțit. RECENZIE
Dr. Gervasio este rezident în oftalmologie la Wills Eye Hospital. Dr. Moster este medic curant în cadrul Serviciului de Neuro-Oftalmologie de la Wills și profesor de neurologie și oftalmologie la Universitatea Thomas Jefferson din Philadelphia. El este președinte al secției de neuro-oftalmologie la Einstein Medical Center din Philadelphia.
1. Hwang CJ, Eftekhari K. Blefarospasm esențial benign: Ce știm și ce nu știm. Int Ophthalmol Clin 2018;58:1:11-24.
2. Miller NR. Miochimia pleoapelor. Surv Ophthalmol 2011;56:3:277-8.
3. Barmettler A, Dinkin MJ, Lelli GJ. Miochimia pleoapelor: Nu întotdeauna benignă. Orbit 2011;30:6:289-90.
4. Jordan DR, Anderson RL, Thiese SM. Miochimia orbiculară intratabilă: Alternative de tratament. Ophthalmic Surg 1989;20:4:280-3.
5. Horowitz SH. Spasmul hemifacial și miokimia facială: Constatări electrofiziologice. Muscle Nerve 1987;10:422-427.
6. Mackenzie W. Caz de fotofobie și blefarospasm intens și de lungă durată, ameliorat prin inhalarea de cloroform. Med Chir Trans 1857;40:175-178.
7. Ozzello DJ, Giacometti JN. Toxine botulinice pentru tratarea blefarospasmului esențial și a spasmului hemifacial. Int Ophthalmol Clin 2018;58:1:49-61.
8. Bradley EA, Hodge DO, Bartley GB. Blefarospasm esențial benign în rândul locuitorilor din Olmsted County, Minnesota, 1976-1995: Un studiu epidemiologic. Ophthal Plast Reconstr Surg 2003;19:177-181.
9. Baker RS, Andersen AH, Morecraft RJ, et al. Un studiu de imagistică prin rezonanță magnetică funcțională la pacienții cu blefarospasm esențial benign. J Neuroophthalmol 2003;23:11-15.
10. Schicatano EJ, Basso MA, Evinger C. Modelul animal explică originile distoniei craniene a blefarospasmului esențial benign. J Neurophysiol 1997;77:2842-2846.
11. Yen MT. Evoluții în tratamentul blefarospasmului esențial benign. Curr Opin Ophthalmol 2018;29:440-44.
12. Coscarelli JM. Blefarospasm esențial. Semin Ophthalmol 2010;25:3:104-8.
13. Herz NL, Yen MT. Modularea fotofobiei senzoriale în blefarospasmul esențial cu lentile cromatice. Ophthalmology 2005;112:2208-2211.
14. Broadbent TJ, Wesley RE, Mawn LA. Un sondaj al modelelor actuale de tratament al blefarospasmului în rândul chirurgilor oculoplasticieni. Ophthalmic Plast Reconstr Surg 2016;32:1:24-7.
15. Ben Simon GJ, McCann JD. Blefarospasmul esențial benign. Int Ophthalmol Clin 2005;45:49-75.
16. Auger RG, Whisnant JP. Spasmul hemifacial în Rochester și Olmsted County, Minnesota, 1960 până în 1984. Arch Neurol 1990;47:1233-34.
17. Nilsen B, Le KD, Dietrichs E. Prevalența spasmului hemifacial în Oslo, Norvegia. Neurology 2004;63:1532-33.
18. Lefaucheur JP, Daamer NB, Sangla S, Guerinel CL. Diagnosticul spasmului hemifacial primar. Neurochiurgie 2018;64:2:82-86.
19. Martinez AR, Nunes MD, Immich ND, et al. Diagnosticul greșit al spasmului hemifacial este un eveniment frecvent în mediul de îngrijire primară. Arq Neuropsiquiatr 2014;72:119-22.
20. Campbell E, Keedy C. Spasm hemifacial: O notă asupra etiologiei în două cazuri. J Neurosurg 1947;4:342-47.
21. Huh R, Han IB, Han IB, Moon JY, et al. Decompresie microvasculară pentru spasm hemifacial: Analize ale complicațiilor operatorii la 1582 de pacienți consecutivi. Surg Neurol 2008;69:153-57.
.