Wissenschaft >Chemie > Elemente der dritten Reihe >Metallischer Charakter der Elemente der dritten Reihe
In diesem Artikel werden wir die Tendenz im metallischen Charakter der Elemente der dritten Reihe untersuchen.
Metallischer Charakter:
Die Tendenz eines Atoms, Elektronen zu verlieren, um ein positiv geladenes Ion zu bilden, wird als metallischer Charakter oder elektropositiver Charakter bezeichnet. Typischerweise glänzen Metalle und sind gute Wärme- und Stromleiter.
Nichtmetallischer Charakter:
Die Tendenz eines Atoms, Elektronen zu gewinnen und negativ geladene Ionen zu bilden, wird als nichtmetallischer Charakter oder elektronegativer Charakter bezeichnet.
Faktoren, die den metallischen und nicht-metallischen Charakter beeinflussen:
- Größe eines Atoms
- Ionisierungsenthalpie
- Kernladung
Trends im metallischen und nicht-metallischen Charakter:
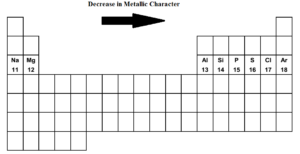
Wenn wir uns im Periodensystem von links nach rechts bewegen, d. h.d. h. von Natrium bis Argon in der dritten Periode nimmt der metallische Charakter ab und der nichtmetallische Charakter zu. Natrium, Magnesium und Aluminium sind typische Metalle. Silizium ist metalloid. (schwach nichtmetallisch). Phosphor, Schwefel und Chlor sind Nichtmetalle. Argon ist ein inertes Gas.
Natrium ist das metallischste Element, während Chlor das nichtmetallischste Element ist. Die beiden extremen Elemente Natrium und Chlor sind extrem reaktiv. Argon ist weder elektropositiv noch elektronegativ.
Wissenschaftliche Begründungen:
Wenn wir uns im Periodensystem von links nach rechts bewegen, d.h. von Natrium zu Argon in der dritten Periode, nimmt der metallische Charakter ab und der nichtmetallische Charakter zu.
Wenn wir uns in der dritten Periode von links nach rechts bewegen, nimmt die Ordnungszahl weiter zu. Wenn wir uns also von Natrium zu Argon bewegen, nimmt die Kernladung zu, und von links nach rechts wird ein zusätzliches Elektron zu demselben, d.h. dritten Orbit, hinzugefügt. Durch die Erhöhung der Kernladung nimmt die Anziehungskraft auf die Elektronen in der äußersten Umlaufbahn zu und somit nimmt die Größe des Atoms ab.
Wenn wir uns in der dritten Periode von links nach rechts bewegen, nimmt die Ionisierungsenthalpie zu. Von links nach rechts in der dritten Periode nimmt die Elektronegativität zu, d.h. die Tendenz, Elektronen zu verlieren, nimmt ab und die Tendenz, Elektronen zu gewinnen, nimmt zu. Wenn wir uns in der dritten Periode von links nach rechts bewegen, nimmt die Anzahl der Valenzen zu. Wenn wir uns also im Periodensystem von links nach rechts bewegen, d.h. von Natrium bis Argon in der dritten Periode, nimmt der metallische Charakter ab und der nichtmetallische Charakter zu.
Natrium, Magnesium und Aluminium sind typische Metalle.
Der metallische und nichtmetallische Charakter der Elemente hängt von ihrer Atomgröße, ihrer Kernladung und ihrem Ionisierungspotential ab. Natrium, Magnesium und Aluminium haben die Ordnungszahlen 11, 12 bzw. 13. Sie enthalten 1, 2, 3 Valenzelektronen in ihrer äußersten Schale.
Im Vergleich zu den anderen Elementen der dritten Reihe sind ihre Atomgrößen größer. Entsprechend sind auch die Kernladungen geringer. Dadurch ist die Anziehungskraft auf die Valenzelektronen geringer. Im Vergleich zu den anderen Elementen der dritten Reihe sind ihre Ionisierungsenthalpien geringer. Daher neigen diese Elemente dazu, ihre Valenzelektronen zu verlieren. Daher sind Natrium, Magnesium und Aluminium typische Metalle.
Phosphor, Schwefel und Chlor sind Nichtmetalle.
Die metallischen und nichtmetallischen Eigenschaften der Elemente hängen von ihrer Atomgröße, ihrer Kernladung und ihrem Ionisierungspotential ab. Phosphor, Schwefel und Chlor haben die Ordnungszahlen 15, 16 bzw. 17. Sie enthalten 5, 6, 7 Valenzelektronen in ihrer äußersten Schale.
Im Vergleich zu den anderen Elementen der dritten Reihe sind ihre Atomgrößen kleiner. Entsprechend sind auch die Kernladungen größer. Dadurch ist die Anziehungskraft auf die Valenzelektronen größer. Im Vergleich zu den anderen Elementen in der dritten Reihe sind ihre Ionisierungsenthalpien höher. Daher neigen diese Elemente nicht dazu, ihre Valenzelektronen zu verlieren, sondern Elektronen zu gewinnen. Daher sind Phosphor, Schwefel und Chlor Nichtmetalle.
Argon ist weder ein elektropositives noch ein elektronegatives Element.
Die metallischen und nichtmetallischen Eigenschaften der Elemente hängen von ihrer Atomgröße, ihrer Kernladung und ihrem Ionisierungspotential ab. Argon hat die Ordnungszahl 18. Es enthält 8 Valenzelektronen in seiner äußersten Schale. Argon hat ein komplettes Oktett und vollständig gefüllte s- und p-Orbitale, so dass es die stabilste Elektronenkonfiguration der Elemente der dritten Reihe hat, die nicht durch die Aufnahme oder den Verlust eines Elektrons gestört wird.
Im Vergleich zu anderen Elementen der dritten Reihe sind seine Atomgrößen größer, aber der Effekt der gefüllten s- und p-Orbitale ist dominierend. Im Vergleich zu den anderen Elementen der dritten Reihe ist seine Ionisierungsenthalpie am höchsten. Die Tendenz von Argon, Valenzelektronen zu verlieren oder zu gewinnen, ist daher fast nicht vorhanden. Daher ist Argon weder ein elektropositives noch ein elektronegatives Element.
Natrium ist das metallischste Element.
Die metallischen und nichtmetallischen Eigenschaften der Elemente hängen von ihrer Atomgröße, ihrer Kernladung und ihrem Ionisierungspotential ab. Natrium hat die Ordnungszahl 11. Es enthält 1 Valenzelektron in seiner äußersten Schale.
Im Vergleich zu den anderen Elementen der dritten Reihe ist seine Atomgröße größer. Entsprechend ist auch die Kernladung geringer. Dadurch ist die Anziehungskraft auf das Valenzelektron geringer. Im Vergleich zu den anderen Elementen in der dritten Reihe ist seine Ionisierungsenthalpie am niedrigsten. Daher neigt Natrium dazu, sein Valenzelektron zu verlieren. Daher ist Natrium das metallischste Element.
Chlor ist das nicht-metallische Element.
Die metallischen und nichtmetallischen Eigenschaften der Elemente hängen von ihrer Atomgröße, ihrer Kernladung und ihrem Ionisierungspotential ab. Chlor hat die Ordnungszahl 17. Es enthält 7 Valenzelektronen in seiner äußersten Schale.
Im Vergleich zu den anderen Elementen der dritten Reihe ist seine Atomgröße die kleinste. Entsprechend ist auch die Kernladung höher. Dadurch ist die Anziehungskraft auf die Valenzelektronen größer. Im Vergleich zu den anderen Elementen in der dritten Reihe ist seine Ionisierungsenthalpie am höchsten. Chlor neigt also nicht dazu, seine Valenzelektronen zu verlieren, sondern Elektronen zu gewinnen. Daher ist Chlor das am wenigsten metallische Element.