Wetenschap > Scheikunde > Derde Rij Elementen >Metallische Karakter van Derde Rij Elementen
In dit artikel zullen we de trend im metallische karakter van derde rij elementen bestuderen.
Metallische eigenschap:
De neiging van een atoom om elektronen te verliezen en een positief geladen ion te vormen, wordt zijn metallische of elektropositieve eigenschap genoemd. Typisch metalen tonen glans en zijn goede geleiders van warmte en elektriciteit.
Niet-metallisch karakter:
De neiging van een atoom om elektronen te winnen en zo een negatief geladen ion te vormen, wordt zijn niet-metallisch karakter of elektronegatief karakter genoemd.
Factoren die metallische en niet-metallische eigenschappen beïnvloeden:
- Grootte van een atoom
- Ionisatie-enthalpie
- Nucleaire lading
Trends in metallische en niet-metallische eigenschappen:
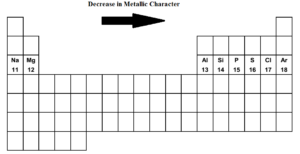
Als we van links naar rechts over het periodiek systeem gaan, d.w.z.d.w.z. van natrium naar argon in de derde periode neemt het metaalkarakter af en het niet-metaalkarakter toe. Natrium, magnesium, aluminium zijn typische metalen. Silicium is een metalloïde. (zwak niet-metallisch). Fosfor, zwavel, chloor zijn niet-metalen. Argon is een inert gas.
Natrium is het meest metallische element terwijl chloor het meest niet-metallische element is. Zowel de extreme elementen natrium als chloor zijn uiterst reactief. Argon is noch elektropositief, noch elektronegatief.
Wetenschappelijke redenen:
Zo lang het periodiek systeem van links naar rechts gaat, d.w.z. van natrium naar Argon in de derde periode, neemt het metaalkarakter af en het niet-metaalkarakter toe.
Zo lang het atoomnummer in de derde periode van links naar rechts gaat, neemt het atoomnummer toe. Dus als we van natrium naar argon gaan, neemt de nucleaire lading toe en van links naar rechts wordt een extra elektron toegevoegd aan dezelfde, d.w.z. derde baan. Door de toename van de kernlading neemt de aantrekkingskracht op de elektronen in de buitenste baan toe en neemt de omvang van het atoom af.
Naarmate we in de derde periode van links naar rechts gaan, neemt de ionisatie-enthalpie toe. Van links naar rechts in de derde periode neemt de elektronegativiteit toe, d.w.z. dat de neiging om elektronen te verliezen afneemt en de neiging om elektronen te winnen toeneemt. Als we van links naar rechts gaan in de derde periode neemt het valentiegetal toe. Naarmate men dus in het periodiek systeem van links naar rechts gaat, d.w.z. van natrium naar Argon in de derde periode, neemt het metaalkarakter af en het niet-metaalkarakter toe.
Natrium, Magnesium, Aluminium zijn typische metalen.
Metallische en niet-metallische karakters van de elementen hangen af van hun atoomgrootte, kernlading en ionisatiepotentiaal. Natrium, magnesium, aluminium hebben respectievelijk de atoomnummers 11, 12, 13. Zij bevatten 1, 2, 3 valentie-elektronen in hun buitenste schil.
Vergeleken met de andere elementen van de derde rij is hun atoomgrootte groter. Evenzo zijn de nucleaire ladingen ook minder. Hierdoor is de aantrekkingskracht op de valentie-elektronen kleiner. In vergelijking met andere elementen in de derde rij zijn hun ionisatie-enthalpie lager. Deze elementen hebben dus de neiging hun valentie-elektronen te verliezen. Vandaar dat natrium, magnesium, aluminium typische metalen zijn.
Fosfor, zwavel, chloor zijn niet-metalen.
Metallische en niet-metallische karakters van de elementen hangen af van hun atoomgrootte, kernlading en ionisatiepotentiaal. Fosfor, zwavel en chloor hebben respectievelijk de atoomnummers 15, 16 en 17. Zij bevatten 5, 6, 7 valentie-elektronen in hun buitenste schil.
Vergeleken met de andere elementen van de derde rij is hun atoomgrootte kleiner. Ook de nucleaire ladingen zijn groter. Hierdoor is de aantrekkingskracht op de valentie-elektronen groter. Vergeleken met andere elementen in de derde rij zijn hun ionisatie-enthalpie hoger. De neiging van deze elementen is dus niet om hun valentie-elektronen te verliezen, maar om elektronen te winnen. Vandaar dat fosfor, zwavel en chloor niet-metalen zijn.
Argon is noch elektropositief, noch elektronegatief.
De metaalachtige en niet-metaalachtige eigenschappen van de elementen hangen af van hun atoomgrootte, kernlading en ionisatiepotentiaal. Argon heeft atoomnummer 18. Het bevat 8 valentie-elektronen in de buitenste schil. Argon heeft een volledig octet en volledig gevulde s- en p-banen, zodat het de meest stabiele elektronische configuratie van de elementen van de derde rij heeft, die niet wordt verstoord door het aanvaarden of verliezen van een elektron.
Vergeleken met de andere elementen van de derde rij is de atoomgrootte groter, maar het effect van gevulde s- en p-banen overheerst. Vergeleken met de andere elementen in de derde rij is de ionisatie-enthalpie het hoogst. De neiging van Argon om valentie-elektronen te verliezen of te winnen is dus vrijwel afwezig. Daarom is Argon noch een elektropositief, noch een elektronegatief element.
Natrium is het meest metallische element.
De metallische en niet-metallische eigenschappen van de elementen hangen af van hun atoomgrootte, kernlading en ionisatiepotentiaal. Natrium heeft atoomnummer 11. Het bevat 1 valentie-elektron in zijn buitenste schil.
Vergeleken met de andere elementen in de derde rij is zijn atoomgrootte groter. Evenzo is de kernlading ook kleiner. Hierdoor is de aantrekkingskracht op het valentie-elektron minder. Vergeleken met de andere elementen in de derde rij is de ionisatie-enthalpie het laagst. De neiging van natrium is dus om zijn valentie-elektron te verliezen. Vandaar dat Natrium het meest metallische element is.
Chloor is het meest niet-metallische element.
Metallische en niet-metallische eigenschappen van de elementen hangen af van hun atoomgrootte, kernlading en ionisatiepotentiaal. Chloor heeft atoomnummer 17. Het bevat 7 valentie-elektronen in zijn buitenste schil.
Vergeleken met de andere elementen van de derde rij is zijn atoomgrootte het kleinst. Ook de kernlading is groter. Hierdoor is de aantrekkingskracht op de valentie-elektronen groter. Vergeleken met de andere elementen in de derde rij is zijn ionisatie-enthalpie het hoogst. De neiging van chloor is dus niet om zijn valentie-elektronen te verliezen, maar om elektronen te winnen. Vandaar dat Chloor het meest niet-metallische element is.